AUMENTO DE LA FRAGMENTACIÓN DEL DNA ESPERMÁTICO EN LOS FUMADORES TRAS LA CAPACITACIÓN MEDIANTE SWIM-UP
Thamara Viloria1, Nicolás Garrido1, José Luis Fernández2, José Remohí1, Antonio Pellicer1, Lourdes Muriel2, Marcos Meseguer1 1IVI Valencia, Universidad de Valencia. 2Sección de Genética y Unidad de Investigación, Hospital "Teresa Herrera," Complejo Hospitalario Universitario Juan Canalejo, A Coruña. 3Departamento de Obstetricia y Ginecología Hospital Dr. Peset, Valencia.
email: tviloria@ivi.es
Resumen: los hábitos tóxicos y su relación con la infertilidad masculina, ha sido objeto de investigación en los últimos años y dentro de los hábitos tóxicos más comunes dentro de la población está fumar el cigarrillo. Por otro lado, la fragmentación del DNA espermático ha sido relacionada con la infertilidad y disminución de la calidad embrionaria en trabajos previos. Este estudio se ha llevado a cabo con la finalidad de investigar la asociación entre el tabaco y la fragmentación del DNA espermático en muestras de semen fresco y capacitado en hombres infértiles que asisten para un tratamiento de reproducción. Un total de 99 pacientes proporcionaron una muestra de semen; se descartaron previamente otras causas de fragmentación del DNA mediante un cuestionario y se establecieron 3 grupos de acuerdo al consumo de tabaco: no fumadores, fumadores moderados (1-19 cigarrillos/día) y muy fumadores (≥20 cigarrillos/día). El análisis de la fragmentación se llevó a cabo mediante la prueba de la Dispersión de la Cromatina (SCD) antes y después del swim-up. No se observaron diferencias significativas en cuanto a la fragmentación del DNA según el hábito de fumar en las muestras en fresco; sin embargo, hubo un incremento significativo de células espermáticas con el DNA fragmentado en los hombres fumadores respecto a los no fumadores en las muestras luego del swim-up. Por lo que podemos concluir que el análisis de la fragmentación del DNA espermático después del capacitado es el que puede realmente detectar el efecto perjudicial producido por el tabaco sobre el espermatozoide. Este efecto nocivo altera el proceso de selección del swim-up en los fumadores, sin embargo, las bases moleculares y celulares de este fenómeno no han sido elucidadas, por tanto es recomendable que los hombres que buscan descendencia eviten el consumo de tabaco.
Palabras clave: Fragmentación del DNA / Prueba de Dispersión de la Cromatina (SCD) / fertilización in vitro /
cigarrillo/ espermatozoide
SPERM SELECTION BY SWIM-UP IN TERMS OF DNA FRAGMENTATION AS MEASURED BY THE SPERM CHROMATIN DISPERSION TEST (SCD) IS ALTERED IN HEAVY SMOKERS
Abstract: Toxic habits and its relation with male infertility has been a matter of investigation in the recent years and smoking is one of the commonest life-style toxic exposures to harmful substances. Sperm DNA fragmentation has been previously linked to infertility and low embryo quality in several works. This cross-sectional study was carried out to investigate the association between cigarette smoking and sperm DNA fragmentation in raw and capacitated sperm from infertile males undergoing assisted reproduction treatments (ART). A total number of 99 infertile males provided one semen sample, other causes of DNA fragmentation was discarded by a previous questionnaire and three groups were established according to the cigarette consumption: non-smokers, light smokers(1-19 cigarettes/day) and heavy smokers (≥20 cigarettes/day), then analyses of the sperm DNA fragmentation was carried out by the Sperm Chromatin Dispersion (SCD) test before and after swim-up treatment. We could observed no differences in the sperm DNA fragmentation in the raw semen samples regardless the smoking habits; nevertheless there is a significant increase in the incidence of sperm cells with DNA strand breaks in male smokers compare to non smokers after the evaluation of post swim-up samples. And we concluded that the analysis of sperm DNA fragmentation after capacitation can really detect the detrimental effect produced by tobacco. This deleterious effect alters the sperm swim-up selective process in smokers but molecular and cellular basis of this phenomenon remain to be elucidated, but based on these evidences, leaving smoking is advisable in males attending to reach parenthood.
Key words: DNA fragmentation / sperm chromatin dispersion test (SCD) / In vitro Fertilization / cigarette smoking / sperm
INTRODUCCIÓN
El término “Infertilidad” se define como la incapacidad de una pareja de conseguir un embarazo luego de relaciones sexuales regulares no protegidas. Aproximadamente un 15% de las parejas con deseo de gestación tienen dificultad de concebir tras este período. El factor masculino es por sí solo el causante de esa infertilidad en un 20% de los casos y contribuye en otro 30-40%, siendo las alteraciones en el semen el origen de la misma (Rodríguez et al., 2005).
El sistema reproductivo es bastante complejo, sin embargo, los diseños experimentales de pruebas in vitro e in vivo nos pueden ser útiles para detectar algunas alteraciones. Por tanto, la reproducción asistida nos brinda un espacio ideal para estudiar algunos factores que podrían estar afectando la calidad seminal y sus implicaciones a nivel reproductivo.
A lo largo de los años, muchos han sido los factores relacionados a la infertilidad masculina, como: infecciones, varicocele (Pomerol, 2002), obstrucciones y alteraciones en la producción espermática (Ballescá, 2002), causas genéticas (Egozcue, 2002) y muchas veces la causa es desconocida y pueden afectar en mayor o menor medida a la calidad seminal. Sin embargo, su relación con los hábitos tóxicos ha sido motivo de investigación en los últimos años, de sus resultados se han descrito algunos agentes ambientales tóxicos que pueden deteriorar la espermatogénesis, ejerciendo efectos nocivos a nivel pretesticular, testicular o post-testicular (Oliva et al., 2001; Pflieger-Bruss et al., 2004). Uno de estos agentes es el consumo del tabaco; el cual está ampliamente reconocido como un problema de salud pública y una de las mayores causas de muertes prevenibles. Aproximadamente una tercera parte de la población mundial mayor de 15 años es fumadora (World Health Organization, 1997). Así mismo, el tabaco afecta la salud reproductiva. El cigarrillo contiene algunos cientos de compuestos (Dube and Green,1982). El tabaco consiste en su mayoría de carbohidratos y proteínas (aprox 50%). Otro constituyente significante son alcaloides (0,5-5%) con la nicotina como compuesto predominante (90-95% de los alcaloides totales), polifenoles (0,5-4,5%), fitoteroles (0,1- 2,5%), ácidos carboxílicos (0,1- 0,7%), hidrocarbonos aromáticos, aldehídos, cetonas, aminas, pesticidas, etc (0,01-5%) y más de 30 compuestos metálicos (Wynder and Hoffmann, 1967; Internacional Agency for Research on Cancer, 1986).
La nicotina, el principal alcaloide del tabaco, está presente en los cigarrillos en una cantidad que varía desde 0,8- 1,8 mg/cigarrillo, dependiendo de la marca y tamaño del mismo (Benowitz et al., 1983; Rosa et al., 1992). Tanto como 1mg de nicotina puede ser absorbido al fumar 1 solo cigarrillo. Este es un alcaloide muy tóxico que se absorbe rápidamente por el tracto respiratorio, la mucosa bucal y la piel (Gandini et al., 1997).
La cotinina, su mayor metabolito, es un compuesto más estable que la nicotina, con un tiempo de vida media de aproximadamente 20h (la vida media de la nicotina es de unas 2h) y su concentración no se ve influenciada por otros factores como por ejemplo la dieta. En el hombre, la nicotina y/o cotinina ha sido detectada en plasma seminal de acuerdo al consumo de cigarrillos (Pacifi et al., 1993, 1995; Vine et al., 1993; Zenzes et al., 1999), lo que indica el paso de estos metabolitos a través de la barrera hemato-testicular.
Esto sugiere que ciertos componentes del tabaco interactúan, directa o indirectamente, afectando la función y viabilidad de los gametos; y el mecanismo que envuelve este resultado aún necesita ser elucidado.
El incipiente incremento del interés público respecto al declive del potencial fértil masculino, y sobre todo, el deseo de conocer el efecto que tienen los componentes medioambientales y ocupacionales, y los hábitos de la sociedad actual, hacen necesarios estudios serios, objetivos y completos que revelen la acción que estos ejercen en el espermatozoide, principalmente en población con deseos de gestación.
Con este fin, hemos aprovechado el conocimiento ganado en los tratamientos de reproducción asistida (TRA) después de la introducción de diversos análisis como la prueba de la Dispersión de la Cromatina (SCD) para estudiar el efecto del tabaco sobre la integridad del DNA de los espermatozoides antes y después del swim-up en parejas que consultan por infertilidad.
Este estudio introduce nuevos avances respecto a las consecuencias del tabaco en la reproducción humana.
Fragmentación del DNA y tabaco:
Se estima que un 25% de las causas de infertilidad son de origen idiopático y la etiología de algunas de estas causas podría estar relacionada con daño en el DNA de los espermatozoides.
La fragmentación de DNA en el espermatozoide está siendo cada vez más reconocida como una importante causa de infertilidad, y aunque el origen del daño a nivel del DNA no es claro (Muratori et al., 2000; Sergerie et al., 2005), se han propuesto algunos mecanismos como: defectos en la compactación de la cromatina durante la espermiogénesis, inducción de la apoptosis durante el proceso de espermatogénesis e inducción de daño de DNA en espermatozoides diferenciados
maduros por espermatozoides inmaduros que producen niveles elevados de radicales libres (ROS) (Garrido et al., 2004).
Una causa potencial de la fragmentación de DNA es la exposición a toxinas ambientales; sin embargo, pocos datos apoyan el concepto de un impacto negativo extenso de contaminantes ambientales en los resultados del análisis del semen (Sun et al., 1997). Algunas de estas toxinas se podían relacionar con el consumo de tabaco.
La relación entre el cigarrillo y la fragmentación del DNA del espermatozoide ha sido establecida por algunos autores (Sun et al., 1997; Muratori et al., 2000; Zenzes, 2000). No obstante, Sergerie et al. (2005) han reportado una no asociación en hombres sanos fumadores y no fumadores; y Belcheva et al. encontraron que el daño en el DNA de los espermatozoides de los fumadores estaba incrementado con respecto al de los no fumadores, pero esta diferencia no resultaba estadísticamente significativa.
Uno de los mecanismos sugeridos podría estar relacionado con la interferencia nicotínica sobre la organización de la membrana espermática y por lo tanto en la reacción acrosómica (Arabi, 2004) inducida por ZP3, una proteína de la zona pelúcida que desempeña un papel fundamental durante la fertilización, funcionando como un receptor específico para el espermatozoide (Hinsch et al., 2005).
El propósito en este estudio es investigar la asociación entre el tabaquismo y la fragmentación de DNA del espermatozoide en parejas infértiles sometidas a tratamientos de reproducción asistida, utilizando el SCD antes y después del procedimiento de swim-up como técnica de capacitación espermática en hombres fumadores y no fumadores.
MATERIALES Y MÉTODOS
Población: La población objeto de estudio son pacientes infértiles que asisten a tratamientos de reproducción asistida en nuestro centro, del cual se seleccionaron aleatoriamente las muestras de semen de los maridos de parejas que asisten al laboratorio de andrología del IVI para un tratamiento de infertilidad con previo consentimiento de los pacientes, ya que son pruebas que no se realizan de rutina en el laboratorio. Un total de 99 hombres proporcionaron 99 muestras de semen para ser analizadas. El rango de edad fue de 26 a 49 años, con una media de 36.
Se les realizó el test de SCD, sin conocer, si eran fumadores o no. Posteriormente a los análisis, se procedió a hacer una encuesta a los pacientes acerca de sus hábitos tabáquicos en el momento en el cual fue realizado el ciclo y los 3 meses anteriores. Se estipularon tres grupos según el consumo diario de cigarrillo en los varones: no fumadores (n= 51), fumadores moderados: de 1-19 cigarrillos
por día (n= 21) y varones muy fumadores: más de 19 cigarrillos por día (n= 27); y se analizaron los datos.
Aquellos pacientes que hubieran consumido drogas o alcohol en los 3 meses previos a la realización del estudio, fueron incluidos. También éstos fueron excluidos, si tenían historia reciente de fiebre o exposición a gonadotoxinas como quimioterapia, radioterapia, pesticidas o exposición ocupacional a metales pesados. Además, se investigó acerca de la presencia de varicocele, torsión testicular, etc., para no incluirlos en los mismos.
Fragmentación del DNA espermático.
Prueba de Dispersión de la Cromatina (SCD)
El SCD (Halosperm® kit, INDAS laboratories, España) es una prueba desarrollada recientemente, descrita por Fernández et al., (2003), basada en el hecho de que en los espermatozoides con las cadenas de DNA intactas se produce una descompactación de los bucles de DNA, empaquetados en la matriz nuclear, tras haber sido expuesto a un tratamiento ácido, seguido a un tratamiento con agentes reductores y detergentes. Esta descompactación produce un halo alrededor de la matriz nuclear que se puede visualizar por microscopía de campo claro usando tinciones habituales como el Diff-Quick. Por el contrario, si una de las cadenas de DNA está dañada, no se produce halo, observándose núcleos condensados.
Para el análisis de las muestras se realizó el estudio macro y microscópico del semen según lo descrito anteriormente. Todas las muestras fueron procesadas por swim-up.
Posteriormente, el sobrenadante (0,1- 0,5ml) fue separado en otro tubo. Luego, para la determinación de la fragmentación del DNA se tomaron alícuotas (entre 10 y 100μl) con concentraciones entre 5-10 millones de spz/ml de cada muestra de semen antes y después del swim-up para ser procesadas como describe Fernández et al. (2003).
Se establecieron 5 patrones de SCD: a) Células espermáticas de halo grande (CHG): su anchura es similar o más grande que el diámetro menor del nucleoide; b) Células espermáticas de halo mediano (CHM): su halo está entre aquellos con halo grande y halo muy pequeño. Células espermáticas sanas (CS): este subgrupo incluye las HG y HM, es decir, aquellas sin fragmentación de DNA; c) Células espermáticas de halo muy pequeño (CHP): su espesor es similar o más pequeño que la tercera parte (1/3) del diámetro menor del nucleoide; d) Células espermáticas sin halo (CSH); e) Células espermáticas degradadas (CD): son similares al grupo “d”, pero además están débilmente o irregularmente teñidas. Las células espermáticas de halo pequeño, sin halo y degradadas contienen DNA fragmentado. Finalmente los nucleoides que no corresponden a células espermáticas fueron separados del recuento.
Análisis estadístico: Las comparaciones de la fragmentación del DNA con respecto a los 3 grupos estudiados antes y después del swim-up, se realizaron por la prueba de análisis de varianzas (ANOVA) cuando los datos seguían una distribución normal, mientras que cuando estas seguían una distribución anormal se utilizó la prueba de Kruskal-Wallis (prueba no paramétrica). El análisis estadístico fue llevado a cabo usando el Statistical Package for the Social Sciences (SPSS Inc., Chicago, IL, USA). La significancia estadística se ha definido como P<0,05.
RESULTADOS
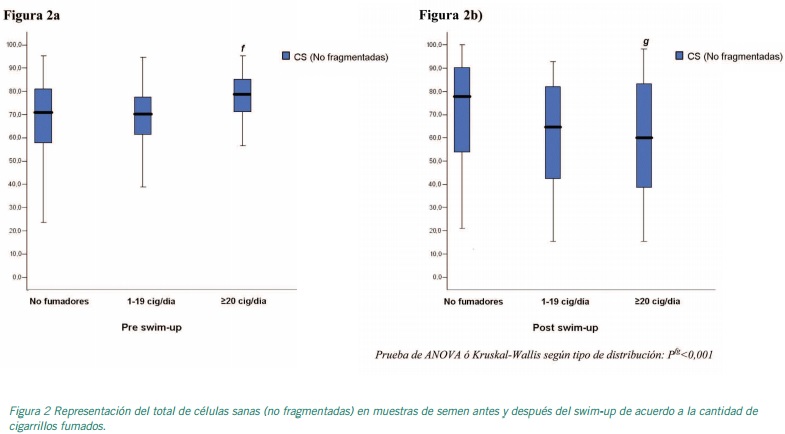
Los resultados de la fragmentación del DNA de espermatozoides en las muestras de los pacientes antes de ser procesadas por swim-up de acuerdo al número de cigarrillos fumados por los varones, no revelaron diferencias significativas entre los 3 grupos estudiados dependiendo de la cantidad de cigarrillos por día. Hombres no fumadores, fumadores moderados y muy fumadores, tuvieron similar patrón de distribución entre las diferentes categorías de acuerdo al tamaño del halo luego de hacer el SCD, es decir, porcentajes de células con CHG, CHM, CS, CHP, CSH y CD (Figura 1a y 2a).
Las Figuras 1b y 2b, muestran los resultados de la fragmentación del DNA de espermatozoides en las muestras luego de ser procesadas por swim-up de acuerdo al número de cigarrillos fumados.
Comparaciones entre esos grupos muestran diferencias significativas en las CHP. Los porcentajes de CHP en los fumadores moderados se incrementaron respecto a aquellos que no fumaban (15,0 IC 95% [6,4-46,0] y 12,2 IC 95% [0,0-32,7]) (Pab=0,020), al igual que en los hombres muy fumadores comparado con el grupo de los no fumadores (19,2 IC 95% [0,9-46,0] y 12,2 IC 95% [0,0-32,7]) (Pac=0,013), demostrándose así un daño en la calidad del DNA entre fumadores en general (moderados y muy fumadores) y no fumadores. Además, los porcentajes de CHG y CS se vieron disminuidos en los dos grupos de hombres fumadores comparados con aquellos que no fumaban, aunque estas diferencias no llegaron a ser significativas.
De igual forma, en los porcentajes de CSH y CD se observó que los daños en el DNA de los espermatozoides de los fumadores moderados estaban incrementados, pero las diferencias no resultaron estadísticamente significativas.
Posteriores comparaciones múltiples entre la fragmentación del DNA de las muestras de semen antes y después del swim-up de acuerdo al número de cigarrillos fumados (comparaciones entre figuras 1a con 1b y 2a con 2b respectivamente), mostraron que en los hombres muy fumadores hubo una disminución significativa (aproximadamente del 50%: 72,8 IC 95% [23,8- 67,3] y 47,3 IC 95% [9,4-97,4]) de las CHG (Pde=0,020), luego del swim-up.
No se encontraron diferencias significativas en las CHM entre los grupos antes y después de la capacitación. También, en los hombres muy fumadores se encontró una disminución muy marcada en las CS (que son el total de las células no fragmentadas) luego del swim-up (Pfg<0,001) (78,7 IC 95% [44,4-95,3] y 60,0 IC 95% [15,4- 98,7]); adicionalmente, se observó un incremento de este tipo de células espermáticas (CS) en el grupo de hombres muy fumadores luego del procesamiento por swim-up, pero este no fue significativo.
Por otra parte, en el mismo gráfico se puede observar, desde otro punto de vista que, las CHP incrementaron significativamente luego del swim-up en los fumadores moderados y muy fumadores (Phb=0,001 y Pic<0.001 respectivamente) en comparación con aquellos hombres sin este hábito, lo que indica una positiva selección de espermatozoides con DNA fragmentado luego de la capacitación en los hombres fumadores. Particularmente en los hombres muy fumadores este incremento fue de más del 100%.
Incluso, en los hombres no fumadores se observó una gran disminución de las CSH y CD (Pjk=0,007 y Plm=0,006 respectivamente), lo cual supone una reducción de espermatozoides con DNA fragmentado luego del swim-up en este grupo, sin embargo esta disminución no fue significativa.
Por tanto, estos hallazgos en las alícuotas post swim-up sugieren que el tabaco altera selectivamente la habilidad del proceso de selección espermática en los hombres fumadores.
DISCUSIÓN
Aunque muchos trabajos sugieren que existen agentes físicos y químicos en el ambiente, muchos de ellos han sido introducidos y propagados por la actividad humana, pudiendo afectar la fertilidad masculina (Oliva et al., 2001), sin embargo, el impacto del consumo de tabaco en la fertilidad masculina resulta un tema controvertido (Vine et al., 1996).
Los resultados de este estudio sostienen que: (i) no hay diferencias en la fragmentación del DNA de los espermatozoides en las muestras de semen en fresco a pesar de los hábitos tabáquicos; y (ii) hay un incremento significativo en la incidencia de células espermáticas con las hebras de DNA rotas en los hombres fumadores luego de evaluar las muestras procesadas por swim-up.
Primero se realizó la prueba de SCD en las muestras de semen en fresco y el resultado de la fragmentación del DNA en los 3 grupos de hombres estudiados, de acuerdo al consumo de cigarrillos por día, fue comparable.
Sergerie et al. (2005), describieron la no asociación entre tabaco y fragmentación de DNA espermático en muestras de semen en fresco de hombres sanos (no infértiles); y Saleh et al. (2002), estudiaron esta asociación en hombres infértiles y reportaron que las diferencias entre fumadores y no fumadores no era estadísticamente significativa.
No obstante, encontraron que las muestras de semen de los hombres infértiles fumadores tenían altos niveles de estrés oxidativo (OS) que en los no fumadores. Esto fortalece los resultados del presente trabajo y refuerza la hipótesis que el efecto ejercido por algunos factores perjudiciales, que afectan los gametos masculinos, podrían estar encubiertos en el eyaculado, siendo los mismos apreciables solo en la selección de espermatozoides por swim-up.
Se debe recalcar que las muestras empleadas en cualquier TRA están previamente procesadas en el laboratorio con la finalidad de eliminar las células no espermáticas y seleccionar los mejores espermatozoides (mejor movilidad y morfología), imitando así los procesos que ocurren en el tracto reproductor femenino en condiciones naturales. Muratori et al., (2000) describieron que hasta cierto punto la fragmentación del DNA estaba positivamente relacionada con una morfología anormal en el espermatozoide y asociada con defectos en la cola; pero encontraron una correlación negativa entre DNA roto y movilidad progresiva.
Basándonos en trabajos previos, donde se encontró que las tasas de fecundación y algunos indicadores de calidad embrionaria estaban relacionados con el alcance de la fragmentación del DNA espermático post swim-up (Muriel et al., 2006); éstos en conjunto con los resultados del actual estudio, se puede concluir que la vía para determinar la fragmentación del DNA parece evidente que debería ser evaluando las alícuotas tras el procesamiento por swim-up.
Con el fin de perfeccionar estos hallazgos, se hicieron comparaciones múltiples entre los 3 grupos estudiados y los resultados antes y después del swim-up; y diferencias significativas indican que los hombres fumadores moderados y muy fumadores presentan un número significativamente mayor de células espermáticas con DNA dañado luego del capacitado que los no fumadores. Es más, los hombres no fumadores tuvieron una disminución significativa de células espermáticas degradadas (CD) y en general menos espermatozoides con DNA deteriorado.
Estudios previos sobre fragmentación del DNA espermático y consumo de tabaco, han sido realizados en semen en fresco (Sergerie et al., 2000; Saleh et al., 2002) o semen capacitado (Sun et al., 1997; Younglai et al., 2001; Belcheva et al., 2004) independientemente, pero no se ha estudiado un diseño como el de este trabajo donde se han comparado las muestras antes y después del capacitado e introduciendo un factor externo.
Respecto al procesamiento en el laboratorio, algunos estudios han analizado la relevancia de la preparación del semen en el porcentaje de células con DNA fragmentado.
La técnica de swim-up para el capacitado de espermatozoides móviles ha sido estudiada por Younglai et al. (2001), en hombres que asisten a una clínica de infertilidad, con el fin de determinar si este procedimiento puede ocasionar efectos perjudiciales en el DNA espermático; y encontraron que no existían diferencias significativas entre la fragmentación del DNA en la muestra fresca y en la procesada por swim-up y por el método de swim-up directo (sin centrifugar); pero en el mismo, no se estudió ningún factor perjudicial externo como por ejemplo el consumo de tabaco.
Al igual que en este estudio, Sun et al. (1997) describieron un incremento en la fragmentación del DNA espermático entre hombres infértiles (fumadores y no fumadores) luego del procesamiento por swim-up que pudiera sugerir un posible vínculo con las toxinas ambientales. Otros estudios llevados a cabo por Belcheva et al. (2004), en donantes por Percoll, concluyeron que la fragmentación del DNA en espermatozoides de donantes sanos (no infértiles) fumadores permanecía dentro del rango normal. Sin embargo, ellos observaron que el fumar cigarrillos inducía un deterioro en la membrana plasmática de las células espermáticas.
En conclusión, el análisis de la fragmentación del DNA en las muestras de eyaculado (en fresco) oculta el efecto perjudicial real del tabaco, ya que no se han encontrado diferencias con respecto al consumo de tabaco, que apuntarían a la conclusión “errónea” que el mismo no influye en la fragmentación del DNA.
Pero es luego del capacitado, donde realmente se puede detectar el efecto perjudicial producido por el tabaco. Este efecto deletéreo está afectando la selección espermática por la interferencia en el proceso del swim-up, demostrando que el tabaco, altera selectivamente la capacitación del semen por swim-up en los hombres fumadores. Las bases celulares y moleculares de este fenómeno quedan aún por elucidar; pero se pueden plantear algunas posibles opciones, como: a) que la fragmentación del DNA (como proceso continuo) se produzca también luego del eyaculado, estando incrementado en los pacientes fumadores y subsecuentemente las células que están algo fragmentadas (halo mediano) terminen fragmentándose completamente tras la incubación durante 1 hora aproximadamente en el proceso de capacitado; b) además esta observación luego del capacitado no significa que este proceso esté aumentando los espermatozoides fragmentados en los fumadores, pero posiblemente si esté seleccionando mejor los espermatozoides no fragmentados en los no fumadores.
La suma de ambos efectos se traduce en esa diferencia significativa luego del swim-up. Basándonos en estas evidencias, es aconsejable que los hombres que son atendidos por infertilidad en TRA o que buscan descendencia eviten el consumo de tabaco.
Referencias
Ballescá JL. “Estudio del varón estéril”. En: Reproducción Humana 2ª ed. McGraw Hill Interamericana. Madrid 2002; 279-286.
Belcheva A, Ivanova-Kicheva M, Tzvetkova P, Marinov M. Effects of cigarette smoking on
sperm plasma membrane integrity and DNA fragmentation. Int J Androl 2004;27(5):296-300.
Benowitz NL, Kuyt F, Jacob P III and Jones RT. Cotinine disposition and effects. Clin. Pharmacol. Ther. 1983. 34, 604-611.
De Jonge C. The clinical value of sperm nuclear DNA assessment. Fertil Steril. 2002;5:51–53.
Dube MF and Green CR. Methods of collection of smoke for analytical purposes. Recent Adv. Tobacco Sci. 1982, 8, 42-102.
Egozcue J. “Esterilidad masculina de causa genética”. En: Reproducción Humana 2ª ed. McGraw-Hill Interamericana. Madrid 2002; 309-312.
Fernandez JL, Muriel L, Rivero MT, Goyanes V, Vazquez R, Alvarez JG. The sperm chromatin dispersion test: a simple method for the determination of sperm DNA fragmentation. J Androl 2003; 24(1):59-66.
Gandini L, Lombardo F, Lenzi A et al. The invitro effects of nicotina and cotinine on sperm motility. Hum. Reprod. 1997, 12, 727-733
Garrido N, Meseguer M, Álvarez JG, Simón C, Pellicer A, Remohí J
Relationship among standard semen parameters, glutathione peroxidase/glutathione reductaseactivity and mRNA expression and reduced gultathione content in ejaculated spermatozoa from fertile and infertile men. Fertil Steril 2004; 82 Suppl 3:1059-66 b.
Hinsch E, Aires VA, Hedrich F, Oehninger S, Hinsch KD. A synthetic decapeptide from a conserved ZP3 protein domain induces the G protein-regulated acrosome reaction in bovine spermatozoa. Theriogenology 2005; 63(6): 1682-94.
Muratori M, Piomboni P, Baldi E, Filimberti E, Pecchioli P, Moretti E et al. Functional and ultrastructural features of DNA-fragmented human sperm. J Androl 2000; 21(6):903-12.
Muriel L, Garrido N, Fernández JL, Remohí J, Pellicer A, De los Santos MJ et al. Value of the sperm DNA fragmentation level, measured by the Sperm Chromatin Dispersion (SCD) test, in the IVF and ICSI outcome. Fertil Steril 2006; 85:371-383.
Oliva A, Spira A, Multigner L. Contribution of environmental factors to the risk of male infertility. Hum Reprod 2001;16(8):1768-76. Pacifi R, Altieri I, Gandini L et al. Nicotine, cotinine and trans-3-cotinine levels in seminal plasma of smokers: effects of sperm parameters. Ther. Drug. Monit. 1993. 15, 358-363.
Pflieger-Bruss S, Schuppe HC, Schill WB The male reproductive system and its susceptibility to endocrine disrupting chemicals. Andrologia 2004; 36(6):337-45.
Pomerol J. “Varicocele e infertilidad”. En: Reproducción Humana 2ª ed. McGraw-Hill Interamericana. Madrid 2002; 303-308.
Rodríguez M, Gil-Salom M, Castillón G and Remohí J. Diagnóstico y conducta a seguir en el varón. En: Manual práctico de esterilidad y reproducción humana. Mc Gaw-Hill Interamericana. 2005; primera parte, cap 6:67
Rosa M, Pacifi R, Altieri I et al. How the steady-state cotinine concentration in cigarette smokers is directly related to nicotine intake. Pharmacol. Epidemiol. Drug Until. 1992. 52, 324-329.
Saleh RA, Agarwal A, Sharma RK, Nelson DR, Thomas AJ Jr. Effect of cigarette smoking on levels of seminal oxidative stress in infertile men: a prospective study. Fertil Steril 2002; 78(3):491-9.
Sergerie M, Bleau G, Teule R, Daudin M, Bujan L. Sperm DNA integrity as diagnosis and prognosis element of male fertility. Gynecol Obstet Fertil 2005; 33(3):89-101.
Sun JG, Jurisicova A, Casper RF. Detection of deoxyribonucleic acid fragmentation in human sperm: correlation with fertilization in vitro. Biol Reprod 1997;56(3):602-7.
Vine MF, Hulka BS, Margolin BH et al. Cotinine concentrations in semen, urine and blood of smokers and nonsmokers. Am. J. Public. Health. 1993. 83, 1335-1338
Vine MF, Tse CK, Hu P, Truong KY. Cigarette smoking and semen quality. Fertil Steril 1996; 65:835–842.
World Health Organization. Tobacco or Health. A Global Status Report. WHO, Geneva, Switzerland. 1997
Younglai EV, Holt D, Brown P, Jurisicova A, Casper RF. Sperm swim-up techniques and DNA fragmentation. Hum Reprod 2001;16(9):1950-3.
Zenzes MT, Bielecki R and Reed TE. Detection of benzo (a) pyrene diol epoxide- DNA adducts in sperm of men exposed to cigarette smoke. Fertil. Steril. 1999. 72, 330-335.
Zenzes MT. Smoking and reproduction: gene damage to human gametes and embryos. Hum Reprod Update. 2000. 6,122–131.