Biopsia Embrionaria “Aspectos Técnicos”
Juan Manuel Moreno
Unidad de Reproducción Hospital Clínica Vistahermosa de Alicante. e- mail:lab@urvistahermosa.com
Resumen: La Biopsia embrionaria es una técnica que se utiliza en los laboratorios de reproducción asistida con el ánimo de mejorar la eficacia de los procesos de fecundación in vitro. Actualmente, entre las razones que hacen difícil apreciar el beneficio verdadero de esta técnica es su heterogeneidad metodológica, por lo que se pretende describir y valorar su utilidad a la luz de los conocimientos existentes.
Palabras clave: Biopsia embrionaria, transferencia embrionaria, ácido Tyrode, DGP.
Embryo Biopsy “Technical Aspects”
Summary: The Embryo Biopsy is a technique that is used in the Assisted Reproduction Laboratories with the spirit to improve the efficacy of the In vitro fertilization cycles. At the moment, between the reasons that make difficult to appreciate the true benefit of this technique is its methodological heterogeneity, reason why it is tried to describe and to value his utility to the light of the existing knowledge.
Key words: Embryo biopsy, embryo transfer, Tyrode´s acid, PGD.
INTRODUCCIÓN
La biopsia embrionaria es una técnica que consiste en extraer una o dos células de un embrión en división para analizarlas genéticamente (diagnóstico genético preimplantacional, DGP) y así poder seleccionar aquellos embriones libres de una determinada alteración genética antes de ser transferidos al útero. El resultado posibilita la identificación de anomalías en estadios previos a la implantación, evitando el desarrollo de anomalías genéticas y previniendo el aborto espontáneo provocado por estas.
La combinación de estos dos procesos, biopsia y posterior estudio genético, surgió en 1990 como alternativa al diagnóstico prenatal en parejas con un elevado riesgo genético (Handyside et al., 1990). Actualmente, es una técnica ampliamente utilizada no sólo en parejas portadoras de enfermedades genéticas hereditarias, anomalías cromosómicas o enfermedades monogénicas (Renwick and Ogilvie, 2007) sino también para aumentar las tasas de implantación en parejas de fecundación in vitro de mal pronóstico (Kuliev and Verlinsky, 2005) tales como pacientes de edad materna avanzada (Rubio et al., 2005), con fallos de implantación (Caglar et al., 2005), abortos previos (Munné et al., 2006) o factor masculino (Donoso et al., 2006). Incluso, se han incorporado otras indicaciones como la detección de determinados tipos de cáncer (Davis et al., 2006), enfermedades degenerativas y tipaje de HLA para transplante de células madre procedentes de sangre de cordón umbilical en niños afectos de patologías hematológicas, genéticas o adquiridas (Verlinsky et al., 2007), aunque algunas de estas indicaciones no están exentas de polémica tanto desde el punto de vista de su utilidad como desde la ética (Coulam et al., 2007; Kuliev and Verlinsky, 2005; Munné et al., 2006; Patricio et al., 2007; Twisk et al., 2006).
VALORACIÓN DE LOS MÉTODOS DE REALIZACIÓN DE BIOPSIA
Según la literatura existente, es aconsejable realizar la microinyección intracitoplasmática (ICSI) para generar los embriones que se vayan a biopsiar, ya que la ausencia de espermatozoides y células de la granulosa adheridas a la zona pelúcida, presentes durante una fecundación in vitro convencional (FIV), evitarían riesgos de contaminación durante el análisis genético posterior (Lissens and Sermon, 1997; Sermon et al., 1998).
Hay estudios que demuestran que la biopsia embrionaria en la etapa de 8 células no es perjudicial para el desarrollo posterior del blastocisto debido a que el índice mitótico es más alto, compensando así con mayor rapidez la célula perdida y además, la ausencia de compactación en los embriones permite que dicho estadio celular sea el idóneo para realizar el proceso (Hardy et al., 1990; Cieslak-Janzen et al., 2006).
Al parecer, si se extrae una célula en el estadio de cuatro células, durante el 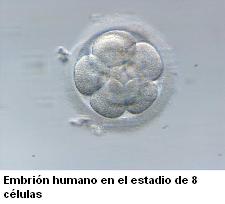 desarrollo del blastocisto se reduce la relación de la masa celular interna con el trofoectodermo (Tarín et al., 1992). No obstante, los embriones en el estadio de 6 u 8 células presentan un cierto grado de compactación debido a la formación de uniones celulares calcio-dependientes. Esto se puede solucionar utilizando un medio que bloquee las uniones entre las células (Dumoulin et al., 1998) y permita realizar la extracción de forma correcta. Sin embargo, para algunos autores esto puede provocar la despolarización de las células interfiriendo en el desarrollo posterior del embrión (Antczak and Van Blerkom, 1999; Edwards and Beard, 1997; Tarín and Handyside, 1993). Otra posibilidad es realizar la biopsia en la etapa de blastocisto, en los días 5 y 6 de desarrollo. Se obtendría un mayor número de células que permitiría una mayor fiabilidad en el diagnóstico aunque se disponga de menos tiempo para realizar el análisis genético. De hecho en un estudio (Evsikov and Verlinsky, 1998) donde se biopsiaron células procedentes de la masa celular interna del blastocisto se observó un porcentaje elevado de blastocistos con mosaicismo. Mas recientemente, Coulam (Coulam et al., 2007) ha demostrado la presencia de un 75% de embriones con una situación de mosaico, discordantes cuando se hace biopsia de dos células y estudio cromosómico de las mismas mediante FISH en día tres; aunque un tercio de estos embriones anómalos se autocorrigen (Munné et al., 2005) no se puede excluir, en estos casos, la posibilidad de una disomía uniparental. Además, hay un estudio experimental para la beta-talasemia (Kokkali et al., 2007) que sugiere que la biopsia del trofoectodermo puede ser más ventajosa que la biopsia del embrión en división con respecto al resultado del diagnóstico al obtener una tasa de implantación del 47,6% frente al 26,7% procedente de la biopsia y análisis efectuado en día 3.
desarrollo del blastocisto se reduce la relación de la masa celular interna con el trofoectodermo (Tarín et al., 1992). No obstante, los embriones en el estadio de 6 u 8 células presentan un cierto grado de compactación debido a la formación de uniones celulares calcio-dependientes. Esto se puede solucionar utilizando un medio que bloquee las uniones entre las células (Dumoulin et al., 1998) y permita realizar la extracción de forma correcta. Sin embargo, para algunos autores esto puede provocar la despolarización de las células interfiriendo en el desarrollo posterior del embrión (Antczak and Van Blerkom, 1999; Edwards and Beard, 1997; Tarín and Handyside, 1993). Otra posibilidad es realizar la biopsia en la etapa de blastocisto, en los días 5 y 6 de desarrollo. Se obtendría un mayor número de células que permitiría una mayor fiabilidad en el diagnóstico aunque se disponga de menos tiempo para realizar el análisis genético. De hecho en un estudio (Evsikov and Verlinsky, 1998) donde se biopsiaron células procedentes de la masa celular interna del blastocisto se observó un porcentaje elevado de blastocistos con mosaicismo. Mas recientemente, Coulam (Coulam et al., 2007) ha demostrado la presencia de un 75% de embriones con una situación de mosaico, discordantes cuando se hace biopsia de dos células y estudio cromosómico de las mismas mediante FISH en día tres; aunque un tercio de estos embriones anómalos se autocorrigen (Munné et al., 2005) no se puede excluir, en estos casos, la posibilidad de una disomía uniparental. Además, hay un estudio experimental para la beta-talasemia (Kokkali et al., 2007) que sugiere que la biopsia del trofoectodermo puede ser más ventajosa que la biopsia del embrión en división con respecto al resultado del diagnóstico al obtener una tasa de implantación del 47,6% frente al 26,7% procedente de la biopsia y análisis efectuado en día 3.
Para poder extraer la célula del embrión es necesario realizar previamente la eclosión asistida que consiste en crear, de manera artificial, un orificio en la zona pelúcida del embrión. En la literatura hay descritos varios métodos (mecánicos, químicos, con láser) y cada laboratorio usa uno u otro dependiendo de la experiencia del embriólogo que lo realiza y la disponibilidad técnica. En cualquier caso, el proceso requiere mucho cuidado en su ejecución para que no se produzca la lisis de alguna de las células del embrión y reste posibilidades de éxito. Además, se ha valorado si la eclosión asistida provocaba algún efecto perjudicial en los embriones y se demostró que la técnica no afecta en la tasa de anomalías cromosómicas en los nacidos vivos (Ma et al., 2006).
Un estudio prospectivo randomizado (Makrakis et al., 2006) que comparaba los métodos mecánicos y el láser dio como resultado una tasa de implantación significativamente más alta en el grupo del láser, además de una tasa de embarazo a término mayor aunque no significativa. Puede que el método mecánico, aunque fácil de ejecutar, no de muy buenos resultados debido a que el pequeño orificio que se crea por la aguja de disección, produzca la posterior estrangulación del blastocisto cuando intenta eclosionar (Cohen et al., 1990). Otro método mecánico, con resultados prometedores es el piezo-micromanipulador que consiste en un sistema de vibración de alta frecuencia que rompe la zona pelúcida. Sin embargo su inconveniente principal es que al igual que el láser es un método costoso (Nakayama et al., 1999).
En otro estudio también prospectivo randomizado (Jones et al., 2006) donde se evaluó el método químico con ácido de Tyrode y el láser en el desarrollo del blastocisto, ambos métodos dieron un resultado similar al no encontrar diferencias significativas en la proporción de blastocistos obtenidos. 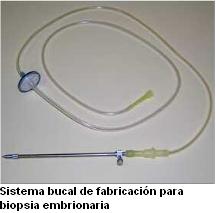 El método químico, aunque requiere entrenamiento previo, tiene la ventaja de estar al alcance de cualquier laboratorio (Moreno and López, 2006a) pero debemos tener cuidado con el ácido pues corremos el riesgo de que un volumen excesivo dañe alguna célula de los embriones. Por otro lado, el láser endurece el área de la zona pelúcida expuesta (Malter et al., 2001), pudiendo dificultar la posterior aspiración de la blastómera. Sin embargo, las ventajas de utilizar el láser frente al ácido de Tyrode son la velocidad y precisión en su ejecución, no es tóxico y puede que se constituya como método de elección al reducir la experiencia técnica necesaria para llevarla a cabo (Joris et al., 2003). En otras palabras, puede estandarizar una técnica que actualmente no está normalizada.
El método químico, aunque requiere entrenamiento previo, tiene la ventaja de estar al alcance de cualquier laboratorio (Moreno and López, 2006a) pero debemos tener cuidado con el ácido pues corremos el riesgo de que un volumen excesivo dañe alguna célula de los embriones. Por otro lado, el láser endurece el área de la zona pelúcida expuesta (Malter et al., 2001), pudiendo dificultar la posterior aspiración de la blastómera. Sin embargo, las ventajas de utilizar el láser frente al ácido de Tyrode son la velocidad y precisión en su ejecución, no es tóxico y puede que se constituya como método de elección al reducir la experiencia técnica necesaria para llevarla a cabo (Joris et al., 2003). En otras palabras, puede estandarizar una técnica que actualmente no está normalizada.
Varios estudios relacionan el tamaño del orificio en la zona pelúcida con el incremento de la frecuencia de gemelos monocigóticos (Hershlag et al., 1999; Schieve et al., 2000) por lo que se aconseja no realizar aberturas muy pequeñas que puedan causar la herniación del blastocisto.
Tampoco son recomendables las aberturas muy grandes ya que se corre el riesgo de la salida de algún blastómero que comprometa la capacidad de desarrollo del embrión. La abertura del orificio debe ser aproximadamente _ partes el diámetro del blastómero a biopsiar.
Una vez realizado el orificio, la célula puede extraerse mediante aspiración del blastómero o desplazamiento del mismo, sea con líquido o ejerciendo presión con la micropipeta contra la zona pelúcida. Nosotros, al igual que la mayoría de los centros, biopsiamos utilizando la aspiración con líquido (Moreno and López, 2006b) pues se controla mejor el proceso sin llegar a dañar la célula extraída ni al embrión biopsiado (Cieslak-Janzen et al., 2006).
Para realizar el proceso de biopsia es necesario usar un medio suplementado con un 10% de HSA para evitar que el embrión y el blastómero extraído se fijen a la placa. Además, debe llevar como solución amortiguadora HEPES que impida cambios de pH durante la realización de la técnica, e incluso carecer de Ca y Mg para bloquear las uniones entre los blastómeros del embrión y así favorecer la extracción. No obstante, es recomendable que el embrión no esté más de 10 minutos en estos medios ya que pueden comprometer el desarrollo in vitro posterior.
La biopsia embrionaria se puede efectuar con ayuda de un microinyector pero 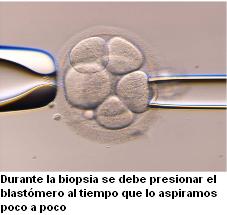 nosotros utilizamos un sistema bucal de fabricación propia que nos permite realizar el proceso de una forma rápida, económica y controlada (Moreno and López, 2006b). Mediante acción controlada con la boca, se aspira en el interior de la micropipeta la cantidad suficiente de medio que evite la presión negativa al aspirar posteriormente el blastómero. A continuación, se acerca la micropipeta a la abertura de la zona pelúcida, se expulsa ligeramente medio para expandir la abertura que bloquearemos con ayuda de la micropipeta. Posteriormente, se aspira el blastómero de forma suave, realizando un movimiento de arriba para abajo, de tal manera que éste pueda adaptarse a la luz de la micropipeta y no se rompa. Para ello, se debe presionar el blastómero al tiempo que lo aspiramos poco a poco.
nosotros utilizamos un sistema bucal de fabricación propia que nos permite realizar el proceso de una forma rápida, económica y controlada (Moreno and López, 2006b). Mediante acción controlada con la boca, se aspira en el interior de la micropipeta la cantidad suficiente de medio que evite la presión negativa al aspirar posteriormente el blastómero. A continuación, se acerca la micropipeta a la abertura de la zona pelúcida, se expulsa ligeramente medio para expandir la abertura que bloquearemos con ayuda de la micropipeta. Posteriormente, se aspira el blastómero de forma suave, realizando un movimiento de arriba para abajo, de tal manera que éste pueda adaptarse a la luz de la micropipeta y no se rompa. Para ello, se debe presionar el blastómero al tiempo que lo aspiramos poco a poco.
A veces, es necesario separar la micropipeta intentando arrastrar el blastómero hacia el exterior del embrión pero en este caso hay que evitar la aspiración porque se corre el riesgo de lisis. Una vez extraído el blastómero, se deja en el medio próximo al embrión.
Por último, se devuelve el embrión biopsiado a la placa de cultivo hasta obtener el diagnóstico.
El número de células a extraer de cada embrión va a depender de la calidad del 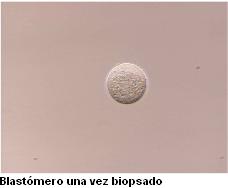 embrión a biopsiar y del análisis genético que se vaya a realizar, no observando diferencias significativas en la tasa de implantación posterior (Van de Velde et al., 2000; Parriego et al., 2003), aunque hay autores que recomiendan extraer dos células para evitar un posible error de diagnóstico (Coulam et al, 2007). Sin embargo, en este estadio se activa el genoma embrionario (Tarín and Handyside, 1993; Fraude et al., 1988; Mottla et al., 1995) y la aspiración de dos células
embrión a biopsiar y del análisis genético que se vaya a realizar, no observando diferencias significativas en la tasa de implantación posterior (Van de Velde et al., 2000; Parriego et al., 2003), aunque hay autores que recomiendan extraer dos células para evitar un posible error de diagnóstico (Coulam et al, 2007). Sin embargo, en este estadio se activa el genoma embrionario (Tarín and Handyside, 1993; Fraude et al., 1988; Mottla et al., 1995) y la aspiración de dos células
afectaría a dicha diferenciación pudiendo dar lugar a blastocistos con una menor proporción en el número de células de la masa celular interna y del trofoectodermo, comprometiendo así su capacidad de implantación.
Los resultados de un ciclo de DGP también van a estar influenciados por el número de embriones que se puedan analizar en cada caso. Por ello, hay grupos que aconsejan cancelar aquellos ciclos en los que se espera obtener menos de 6 ovocitos, ya que las expectativas de transferencia y embarazo se reducen considerablemente pues no todos los ovocitos se fecundan, ni todos los embriones son aptos para realizar el proceso (Vandervorst et al., 1998; Platteau, 2006). Incluso, durante el proceso algún embrión puede dañarse accidentalmente, comprometiendo así su desarrollo.
COMENTARIOS FINALES
La incorporación de la biopsia embrionaria a los Laboratorios de Fecundación in vitro y posterior estudio genético parece mejorar en el resultado general de los programas de reproducción asistida pues favorece un embarazo sano evolutivo con un menor gasto psicológico, fisiológico, e incluso económico. Es una técnica ampliamente utilizada no sólo en parejas con cariotipo alterado (Renwick and Ogilvie, 2007) sino también para aumentar las tasas de implantación en parejas de fecundación in vitro de mal pronóstico (Kuliev and Verlinsky, 2005; Rubio et al., 2005; Caglar et al., 2005; Munné et al., 2006; Donoso et al., 2006). Incluso, se han incorporado otras indicaciones como la detección de determinados tipos de cáncer (Davis et al., 2006), enfermedades degenerativas y tipaje de HLA para transplante de células madre procedentes de sangre de cordón umbilical en niños afectos de patologías hematológicas, genéticas o adquiridas (Verlinsky et al., 2007).
Sin embargo, a la luz de los últimos estudios, el beneficio real del DGP es materia de controversia. En un metaanálisis realizado por Twisk y colaboradores (Twisk et al., 2006) se ha concluido que en los casos de edad maternal avanzada, fallos repetidos de FIV, abortos de repetición y factor masculino su eficacia sigue siendo confusa. De hecho, los datos disponibles para la edad maternal avanzada no demostraron ninguna diferencia en las tasas de embarazo evolutivo y nacido vivo. Por tanto, concluían que hasta que no se demuestre un beneficio significativo debemos evitar su uso rutinario.
CONCLUSIÓN
La biopsia embrionaria y posterior estudio genético son claramente útiles para la selección de embriones con o sin enfermedades monogénicas y en el tipaje de HLA para obtener embriones compatibles con hermanos que tengan algunas enfermedades hematológicas susceptibles de recibir trasplantes.
Sin embargo, en parejas de fecundación in vitro de mal pronóstico debemos ser cautos y hacer una correcta selección de los casos que se van a beneficiar del estudio genético. Además, el avance de la técnica debe ir unido al desarrollo de los aspectos profesionales, éticos, legales y sociales que aseguren una accesibilidad, seguridad y equidad en los procedimientos.
Referencias
Antczak M, Van Blerkom J. Temporal and spatial aspects of fragmentation in early human embryos: possible effects on developmental competence and association with the differential elimination of regulatory proteins from polarized domains. Hum Reprod 1999; 14:429-47.
Braude PR, Bolton V, Moor S. Human gene expression first occurs between four-and eight- cell stages of preimplantation development. Nature 1988; 332:459-62.
Caglar GS, Asimakopoulos B, Nikolettos N, Dietrich K, Al-Hasani S. Preimplantation genetic diagnosis for aneuploidy screening in repeated implantation failure. Reprod Biomed Online 2005; 10:381-88.
Cieslak-Janzen J, Tur-Kaspa I, Ilkevitch Y, Bernal A, Morris R, Verlinsky Y. Multiple micromanipulations for preimplantation genetic diagnosis do not affect embryo development to the blastocyst stage. Fertil Steril 2006; 85:1826-29.
Cohen J, Elsner C, Kort H, Malter H, Massey J, Mayer MP, et al. Impairment of the hatching process following IVF in the human and improvement of implantation by assisted hatching using micromanipulation. Hum Reprod 1990; 5:7-13.
Coulam CB, Jeyendran RS, Fiddler M, Pergament E. D Discordance among blastomeres renders preimplantation genetic diagnosis for aneuploidy ineffective. J Assist Reprod Genet 2007; 24:37-41.
Davis T, Song B, Cram DS. Preimplantation genetic diagnosis of familial adenomatous polyposis. Reprod Biomed Online 2006; 13:707-11.
Donoso P, Platteau P, Papanikolaou EG, Staessen C, Van Steirteghem A, Devroey P. Does PGD for aneuploidy screening change the selection of embryos derived from testicular sperm extraction in obstructive and non-obstructive azoospermic men? Hum Reprod 2006; 21:2390-5.
Dumoulin JCM, Bras M, Coonen E, Dreesen J, Geraedts JPM, Evers JLH. Effect of Ca2+/Mg free medium on the biopsy procedure for preimplantation genetic diagnosis and further development of human embryos. Hum Reprod 1998; 13:2880-3.
Edwards R, Beard H. Oocyte polarity and cell determination in early mammalian embryos. Mol Hum Reprod 1997; 3:863-905.
Evsikov S, Verlinsky Y. Mosaicism in the inner cell mass of human blastocysts. Hum Reprod 1998; 13:3151-5.
Handyside AH, Kontogianni EH, Ardí K, Winston RM. Pregnancies from biopsied human preimplantation embryos sexed by Y-specific DNA amplification. Nature 1990; 344:768-70.
Hardy K, Martin KL, Leese HJ, Winston RM, Handyside AH. Human preimplantation development in vitro is not adversely affected by biopsy at the 8-cell stage. Hum Reprod 1990; 5:708-4.
Hershlag A, Paine T, Cooper GW, Scholl GM, Rawlinson K, Kvapil G. Monozygotic twinning associated with mechanical assisted hatching. Fertil Steril 1999; 71:144-6.
Jones AE, Wright G, Kort HI, Straub RJ, Nagy ZP. Comparison of laser-assisted hatching and acidified Tyrode's hatching by evaluation of blastocyst development rates in sibling embryos: a prospective randomized trial. Fertil Steril 2006; 85:487-91.
Joris H, de Bos A, Janssens R Devroey P, Liebaers I, Van Steirteghem A. Comparison of the results of human embryos biopsy and outcome of PGD alter zona drilling using
acid Tyrode médium or a laser. Hum Reprod 2003; 18:1986-92.
Kokkali G, Traeger-Synodinos J, Vrettou C, Stavrou D, Jones GM, Cram DS, et al. Blastocyst biopsy versus cleavage stage biopsy and blastocyst transfer for preimplantation genetic diagnosis of beta-thalassaemia: a pilot study. Hum Reprod 2007; 22:1443-9.
Kuliev A, Verlinsky Y. Preimplantation diagnosis: a realistic opcion for assisted reproduction and genetic practice. Curr Opin Obstet Gynecol 2005; 17:179-83.
Lissens W, Sermon K. Preimplantation genetic diagnosis: current status and new developments. Hum Reprod 1997; 12:1756-61.
Ma S, Rowe T, Yuen BH. Impact of assisted hatching on the outcome of intracytoplasmic sperm injection: a prospective, randomized clinical trial and pregnancy follow-up. Fertil Steril 2006; 85:895-900.
Makrakis E, Angeli I, Agapitou K, Pappas K, Dafereras A, Pantos K. Laser versus mechanical assisted hatching: a prospective study of clinical outcomes. Fertil Steril 2006; 86:1596- 1600.
Malter H, Schimmel T, Calderón G, Cohen J. Use of Lasers in assisted Reproduction. Annual Review of Preimplantation Embryology 2001:147-156.
Moreno JM, López JJ. Enciclopedia audiovisual de técnicas de reproducción asistida: Eclosión asistida. Animatic 2006, vol 1.
Moreno JM, López JJ. Enciclopedia audiovisual de técnicas de reproducción asistida: Biopsia embrionaria y fijación para FISH. Animatic 2006, vol 2.
Mottla GI, Adelman MR, Hall JI, Gindoff PR, Stillman RJ, Johnson KE. Lineage tracing demonstrates that blastomeres of early cleavage-stage human pre-embryos contribute to both trophectoderm and inner cell mass. Hum Reprod 1995; 10:384-91.
Munné S, Velilla E, Colls P, Garcia Bermudez M, Vemuri MC, Steuerwald N, et al. Self-correction of chromosomally abnormal embryos in culture and implications for stem cell production. Fertil Steril 2005; 84:1328-34.
Munné S, Fischer J, Warner A, Chen S, Zouves C, Cohen J. Preimplantation genetic diagnosis significantly reduces pregnancy loss infertile couples: a multicenter study. Fertil Steril 2006; 85:326-32.
Nakayama T, Fujiwara H,Yamada S, Tastumi K, Honda T, Fujii S. Clinical application of a new assisted hatching method using a piezo-micromanipulator for morphologically lowquality embryos in poor-prognosis infertile patients. Fertil Steril 1999; 71:1014-18.
Parriego M, Solé M, Vidal F, et al. Oneor two-cell biopsy; does it affect implantation potencial in PGD? TWINMeeting Alpha-Andrology; 2003, P- 31.
Patrizio P, Bianchi V, Lalioti MD, Gerasimova T, Sakkas D. High rate of biological loss in assisted reproduction: it is in the seed, not in the soil. Reprod Biomed Online 2007; 14:92- 5.
Platteau P, Staessen C, Michiels A, Van Steirteghem A, Liebaers I, Devroey P. Which patients with recurrent implantation failure after IVF benefit from PGD for aneuploidy screening? Reprod Biomed Online 2006; 12:334-9.
Renwick P, Ogilvie CM. Preimplantation genetic diagnosis for monogenic diseases: overview and emerging issues. Expert rev Mol Diagn 2007;7:33-43.
Rubio C, Rodrigo L, Perez-Cano I, Mercader A, Mateu E, Buendia P, et al.. FISH screening of aneuploidies in preimplantation embryos to improve IVF outcome. Reprod Biomed Online 2005; 11:497-506.
Schieve LA, Meikle SF, Peterson HB, Jeng G, Burnett NM, Wilcox LS. Does assisted hatching pose a risk for monogygotic twinning in pregnancies conceived through in vitro fertilization? Fertil Steril 2000; 74:288-94.
Sermon K, Goossens V, Seneca S, Lissens W, De Vos A, Vandervorst M, et al. Preimplantation diagnosis of Huntington´s disease (HD): clinical application and analysis of the HD expansion in affected embryos. Prenat Diagn 1998; 18:1427-36.
Tarín JJ, Conaghan J, Winston RML, Handyside AH. Human embryo biopsy on the second day after insemination for preimplantation diagnosis: removal of a quarter of the embryo retards cleavage. Fertil Steril 1992; 58:970-6.
Tarín JJ, Handyside AH. Embryos biopsy strategies for preimplantation diagnosis. Fertil Steril 1993; 59:943-52.
Twisk M, Mastenbroek S, van Wely M, Heineman MJ, Van der Veen F, Repping S. Preimplantation genetic screening for abnormal number of chromosomes (aneuploidies) in in vitro fertilisation or intracytoplasmic sperm injection (Review). The Cochrane Library 2006; 1:1-16.
Van de Velde H, De Vos A, Sermon K, Staessen C, De Rycke M, Van Assche E, et al. Embryo implantation after biopsy of one or two cells from cleavage-stage embryos with a view to preimplantation genetic diagnosis. Prenat Diagn 2000; 20:1030-7.
Vandervorst M, Liebaers I, Sermon K, Staessen C, De Vos A, Van de Velde H, et al. Successful preimplantation genetic diagnosis is related to the number of available cumulus-oocyte complexes. Hum Reprod 1998; 13:3169-76.
Verlinsky Y, Rechitsky S, Sharapova T, Laziuk K, Barsky I, Verlinsky O, et al. Preimplantation diagnosis for immunodeficiencies. Reprod Biomed Online 2007; 14:214-23.
