CARACTERÍSTICAS MORFOLÓGICAS Y ULTRAESTRUCTURALES DE CIGOTOS Y EMBRIONES ANORMALES TRAS FIV / ICSI
M.Boada (1), M. Ponsà (2) (1) Servicio de Medicina de la Reproducción. Departamento de Obstetricia y Ginecología. Institut Universitari Dexeus (2) Departamento de Biología Celular, Fisiología e Inmunología. Universitat Autònoma de Barcelona.
monboa@dexeus.com
Resumen: La presencia de dos pronúcleos y dos corpúsculos polares a las 16-22 horas post inseminación in vitro mediante FIV/ICSI, se considera signo inequívoco de una correcta fecundación. Al realizar la valoración de la fecundación otros estados pueden observarse como consecuencia de un fallo de fecundación, una fecundación anómala o un desarrollo incorrecto. En este trabajo se describen las distintas situaciones anómalas que pueden observarse en las primeras fases de desarrollo embrionario: 3PN+2CP, 3PN+1CP, 2PN+1CP, 1PN+1CP, 1PN+2CP y No PN+2CP en D+1, así como los embriones parados en 2PN+2CP, embriones fragmentados y embriones multinucleados en D+2 o D+3. Se detallan las características morfológicas y ultraestructurales de cada caso y se describen los posibles orígenes y su posible viabilidad para la transferencia uterina.
Palabras clave: Ultraestructura / Desarrollo embrionario / Embriones humanos anormales / Polispermia / Fragmentación celular / Multinucleación.
Morphological and ultraestructural characteristics of abnormal zygotes and
cleavage embryos after IVF / ICSI
Summary: The presence of two pronuclei and two polar bodies 16-22 hours after in vitro insemination (IVF/ICSI) is considered as the unequivocal sign of correct fertilization. When fertilization is being evaluated, other stages can be observed as a consequence of a fertilization failure, an anomalous fertilization or an abnormal development. In this paper we describe the different anomalous situations that can be detected at the first stages of embryo development: 3PN+2PB, 3PN+1PB, 2PN+1PB, 1PN+1PB, 1PN+2PB and No PN+2PB at D+1, as well as embryos arrested at stage 2PN+2PB, fragmented embryos and multinucleated embryos at D+2 or D+3. The morphological and ultrastructural characteristics of each case are described, together with their possible origins and viability for uterine transfer.
Key words: Ultrastructure/ Embryo development/ Abnormal human embryos/ Polyspermy/ Cell fragmentation/ Multinucleation
La valoración de los ovocitos inseminados in vitro a las 16-22 horas post inseminación es el procedimiento comúnmente aceptado para evaluar la fecundación. No obstante, en ovocitos inseminados por microinyección espermática (ICSI) la formación de pronúcleos acostumbra a ser más rápida por lo que este periodo suele restringirse a las 16-19 horas post inseminación para evitar una observación excesivamente tardía en la que los pronúcleos ya hayan empezado a desaparecer (ASEBIR, 2008).
Si bien la observación de dos pronúcleos más o menos centrados en el interior del citoplasma y dos corpúsculos polares en el espacio perivitelino (2PN+2CP), al día siguiente de la inseminación (D+1), se considera el estado correspondiente a una correcta fecundación, existen otras situaciones con las que podemos encontrarnos generalmente como consecuencia de procesos erróneos. Una activación partenogenética del ovocito, la polipenetración por parte de más de un espermatozoide o una reactivación anómala de la meiosis que comporte alteraciones en los procesos de formación de los pronúcleos y/o en la extrusión del segundo corpúsculo polar pueden originar situaciones que en la mayoría de los casos se consideran anómalas y en consecuencia, cigotos y/o embriones no transferibles que deben ser descartados (ASEBIR, 2008).
CIGOTOS ANORMALES (D+1) 3PN+2CP
Generalmente el estado de 3PN+2CP se produce en la inseminación mediante FIV convencional y el origen suele ser masculino (diándrico) como consecuencia de la fecundación por parte de dos espermatozoides (dispermia). La polipenetración por más de dos espermatozoides es menos frecuente pero también puede producirse cuando el fallo en el bloqueo contra la polispermia ha sido mayor (>3PN+2CP). Las causas de la polipenetración tanto pueden ser por inmadurez como por hipermadurez de los ovocitos tras inseminaciones con co-incubaciones largas. También se ha relacionado la polipenetración con la presencia de alteraciones de la zona pelúcida ya sean naturales o producidas durante la manipulación, con una incompleta reacción cortical, con la edad de la paciente, con el protocolo de estimulación y con la concentración de espermatozoides utilizada en la inseminación (Austin, 1974; Sathananthan and Trounson, 1982; Trounson et al., 1982; Ducibella 1996).
En la inseminación por ICSI en la que ciertamente se ha introducido un solo espermatozoide, la presencia de más de dos pronúcleos suele ser de origen femenino (digínico) y la observación de 3PN+2CP generalmente corresponde a una no extrusión del 2º corpúsculo polar y fragmentación o división del 1er corpúsculo polar que se ha confundido con la presencia de dos corpúsculos polares. En realidad sería 3PN+1CP.
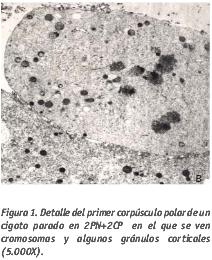
La extrusión del 2º CP suele producirse muy cerca de donde se encuentra el 1er CP que corresponde al polo animal del ovocito (Antzak and Van Blerkom, 1999). El primer corpúsculo polar se diferencia del segundo corpúsculo polar por presentar gránulos corticales (GC), microtúbulos y material nuclear en forma de cromosomas en su interior (Fig. 1). Los orgánulos citoplasmáticos que presenta son los mismos que se encuentran en el citoplasma del ovocito. Frecuentemente se observa dividido o fragmentado. En el segundo corpúsculo polar se observan los mismos orgánulos citoplasmáticos que en el primero pero no suelen observarse GC y el material nuclear se presenta envuelto por membrana nuclear en forma de núcleo o micronúcleos.
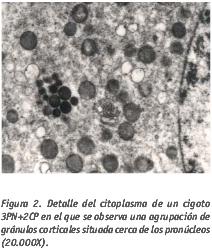
En los ovocitos 3PN fruto de una polispermia, se observan esporádicamente algunos gránulos corticales residuales en la periferia del citoplasma. Si la inseminación de los ovocitos se ha realizado precozmente (ovocitos inmaduros) es frecuente observar los gránulos corticales en regiones más internas del citoplasma formando pequeñas agrupaciones (Fig. 2). En el ovocito maduro los GC se encuentran dispuestos en la periferia debajo de la membrana plasmática. La formación de los GC ocurre en los primeros estadios de la maduración de los ovocitos aunque el momento varía según las especies (Berg and Wessel, 1997). Se originan a partir del complejo de Golgi que se hipertrofia formándose unas vesículas de contenido electrodenso que migran hacia la periferia de la célula gracias a la red de microfilamentos citoplasmáticos (Dimaggio et al., 1997, Wessel et al., 2002). La migración de los GC y la maduración del ovocito son procesos paralelos en la mayoría de las especies. Como consecuencia de la fecundación del ovocito por parte de un espermatozoide, se produce normalmente la reacción cortical para evitar la polispermia. Durante la reacción cortical, la membrana que limita los GC se fusiona con la membrana plasmática (oolema) y el contenido de los gránulos se vierte al espacio perivitelino iniciándose las reacciones químicas que provocan el endurecimiento de la zona pelúcida (ZP) haciéndola menos vulnerable a los enzimas proteolíticos del acrosoma espermático. Los cambios producidos en la matriz extracelular producen una separación tanto física como bioquímica entre la célula y los espermatozoides externos. Actualmente, observaciones de microscopía electrónica y estudios citoquímicos utilizando lectinas parecen indicar que en el oocito humano existen diferentes tipos de GC (Jimenez-Movilla et al., 2004) que podrían desempeñar distintas funciones: modificación de la ZP para evitar la reacción acrosómica, modificación de la membrana del ovocito evitando la fusión con la membrana de otros espermatozoides, e incluso podrían estar relacionados con procesos previos a la fusión de membranas (Liu et al., 2003). Del contenido de los GC se conoce que varía según las especies demostrándose la presencia de determinados carbohidratos reactivos a las Lectinas y tipo N-glycanos
en los GC de la especie humana (Jimenez-Movilla et al., 2004).
La falta o escasez de GC adyacentes a la membrana en los ovocitos polipenetrados, indica que la reacción cortical ya se ha realizado cuando se procede a la fijación de la muestra para su estudio ultraestructural. Generalmente se observan los dos corpúsculos polares en el espacio perivitelino más o menos degenerados y/o fragmentados en función del tiempo transcurrido antes de su fijación. En el citoplasma, se observa una mayor concentración de orgánulos citoplasmáticos alrededor de los pronúcleos. Los orgánulos más abundantes son las mitocondrias que son redondas o ligeramente ovales y con pocas crestas, y las vesículas de retículo endoplasmático liso (REL). 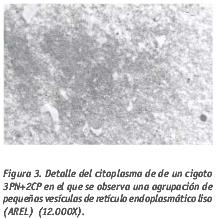 Igual que en los ovocitos y otros cigotos no evolutivos es frecuente observar asociaciones de grandes vesículas de REL con mitocondrias redondas dispuestas a su alrededor. También se observan de forma esporádica, agrupaciones de gran tamaño de pequeñas vesículas de retículo endoplasmático liso (AREL) (Fig. 3) que algunos autores relacionan con ovocitos envejecidos (Sathananthan and Gunasheela, 2007). Al microscopio óptico, las AREL parecen grandes vacuolas aunque difieren de estas por su aspecto translúcido y según se ha visto al microscopio electrónico de transmisión (MET), por carecer de membrana que las delimite. Según su tamaño y posición, pueden llegarse a confundir con un pronúcleo. La existencia de AREL podría ser consecuencia de niveles elevados de estradiol en el día de administración de la hCG y su presencia se ha relacionado con bajas tasas de embarazo (Otsuki et al., 2004). Estos autores sugieren que un patrón anormal en la formación y distribución de REL podría comportar anomalías en el mecanismo de regulación del Ca2+ y por tanto llegar a afectar el desarrollo embrionario. Alteraciones en el mecanismo regulador del calcio que modifiquen las oscilaciones que regulan la expresión del RNAm del ovocito pueden afectar la correcta formación y funcionamiento de los pronúcleos en el cigoto, comprometiendo la activación de la síntesis de RNA nuclear, la primera síntesis de DNA durante la fase S y la posterior unión de los dos genomas en un único genoma embrionario (Tesarik et al., 2007).
Igual que en los ovocitos y otros cigotos no evolutivos es frecuente observar asociaciones de grandes vesículas de REL con mitocondrias redondas dispuestas a su alrededor. También se observan de forma esporádica, agrupaciones de gran tamaño de pequeñas vesículas de retículo endoplasmático liso (AREL) (Fig. 3) que algunos autores relacionan con ovocitos envejecidos (Sathananthan and Gunasheela, 2007). Al microscopio óptico, las AREL parecen grandes vacuolas aunque difieren de estas por su aspecto translúcido y según se ha visto al microscopio electrónico de transmisión (MET), por carecer de membrana que las delimite. Según su tamaño y posición, pueden llegarse a confundir con un pronúcleo. La existencia de AREL podría ser consecuencia de niveles elevados de estradiol en el día de administración de la hCG y su presencia se ha relacionado con bajas tasas de embarazo (Otsuki et al., 2004). Estos autores sugieren que un patrón anormal en la formación y distribución de REL podría comportar anomalías en el mecanismo de regulación del Ca2+ y por tanto llegar a afectar el desarrollo embrionario. Alteraciones en el mecanismo regulador del calcio que modifiquen las oscilaciones que regulan la expresión del RNAm del ovocito pueden afectar la correcta formación y funcionamiento de los pronúcleos en el cigoto, comprometiendo la activación de la síntesis de RNA nuclear, la primera síntesis de DNA durante la fase S y la posterior unión de los dos genomas en un único genoma embrionario (Tesarik et al., 2007).
En el interior de los pronúcleos, se observan pequeños grumos de cromatina y precursores nucleolares densos y compactos, polarizados hacia la zona que convergen los tres pronúcleos (Fig. 4). 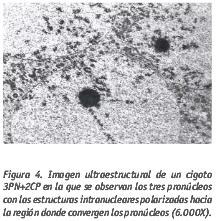 Los paquetes de láminas anilladas citoplasmáticas están presentes también en los cigotos (Fig. 5). Tienen unas características ultraestructurales como las de la envoltura nuclear observándose en sus cisternas numerosos poros complejos. También pueden encontrarse en el interior del núcleo en forma de fragmentos simples, preferentemente convergiendo hacia la zona de confluencia de los pronúcleos. Esta característica se considera como un signo de apoptosis igual que una baja concentración de poros en la membrana nuclear, típico de estados no evolutivos (Rawe et al., 2003).
Los paquetes de láminas anilladas citoplasmáticas están presentes también en los cigotos (Fig. 5). Tienen unas características ultraestructurales como las de la envoltura nuclear observándose en sus cisternas numerosos poros complejos. También pueden encontrarse en el interior del núcleo en forma de fragmentos simples, preferentemente convergiendo hacia la zona de confluencia de los pronúcleos. Esta característica se considera como un signo de apoptosis igual que una baja concentración de poros en la membrana nuclear, típico de estados no evolutivos (Rawe et al., 2003).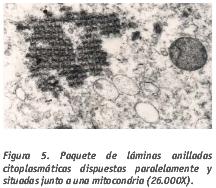 La presencia de pequeños complejos de Golgi indica que ya hay actividad puesto que en los ovocitos maduros parados en metafase II, es raro observar vesículas o cisternas de Golgi. Realizando un estudio secuencial de todo el cigoto y tras una observación minuciosa del citoplasma, se pueden observar restos de los axonemas espermáticos con los nueve pares de microtúbulos, los dos microtúbulos centrales y las nueve fibras densas, mientras que no es posible identificar las mitocondrias procedentes de las piezas intermedias. Generalmente, los restos espermáticos se encuentran muy cerca de los PN (Fig. 6) y raras veces se han descrito
La presencia de pequeños complejos de Golgi indica que ya hay actividad puesto que en los ovocitos maduros parados en metafase II, es raro observar vesículas o cisternas de Golgi. Realizando un estudio secuencial de todo el cigoto y tras una observación minuciosa del citoplasma, se pueden observar restos de los axonemas espermáticos con los nueve pares de microtúbulos, los dos microtúbulos centrales y las nueve fibras densas, mientras que no es posible identificar las mitocondrias procedentes de las piezas intermedias. Generalmente, los restos espermáticos se encuentran muy cerca de los PN (Fig. 6) y raras veces se han descrito 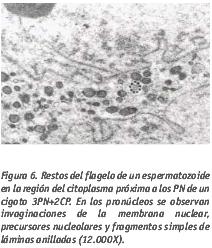 observaciones que permitan asegurar que hay restos de distintos espermatozoides aunque algunas imágenes parecen sugerirlo (Van Blerkom et al., 1984; Boada and Ponsà 1987; Boada 1992; Sathananthan et al., 1999). La presencia de más de un centrosoma espermático, estructura de gran importancia en las primeras divisiones mitóticas por actuar como centro organizador de los microtúbulos y encargado de dirigir la organización de la placa metafásica y del citoesqueleto, puede comportar una segregación tripolar o una segregación totalmente desorganizada con dispersión de los cromosomas. En los 3PN+2CP que pasan a dos células tras una división aparentemente normal, pero cromosómicamente anormal, la explicación más probable es que se haya producido una segregación bipolar quedando uno de los dos centrosomas espermáticos excluido del proceso (Sathananthan et al., 1999).
observaciones que permitan asegurar que hay restos de distintos espermatozoides aunque algunas imágenes parecen sugerirlo (Van Blerkom et al., 1984; Boada and Ponsà 1987; Boada 1992; Sathananthan et al., 1999). La presencia de más de un centrosoma espermático, estructura de gran importancia en las primeras divisiones mitóticas por actuar como centro organizador de los microtúbulos y encargado de dirigir la organización de la placa metafásica y del citoesqueleto, puede comportar una segregación tripolar o una segregación totalmente desorganizada con dispersión de los cromosomas. En los 3PN+2CP que pasan a dos células tras una división aparentemente normal, pero cromosómicamente anormal, la explicación más probable es que se haya producido una segregación bipolar quedando uno de los dos centrosomas espermáticos excluido del proceso (Sathananthan et al., 1999).
La mayoría de los embriones con tres pronúcleos no evolucionan, observándose en su interior, signos estructurales típicos de degeneración como son: fragmentación citoplasmática, aumento de vesículas de REL que evolucionan hacia vacuolas con mitocondrias asociadas y posición excéntrica de los pronúcleos. Su capacidad de división es inferior a la de los cigotos correctamente fecundados pero, si se dividen, los cambios que ocurren no se distinguen de los que se producen en los cigotos 2PN: migración de los PN, interdigitación de las envolturas nucleares y posición convergente de la cromatina, precursores nucleolares y demás estructuras nucleares. Cuando se bloquean y no se dividen, las características morfológicas son equivalentes a las de los cigotos parados en estado de 2PN que no avanzan en el desarrollo embrionario. El timing de división de los cigotos con tres pronúcleos suele verse alterado (Van Blerkom, 1989), observándose normalmente retrasos (Sathananthan et al., 1999). La división de cigotos 3PN genera frecuentemente blastómeros multinucleados. Se ha visto que los cigotos 3PN pueden llegar al estado de blastocisto pudiendo incluso llegar a implantar ya que se conocen tanto fetos como recién nacidos triploides (69XXX o 69XXY) (Edwards, 1986). Los estudios citogenéticos de embriones polipenetrados demuestran que en muchos casos se trata de mosaicos en los que coexisten blastómeros normales y blastómeros con un número anómalo de cromosomas (Munné and Cohen, 1998; Sathananthan et al,1999) Es importante destacar que las observaciones al estereomicroscopio o al microscopio invertido, si no se realizan con suficiente detenimiento, pueden en ocasiones llevar a confusiones. Un cigoto fecundado normalmente (2PN+2CP) que además presente grandes AREL, o una o más vesículas de tamaño similar al de los pronúcleos, puede interpretarse como un cigoto con tres o más PN. En estos casos, una observación más precisa o por un embriólogo más experimentado permitiría distinguir el pseudopronúcleo (PPN) de los verdaderos pronúcleos. Los PPN se distinguen fácilmente de los PN por no presentar precursores nucleolares ni las modificaciones típicas de la membrana en las regiones de convergencia de los pronúcleos (Van Blerkom, 1987). Es importante una observación detallada y responsable ya que a diferencia de los 3PN, el desarrollo de los cigotos con 2PN y un pseudopronúcleo debería ser normal.
3PN+1CP
La explicación de esta situación suele ser la no segregación del 2º corpúsculo polar. Se presenta más frecuentemente en casos de ICSI aunque también puede darse en la FIV convencional. En estos casos correspondería también a una fecundación correcta por parte de un solo espermatozoide y la no extrusión del segundo corpúsculo polar que formaría un segundo pronúcleo de origen femenino (diginia). Las características ultraestructurales de los 3PN+1CP son parecidas a los 3PN+2CP a diferencia de que en estos casos sólo podrían encontrarse restos de un espermatozoide en el interior del ovocito. Igual que los anteriores, estos cigotos pueden dividirse normalmente y llegar a término por lo que deben descartarse desde un principio para su utilización clínica.
2PN+1CP
Puede tratarse de una activación partenogenética sin extrusión del segundo corpúsculo polar y formación de dos pronúcleos femeninos (Kaufan, 1983), o bien ser el producto de una fecundación normal por parte de un espermatozoide pero con la no extrusión del segundo corpúsculo polar por lo que el pronúcleo femenino tendría dotación diploide y el cariotipo fetal correspondería a una triploidía. Los fetos triploides de origen digínico suelen presentar retraso del crecimiento, macrocefalia y placenta no quística (Carceller et al., 2004). Únicamente el estudio cromosómico o molecular del material nuclear permitiría establecer el origen de estos casos que bajo ninguna circunstancia deberían ser transferidos por el riesgo de patologías fetales que pueden comportar. Es importante realizar una observación detallada antes de descartar dichos cigotos con el fin de confirmar la existencia de un solo corpúsculo polar único y bien diferenciado.
En el análisis ultraestructural al MET, la visualización de restos espermáticos en el interior del citoplasma constituiría la prueba irrefutable del origen no partenogenético de estos cigotos.
1PN+1CP
Generalmente se trata de una activación partenogenética sin extrusión del segundo corpúsculo polar y formación de un solo pronúcleo femenino (Kaufman, 1983). Otras explicaciones como la fecundación normal por parte de un espermatozoide pero con ausencia de formación de uno de los dos pronúcleos y no extrusión del segundo corpúsculo polar son menos probables. Igual que en el caso anterior, únicamente la observación de restos espermáticos o el estudio del material nuclear puede esclarecer el origen de dichos cigotos que no deben considerarse para la transferencia uterina a pesar de que generalmente no evolucionan más allá del estado de 6-8 células (Sathananthan and Gunasheela, 2007).
1PN+2CP
La viabilidad de los cigotos 1PN +2CP varía según su origen. Mientras que los procedentes de FIV con inseminación convencional acostumbran a tener una dotación cromosómica diploide y en consecuencia son considerados generalmente como embriones transferibles, los procedentes de ICSI se ha visto que solamente son cromosómicamente normales el 14- 28% de los casos (Staessen and Van Steirteghem, 1997; Balaban et al., 2004) por lo que suelen considerarse como no aptos para uso reproductivo.
Otsu y colaboradores (2004) postulan que cuando el pronúcleo mide 29 μm o más, lo más probable es que sea diploide, mientras que si el tamaño de éste es inferior, el cigoto es cromosómicamente anormal en la mayoría de los casos. Generalmente, los 1PN+2CP de ICSI son producto de una activación partenogenética (Kaufman, 1983; Balakier et al 1993) y raras veces (7%) consiguen llegar a estado de blastocisto (Campos et al., 2007). Su composición genética acostumbra a ser haploide (31- 47%) (Balaban et al., 2004; Sultan et al., 1995) sin embargo en los embriones que derivan de estas estructuras también pueden encontrarse aneuploidías simples o complejas e incluso mosaicos y embriones caóticos (Campos et al., 2007).
En general, la existencia de embriones diploides procedentes de cigotos 1PN+2CP, fenómeno mucho más frecuente en FIV convencional que en ICSI, puede tener distintos orígenes y suele interpretarse como consecuencia de una fecundación normal pero con asincronía en la formación de los dos pronúcleos que dificulta visualizarlos simultáneamente (Sultan et al., 1995; Payne et al., 1997) o como consecuencia de la fusión del pronúcleo masculino y femenino dando lugar a un único pronúcleo diploide de gran tamaño (Levron et al., 1995). La posibilidad de una diploidización temprana de cigotos haploides es la explicación menos probable.
En FIV convencional, la observación de cigotos con solo 1PN+2CP suele considerarse normal y se interpreta como una asincronía en la aparición de los dos pronúcleos. Payne et al (1997) observa sincronización en la formación de los dos pronúcleos en un 63% de los casos. Para la formación del pronúcleo masculino es necesario que se descondense la cromatina espermática, altamente compactada gracias a las protaminas nucleares, mediante la acción de histonas ovocitarias. Una disponibilidad insuficiente de histonas puede comportar un retraso en la transformación del núcleo espermático en pronúcleo masculino y con ello, una asincronía de los pronúcleos.
Para detectar los posibles casos de asincronía, en los cigotos 1PN+2CP se recomienda la realización de una segunda observación para constatar la presencia o ausencia del segundo pronúcleo. Staessen et al (1993) observan que el 25% de estos cigotos forman un segundo pronúcleo asincrónico al cabo de 4-6 horas.
A pesar de que se haya demostrado que un gran número de los cigotos 1PN+2CP son cromosómicamente normales, si las observaciones se han realizado en el timing adecuado y no se observaron los 2PN+2CP, debe tenerse en cuenta que únicamente con microscopía óptica no puede descartarse un posible origen partenogenético por lo que en igualdad de score embrionario, preferentemente se seleccionarán para la transferencia embriones en los que se hayan observado los dos pronúcleos. Tan solo la observación ultraestructural de restos espermáticos en el interior del citoplasma del cigoto o el estudio del material nuclear puede esclarecer definitivamente el origen de dichos casos.
No PN+2CP
La no observación de pronúcleos pero con presencia de dos corpúsculos polares frecuentemente se mal cataloga como “no fecundado” (NF+2CP). Este estado es susceptible de distintas interpretaciones aunque estudios genéticos han demostrado que en un 40% de los casos se trata de cigotos diploides con una tasa de blastocisto de hasta el 56%, lo que parece indicar que podría tratarse de embriones con una velocidad de división distinta (Campos et al., 2007). Para esclarecer la situación, en estos casos se requiere una segunda observación al cabo de unas horas. Pasado este tiempo, si siguen sin observarse estructuras nucleares, se aconseja repetir la observación a las 25-27 horas post inseminación para valorar la división temprana o early cleavage (EC).
En caso de observarse división, la explicación más probable es que la fecundación hubiera sido muy temprana y/o la velocidad de división muy rápida por lo que en el momento de valorar la fecundación, los pronúcleos ya no fueran visibles y el cigoto se estuviera preparando para la primera división embrionaria. Si por el contrario, a las 25-27 horas post inseminación se observan por primera vez los dos pronúcleos correspondería a una fecundación tardía.
Cuando las observaciones se han realizado en el timing adecuado y en ningún momento se han observado los dos PN y dos CP, no se puede excluir un posible origen partenogenético por lo que preferentemente se escogerán para la transferencia uterina, aquellos embriones en los que se hayan observado los dos pronúcleos.
 Si no se observa división ni a las 25-27h post inseminación (EC D+1) ni al día siguiente (D+2), la explicación más probable es la no fecundación del ovocito con división o fragmentación del 1er CP o un paro muy precoz en el correcto desarrollo hacia el estado de cigoto, justo después de la extrusión del 2º CP pero antes de la formación de los PN, lo que se conoce como una fecundación silenciada. En estos casos, el estudio ultraestructural permite observar estructuras espermáticas en el interior del ovocito que confirman la penetración del espermatozoide. Generalmente se observa la cromatina espermática más o menos descompactada y restos de la estructura axonemática del flagelo. También es posible observar fragmentos de membrana nuclear alrededor de los cromosomas del ovocito y/o de la cromatina espermática, dispuestos desordenadamente indicando deficiencias en la formación de la membrana nuclear (Fig. 7).
Si no se observa división ni a las 25-27h post inseminación (EC D+1) ni al día siguiente (D+2), la explicación más probable es la no fecundación del ovocito con división o fragmentación del 1er CP o un paro muy precoz en el correcto desarrollo hacia el estado de cigoto, justo después de la extrusión del 2º CP pero antes de la formación de los PN, lo que se conoce como una fecundación silenciada. En estos casos, el estudio ultraestructural permite observar estructuras espermáticas en el interior del ovocito que confirman la penetración del espermatozoide. Generalmente se observa la cromatina espermática más o menos descompactada y restos de la estructura axonemática del flagelo. También es posible observar fragmentos de membrana nuclear alrededor de los cromosomas del ovocito y/o de la cromatina espermática, dispuestos desordenadamente indicando deficiencias en la formación de la membrana nuclear (Fig. 7).
EMBRIONES ANORMALES EN ESTADOS PRECOCES DE DIVISIÓN (D+2 /D+3)
La valoración de las primeras divisiones embrionarias debe realizarse a las 44- 47 horas post inseminación en D+2 o a las 67-71 horas en D+3. Los criterios para evaluar el desarrollo embrionario incluyen la valoración del número de células o blastómeros, simetría, presencia de núcleos y grado de fragmentación, como parámetros más significativos (ASEBIR, 2008). El número y la semejanza de tamaño de los blastómeros se consideran algunos de los parámetros más importantes, ya que la coexistencia de blastómeros de distinta medida se relaciona con elevadas tasas de aneuploidía y multinucleación (Hardarson et al., 2001).
Existen distintos métodos para la clasificación y selección de los embriones de mejor pronóstico basándose en la observación de dichos parámetros, existiendo unanimidad en considerar embriones de mal pronóstico los que presentan una tasa de fragmentación superior al 25% y/o multinucleación en alguna de sus células.
En D+2, el embrión debería estar en estado de cuatro células o blastómeros similares, fruto de dos divisiones mitóticas. En D+3, una nueva división debería haberse producido en todas sus células dando lugar a un embrión de ocho células. Embriones con un timing de división lento o excesivamente rápido se consideran embriones de mal pronóstico. Estados distintos suelen ser debidos a una mayor o menor velocidad de división de las células así como a una asincronía entre ellas que origina la coexistencia de blastómeros de distinto tamaño, procedentes de distintas divisiones o ciclos celulares.
EMBRIONES PARADOS EN 2PN+2CP EN D+2
La ausencia de división es un fenómeno que se produce ocasionalmente y corresponde a una interrupción del desarrollo en la transición entre la primera interfase y la primera mitosis. En estos casos, la condensación del DNA en cromosomas, la rotura de la membrana nuclear y la formación del huso mitótico bipolar no se producen (Asch et al., 1995). Algunos autores correlacionan este fenómeno con cigotos con pronúcleos separados que no consiguen disponerse en aposición (Tesarik et al., 2007). Estudios de epifluorescencia lo asocian con fenómenos de condensación anómala y fragmentación del DNA no visibles con microscopía óptica (Rawe et al., 2003).
Estudios ultraestructurales de estos cigotos parados muestran un mayor número de paquetes de láminas anilladas citoplasmáticas cerca de los pronúcleos en comparación con los cigotos evolutivos, menor número de poros en la membrana de los pronúcleos, fragmentos de láminas anilladas atrapadas en el interior de los pronúcleos y presencia de numerosas mitocondrias con inclusiones. 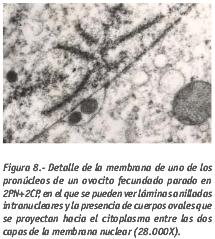 Dichas observaciones sugieren una comunicación núcleocitoplasma comprometida que podría ser la responsable de la interrupción del desarrollo embrionario y de la ausencia de las primeras divisiones mitóticas (Rawe et al., 2003). Entre las dos capas de la membrana nuclear de los embriones parados en fase de pronúcleos se observan frecuentemente pequeños cuerpos ovales, electrodensos y con membrana propia que los delimita. Se encuentran preferentemente en la zona donde convergen los pronúcleos igual que los fragmentos de láminas anilladas y otras estructuras nucleares. Son de 0,15-0,30 μm y parece que se proyectan del núcleo hacia el citoplasma ya que es la lámina externa de la membrana la que se encuentra dilatada hacia el citoplasma (Fig. 8) (Boada,1992). La presencia de estas vesículas o cuerpos ovales intermembrana también se ha observado en cigotos polispérmicos y en embriones tempranos, y su función y contenido sigue estando por determinar
Dichas observaciones sugieren una comunicación núcleocitoplasma comprometida que podría ser la responsable de la interrupción del desarrollo embrionario y de la ausencia de las primeras divisiones mitóticas (Rawe et al., 2003). Entre las dos capas de la membrana nuclear de los embriones parados en fase de pronúcleos se observan frecuentemente pequeños cuerpos ovales, electrodensos y con membrana propia que los delimita. Se encuentran preferentemente en la zona donde convergen los pronúcleos igual que los fragmentos de láminas anilladas y otras estructuras nucleares. Son de 0,15-0,30 μm y parece que se proyectan del núcleo hacia el citoplasma ya que es la lámina externa de la membrana la que se encuentra dilatada hacia el citoplasma (Fig. 8) (Boada,1992). La presencia de estas vesículas o cuerpos ovales intermembrana también se ha observado en cigotos polispérmicos y en embriones tempranos, y su función y contenido sigue estando por determinar
EMBRIONES DIVIDIDOS
El estudio ultraestructural de embriones humanos en D+2/ D+3 nos muestra la presencia de blastómeros de forma oval o redondeada de 75-85 μm de diámetro máximo y 50-60 μm de diámetro mínimo. La membrana citoplasmática es prácticamente lisa. Se observan pocos microvilli en la región de la membrana correspondiente a la parte del blastómero que queda libre mientras que en la región que se encuentra en contacto con los otros blastómeros presenta más microvilli frecuentemente interconectados entre sí, uniones celulares primitivas y pequeñas vesículas o fragmentos citoplasmáticos de distinta electrodensidad. Generalmente, las uniones intercelulares son más abundantes en D+3 que en D+2 y se observan como un engrosamiento de la membrana de mayor electrodensidad. Uniones celulares más complejas, gap y tigh junction, no empiezan a aparecer hasta estadios más avanzados (Lopata et al.,1983). La comunicación intercelular juega un papel importante en la diferenciación celular. Parece comúnmente aceptado que la polarización y diferenciación celular de los embriones se produce bajo control genético, sin embargo, queda mucho por conocer sobre los efectos de los distintos productos génicos que intervienen en dichos procesos (Scott, 2000). Tanoue y Takeichi (2004) describen la existencia de determinadas proteínas responsables de regular la organización del citoesqueleto de la periferia de las células, modulando así los contactos entre blastómeros y la polaridad. Estudios recientes en bovino sugieren que la diferencia de longitud en los puntos de contacto intercelulares podría estar relacionada con el comportamiento de los blastómeros al inicio de la diferenciación celular (Bhojwani et al., 2007).
Los orgánulos suelen distribuirse por todo el citoplasma aunque se observa un ligero incremento alrededor del núcleo y en algunos casos, una menor distribución en la región periférica de los blastómeros más externos en contacto con la zona pelúcida, pero no visible en la región del córtex citoplasmático que se encuentra en aposición con otros blastómeros. Las mitocondrias siguen siendo preferentemente redondas, de matriz muy electrodensa con inclusiones y pocas crestas normalmente aplanadas. Se observan también algunas mitocondrias alargadas y con crestas transversales, típicas de estadios más avanzados con mayor actividad tras la diferenciación celular. Las mitocondrias pueden presentarse libres o formando complejos con vesículas de retículo endoplasmático. El retículo endoplasmático se presenta exclusivamente en forma de retículo liso. Se observan vesículas de distintos tamaños (50-500 nm) distribuidas por todo el citoplasma. Además de los complejos vesícula–mitocondrias, también se observa REL asociado a las uniones intercelulares y a paquetes de láminas anilladas, formando continuidad con éstas. La frecuencia de láminas anilladas es mucho menor en los embriones que en los ovocitos o cigotos. Se observan también algunos complejos de Golgi en forma de pequeñas asociaciones de túbulos que se presentan de forma esporádica y aislada en el citoplasma de estos embriones. Puntualmente se observa la presencia de algún lisosoma secundario en forma de cuerpo multivesiculado. En la periferia del citoplasma se puede encontrar aisladamente algún gránulo cortical y paquetes de microtúbulos (40 o más) dispuestos paralelamente entre sí y con la membrana citoplasmática. La presencia de microtúbulos en la periferia de los blastómeros se relaciona con el importante papel que éstos desempeñan durante la división celular. En el citoplasma de los embriones de pocas células empiezan a observarse también algunos ribosomas aunque la concentración de estos orgánulos en forma libre o de polisomas incrementa a medida que transcurren las primeras divisiones embrionarias siendo muy abundantes en embriones de 14-16 células (Lopata et al., 1983). La presencia de ribosomas al tercer día de desarrollo coincide con la activación del genoma. En la especie humana, la activación del genoma embrionario empieza en el estadio de cuatro células con la activación de la síntesis de RNA nuclear y justo a continuación, entre cuatro y ocho células, empiezan a aparecer los primeros signos bioquímicos y morfológicos de la expresión génica embrionaria (Tesarik et al., 2007). Si bien durante los primeros tres días el embrión sobrevive mayoritariamente gracias a las reservas ovocitarias y según estudios recientes, también a los RNAm que aporta el espermatozoide (Ostermeier et al., 2004; Ambartsumyan y Clark, 2008), a partir de este momento debe iniciarse la actividad transcripcional del DNA del propio embrión.
El núcleo de los blastómeros es poco electrodenso, tiene forma esférica (20- 25μm) y suele estar en el centro de la célula. La membrana nuclear es doble con numerosos poros y dilataciones de la membrana externa en las que se encuentran pequeños cuerpos ovales (Dvorak et al.,1982; Sathananthan, 1984; Boada, 1992). En el interior del núcleo se encuentran distintos precursores nucleolares de aproximadamente 2μm de diámetro próximos a la membrana nuclear. En embriones de 2-4 células, tienen forma esférica y son extremadamente densos y compactos similares a los que se observan en los pronúcleos de los cigotos. En estadios posteriores (8-16 células), los nucleolos ya presentan un aspecto granular y reticulado, menos compacto y con menor electrodensidad indicativo de actividad nucleolar tras la activación de la expresión del genoma embrionario (Lopata et al., 1983; Sathananthan, 1993). En el interior del núcleo se observan también pequeños agregados de heterocromatina de forma dispersa y, en ocasiones, algún fragmento simple de láminas anilladas intranucleares.
EMBRIONES FRAGMENTADOS
La presencia abundante de fragmentos citoplasmáticos puede llegar a comprometer la viabilidad y potencial implantatorio del embrión. Dependiendo del tamaño y distribución de los fragmentos, la existencia de fragmentación puede tener distinto pronóstico (Alikani and Cohen, 1995; Alikani et al., 2000). Se ha sugerido que algunos patrones de fragmentación conllevarían la pérdida total o parcial de algunas proteínas reguladoras específicas de los blastómeros, lo que podría comportar consecuencias negativas para el desarrollo embrionario tanto de los blastómeros fragmentados como del embrión en su totalidad (Antzak and Van Blerkom, 1999).
Algunos autores relacionan la fragmentación con fenómenos apoptóticos (Jurisicova et al., 1996) aunque la existencia de dicha relación sigue siendo controvertida. Estudios realizados con Anexina V, proteína calcio-dependiente con gran afinidad por los fosfolípidos internos de la membrana citoplasmática, parecen indicar que no existe correlación (Antzak and Van Blerkom, 1999). Según un estudio de Spanos y colaboradores (2002) en el que evalúan la capacidad fagocitaria de los blastómeros, los fenómenos apoptóticos se encuentran inhibidos durante las primeras fases de desarrollo embrionario y no se inician hasta después de la fase de compactación. Sin embargo, estudios más recientes demuestran que la fragmentación podría estar regulada por ciertos componentes del programa genético de la apoptosis como el gen Caspase-3, inductor de la muerte celular (Jurisicova et al., 2003).
Algunos autores atribuyen la reducida viabilidad de los embriones fragmentados a la presencia de fragmentos per se, sin embargo, los beneficios de efectuar una extracción de los fragmentos previamente a la transferencia embrionaria parecen limitados. Según Alikani (2007), únicamente se observa un aumento de la tasa de implantación tras la aplicación de esta técnica en los embriones con 15-35% de fragmentos. En los embriones con <15% o >35% de fragmentos la influencia es menor en la mayoría de los casos ya sea por que la fragmentación es muy leve y apenas comporta consecuencias negativas para el embrión o bien por que el daño es excesivo y probablemente irreversible.
Trabajos con video-filmaciones han demostrado que en algunos embriones la fragmentación puede considerarse como un episodio temporal que puede reducirse o incluso desaparecer al cabo de algunas divisiones celulares. También se ha constatado que los embriones mitóticamente inactivos no se fragmentan por lo que el proceso de fragmentación se relaciona únicamente con las células en división (Alikani, 2007).
Los fragmentos son de origen citoplasmático y están delimitados por membrana citoplasmática lisa en la que prácticamente no se observan microvilli. Tampoco se observan uniones que los conecten entre sí ni con los blastómeros. Según su tamaño pueden llegarse a confundir con un blastómero o con los corpúsculos polares aunque se distinguen de ellos por ser anucleados y por presentar formas variadas. 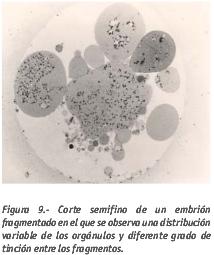 Por lo general, los fragmentos no presentan ningún tipo de material nuclear en su interior y el citoplasma contiene los mismos orgánulos citoplasmáticos que el de los blastómeros aunque la distribución suele ser distinta. Los orgánulos se concentran en determinadas zonas de los fragmentos dejando regiones sin orgánulos que se observan como regiones más claras que en ocasiones pueden tener forma de anillo y abarcar toda la región periférica del fragmento, similar al anillo acitoplasmático que se observa en los blastómeros en procesos degenerativos (Veeck, 1999), o incluso ocupar prácticamente todo el fragmento (fragmentos de aspecto vacío). La electrodensidad de los fragmentos suele ser variable pudiéndose encontrar en un mismo embrión, fragmentos más oscuros que otros, que en cortes semifinos se observan con diferente grado de tinción (Fig. 9).
Por lo general, los fragmentos no presentan ningún tipo de material nuclear en su interior y el citoplasma contiene los mismos orgánulos citoplasmáticos que el de los blastómeros aunque la distribución suele ser distinta. Los orgánulos se concentran en determinadas zonas de los fragmentos dejando regiones sin orgánulos que se observan como regiones más claras que en ocasiones pueden tener forma de anillo y abarcar toda la región periférica del fragmento, similar al anillo acitoplasmático que se observa en los blastómeros en procesos degenerativos (Veeck, 1999), o incluso ocupar prácticamente todo el fragmento (fragmentos de aspecto vacío). La electrodensidad de los fragmentos suele ser variable pudiéndose encontrar en un mismo embrión, fragmentos más oscuros que otros, que en cortes semifinos se observan con diferente grado de tinción (Fig. 9).
EMBRIONES MULTINUCLEADOS
A pesar de que algunos autores habían sugerido que la multinucleación podría ser un fenómeno temporal y reversible de la división celular (Staessen and Van Steirteghem, 1998), la presencia de multinucleación se correlaciona directamente con un incremento en la tasa de aneuploidías y mosaicismo (Sathananthan et al., 1999; Hardarson et al., 2001) por lo que los embriones que la presentan se consideran de mal pronóstico y existe consenso en considerarlos como no transferibles, por lo que deberían excluirse para la transferencia uterina a menos que no exista ningún otro embrión de mejor pronóstico (Gil et al., 2007)
En muchas ocasiones la multinucleación se presenta asociada a otros fenómenos anómalos como la polispermia (Van Blerkom et al., 1984) fruto de una segregación anómala (Kola and Trounson, 1989, Sathananthan et al., 1999), el cese del desarrollo embrionario o la fragmentación citoplasmática (Van Royen et al., 2003). También puede detectarse en embriones sin ningún otro signo de anormalidad morfológica (Fig. 10).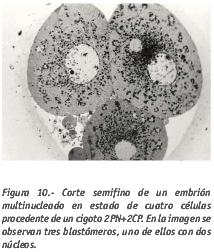
Distintos estudios han reportado una incidencia variable de blastómeros multinucleados de hasta el 74% en embriones de D+2/D+3 procedentes de cigotos 2PN+2CP (Gil et al., 2007).
Mayoritariamente, la multinucleación se considera fruto de la ausencia de división citoplasmática (citocinesis) tras una replicación mitótica del material nuclear, división nuclear (cariocinesis) o fragmentación del núcleo (Lopata et al., 1983, Hardy et al.,1993). Según Tesarik et al., (1987), este fenómeno se produce por una migración deficiente de los cromosomas durante la anafase mitótica, que comportaría la aparición de grupos aislados de cromosomas que posteriormente quedarían individualmente envueltos por membrana nuclear formando distintos núcleos o micronúcleos. La presencia de blastómeros multinucleados puede tener distintos orígenes, siendo los más probables los defectos en el citoesqueleto o en la placa metafásica del ovocito o blastómero y las anomalías en el centrosoma espermático. Se han relacionado con el fenómeno de la multinucleación: las condiciones no adecuadas de cultivo embrionario como por ejemplo cambios en la temperatura (Winston et al., 1991), determinados medios de cultivo (Pickering et al., 1995) o incluso los fármacos empleados en la estimulación del ciclo ovulatorio (De Vincentiis et al., 2005).
Existen distintos patrones de multinucleación que tienen en cuenta el número de células afectadas, el número de núcleos que se observan y el día de desarrollo en el que se detecta la anomalía. Según el patrón de multinucleación, el pronóstico del embrión será distinto. Meriano et al (2004) distingue dos fenotipos embrionarios distintos según presenten blastómeros binucleados o multinucleados, y encuentra mayor tasa de embarazo transfiriendo embriones con blastómeros binucleados (48%) en comparación con los multinucleados (15.4%).
La observación de la división temprana (EC) en la tarde del D+1 permite detectar los primeros blastómeros multinucleados. Kligman y colaboradores (1996) describen que el 70% de las células con multinucleación en D+2/D+3 presentan tres o más núcleos, mientras que en estadios más avanzados (D+4) suelen ser binucleadas. Dichos autores postulan que la multinucleación en D+2/D+3 produce mayoritariamente embriones cromosómicamente anormales mientras que si se observa en D+4 o estadios posteriores, la mayoría de los embriones serán cromosómicamente normales.
También se han descrito embriones multinucleados en los primeros estadios de desarrollo embrionario que posteriormente son mononucleados (Gil et al., 2007) y distintos autores han reportado el nacimiento de niños sanos a partir de la transferencia de embriones multinucleados (Balakier and Cadesky, 1997; Jackson et al., 1998; Pelinck et al., 1998). La explicación a este fenómeno de reparación o corrección de la multinucleación también es muy variada e incluye distintas hipótesis como la recuperación en divisiones posteriores de la citocinesis, la fusión posterior de los núcleos derivados inicialmente de un mismo núcleo (Kligman et al., 1996) y la relegación al trofectodermo de las células cromosómicamente anormales (Mottla et al., 1995).
El volumen de los blastómeros multinucleados es significativamente mayor que el de sus blastómeros hermanos. Los análisis morfométricos demuestran que los blastómeros mononucleados de embriones multinucleados son menores que los mononucleados de embriones normales (Hnida and Ziebe, 2007).
Los núcleos de las células multinucleadas suelen ser de menor tamaño que los de las células mononucleadas (Lopata et al., 1983), aunque frecuentemente se observan núcleos de distinto tamaño en un mismo blastómero. 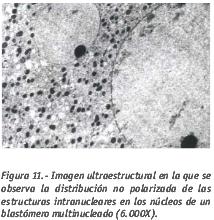 Los núcleos suelen ser redondos aunque a veces pueden ser ovales e incluso lobulados. La membrana nuclear presenta múltiples poros y la presencia de pequeños cuerpos ovales entre las dos capas de la membrana, que en ocasiones son de mayor tamaño y menor
Los núcleos suelen ser redondos aunque a veces pueden ser ovales e incluso lobulados. La membrana nuclear presenta múltiples poros y la presencia de pequeños cuerpos ovales entre las dos capas de la membrana, que en ocasiones son de mayor tamaño y menor
electrodensidad que los observados en los pronúcleos. Una característica particular de los blastómeros multinucleados es la ausencia de polarización de las estructuras nucleares. A diferencia de la polarización observada en las estructuras nucleares de los pronúcleos de los cigotos hacia la zona de convergencia de estos, las estructuras nucleares de los distintos núcleos de un mismo blastómero no presentan esta tendencia a polarizarse de forma convergente (Fig. 11) (Boada, 1992).
Referencias
Alikani M, Cohen J. Patterns of cell fragmentation in the human embryo. J Assist Reprod Genet 1995;12:28S.
Alikani M, Calderón G, Tomkin G, Garrisi J, Kokot M, Cohen J. Cleavage anomalies in early human embryos and survival after prolonged culture in-vitro. Hum Reprod 2000;15:2634-2643.
Alikani M. The origins and consequences of fragmentation in mammalian eggs and embryos. En: Elder K, Cohen J, editors. Human preimplantation embryo selection. London: Informa Healthcare; 2007. p. 51-77.
Ambartsumyan G, Clark AT. Aneuploidy and early human embryo development. Hum Mol Genet 2008;17(R1):R10-5.
Antezak M, Van Blerkom J. Temporal and spatial aspects of fragmentation in early human embryos: possible effect on developmental competence and association with the differential elimination of regulatory proteins from polarised domains Hum Reprod 1999;14:429-447.
Asch R, Simerly CS, Ord T, Ord VA, Schatten G. The stages at which human fertilization arrests: microtubule and chromosome configurations in inseminated oocytes which fail to complete fertilization and development in humans. Hum Reprod 1995;10:1897-1906.
ASEBIR. Cuadernos de embriología clínica. II Criterios ASEBIR de valoración morfológica de oocitos, embriones tempranos y blastocistos humanos. 2ª edición. 2008.
Austin, CR. Fertilization. En: Lash J, Whittaker JR editors. Concepts of Development. Stanford: Sinauer Associates; 1974. p. 48–75
Balaban B, Yakikn K, Urman B, Isiklar A, Tesarik J. Pronuclear morphology predicts embryo development and chromosome constitution. Reprod BioMed Online 2004;8:695-700.
Balakier H, Squire J, Casper RF. Characterization of abnormal pronuclear human oocytes by morphology, cytogenetics and in-situ hybridization. Hum Reprod 1993;8:402-408.
Balakier H, Cadesky K. The frequency and developmental capability of human embryos containing multinucleated blastomeres. Hum Reprod 1997;12:800-804.
Berg LK, Wessel GM. Cortical granules of the sea urchin translocate early in oocyte maturation. Development 1997;124:1845- 1850.
Bhojwani S, Tomek W, Jonas L, Becker F, Alm H, Torner H, et al. Ultraestructural analysis reveals differences of intracellular contact lengths in bovine embryos produced in vivo, in vitro and by somatic cell nuclear transfer. Mol Reprod Dev 2007;74:775-784.
Boada M. Ultraestructura d’oòcits humans inseminats in vitro. Tesis Doctoral. Universidad Autónoma de Barcelona. 1992.
Boada M, Ponsà M. Ultrastructural studies of human zygotes. En: Egozcue J, Barberá- Guillem E, editors. Cellular aspects of in vitro fertilization. Cell Biology Reviews. Leioa-Vizcaya: Springer International; 1987. p. 32-38.
Campos G, Parriego M, Vidal F, Coroleu V, Veiga A. Análisis cromosómico y potencial de desarrollo de cigotos monopronucleares y apronucleares. Rev Iberoam Fertilidad 2007;24:29-34.
Carceller R, Saenz I, Gracia E, Bassecourt M, Ureña T, Garcia-Dihinx J, et al. Triploidia completa 69 XXY. Carta al director. An Pediatr (Barc) 2004;61:562-564.
De Vincentiis S, Nodar F, Lavolpe M, Fiszbajn G, Rawe V, Brugo Olmedo S. Embryo multinucleation (MNC) and clinical outcome: Its relationship with the use of agonists and antagonists of GnRH in ART and the cellular events associated with this nuclear alteration. Fertil Steril 2005;84(supl 1), P373:S284.
Dimaggio AJ, Lonergan TA, Stewart-Savage J. Cortical granule exocytosis in hamster eggs requires microfilaments. Mol Reprod Dev 1997;47:334-340.
Ducibella T.The cortical reaction and development of activation competence in mammalian oocytes. Hum Reprod Update 1996;1:29–42.
Dvorak M, Tesarik J, Ladislav P, Travnik P. Fine structure of human two cell ova fertilized and cleaved in vitro. Fertil Steril 1982;37:661-667.
Edwards RG. Causes of early embryonic loss in human pregnancy. Hum Reprod 1986;1:185-198.
Gil M, D’Ommar G, Póo M, Sosa A, Piras M, Piras R, et al. Insights on blastomere nuclearity. J Assist Reprod Genet 2007; 24:17-22.
Hardarson T, Hanson C, Sjögren A, Lundin K. Human embryos with unevenly sized blastomeres have lower pregnancy and implantation rates: indications for aneuploidy and multinucleation. Hum Reprod 2001;16:313-318.
Hardy K, Winston R, Handyside A. Binucleated blastomeres in preimplantation human embryos in vitro: Failure of cytokinesis during early cleavage. J Reprod Fertil 1993;98:549-558.
Hnida C, Ziebe S. Morphometric análisis of human embryos En: Elder K, Cohen J, editors. Human preimplantation embryo selection. London: Informa Healthcare; 2007. p. 89-99.
Jackson KV, Ginsburg ES, Hornstein MD, Rein MS, Clarke RN. Multinucleation in normally fertilized embryos is associated with an accelerated ovulation induction response and lower implantation and pregnancy rates in in vitro fertilizationembryo transfer cycles. Fertil Steril 1998;70:60-66.
Jiménez-Movilla M, Avilés M, Gómez-Torres MJ, Fernández-Colom PJ, Castells MT, de Juan J, et al. Carbohydrate analysis of the zona pellucida and cortical granules of human oocytes by means of ultrastructural cytochemistry. Hum Reprod 2004;19:1842-1855.
Juriscova A, Varmuza S, Casper RF. Programmed cell death and human embryo fragmentation. Mol Hum Reprod 1996;2:93-98.
Jurisicova A, Antenos M, Varmuza S, Tilly JL, Casper RF. Expression of apoptosisrelated genes during human preimplantation embryo development: potential roles for the Harakiri gene product and Caspase-3 in blastomere fragmentation. Mol Hum Reprod 2003;9:133-141.
Kaufman MH. Mammalian parthenogenesis: background to experimental studies, terminology and pathways of development. En: Kaufman MH, editors. Early mammalian development. Parthenogenetic studies. Cambridge: Cambridge University Press; 1983. p. 1-259.
Kligman I, Benadiva C, Alikani M, Munné S. The presence of multinucleated blastomeres in human embryos is correlated with chromosomal abnormalities. Hum Reprod 1996;11:1492-1498.
Kola I, Trounson A. Dispermic human fertilization: Violation of expected cell behaviour. En: Schattently Schatten G, editor. The cell biology of fertilization. San Diego: Academic Press. Inc; 1989. p. 277-293.
Levron J, Munné S, Willadsen S, Rosenwaks Z, Cohen J. Male and female genomes associated in a single pronúcleos in human zygotes. Biol Reprod 1995;52:653-657.
Liu M, Sims D, Calarco P, Talbot P. Biochemical heterogeneity, migration, and prefertilization release of mouse oocyte cortical granules Reprod Biol Endocrinol 2003;1:77.
Lopata A, Kohlman D, Johnston J. The fine structure of normal and abnormal human embryos developed in culture. En: Beier H, Lindener H, editors. Fertilization of human eggs in vitro. Heidelberg: Springer Verlag; 1983. p.189-210.
Merino J, Clark C, Cadesky K, Laskin CA. Binucleated and micronucleated blastomeres in embryos derived from human assisted reproduction cycles. Reprod Biomed Online 2004;9:511-520.
Mottla GL, Adelman MR, Hall JL, Gindorff PR, Stillman RJ, Johnson KE. Lineage tracing demonstrates that blastomeres of early cleavage-stage human pre-embryos contribute to both trophectoderm and inner cell mass. Hum Reprod 1995;10:384-391.
Munné S, Cohen J. Chromosome abnormalities in human embryos. Hum Reprod Update 1998;4:842-855.
Ostermeier GC, Millar D, Huntriss JD, Diamond MP, Krawetz SA. Reproductive biology:delivering spermatozoan RNA to the oocyte. Nature 2004;6988:154.
Otsu E, Sato A, Nagaki M, Araki Y, Utsunomiya T. Developmental potential and chromosomal constitution of embryos derived from larger single pronuclei in human zygotes used in in vitro fertilization. Fertil Steril 2004;81:723-724.
Otsuki J, Okada A, Morimoto K, Nagai Y, Kubo H. The relationship between pregnancy outcome and smooth endoplasmic reticulum clusters in MII human oocytes. Hum Reprod 2004;19:1591-1597.
Payne D, Flaherty SP, Barry MF, Matthews CD. Preliminary observations on polar body extrusion and pronuclear formation in human oocytes using time-lapse cinematography. Hum Reprod 1997;12:532-541.
Pelinck MJ, De Vos M, Dekens M, Van Der Elst J, De Sutter P, Dhont M. Embryos cultured in vitro with multinucleated blastomeres have poor implantation potencial in human in-vitro fertilization and intracytoplasmic sperm injection. Hum Reprod 1998;13:960-963.
Pikering S, Taylor A, Johnson M, Braude P. An analysis of multinucleated blastomere formation in human embryos. Hum Reprod 1995;10:1912-1922.
Rawe VY, Brugo Olmedo S, Nodar FN, Ponzio R, Sutovsly P. Abnormal assembly of annulate lamellae and nuclear pore complexes coincides with fertilization arrest at the pronuclear stage of human zygotic development. Hum Reprod 2003;18:576-582.
Sathananthan AH, Trounson AO. Ultrastructure of cortical granule release and zona reaction in monospermic and polyspermic human ova fertilized in vitro. Gamete Res 1982;6:225-334.
Sathananthan AH. Ultrastructural morphology of fertilization and early cleavage in the human. En: Trounson A, Wood C, editors. In vitro fertilization and embryo transfer. Edinburgh. Churchill Livingstone; 1984. p. 131-158.
Sathananthan AH. Ultrastructure in fertilization and embryo development. En:Trounson A, Gardner D, editors. Handbook of In vitro fertilization. Florida: CRC Press; 1993. p. 237-261.
Sathananthan AH, Tarin JJ, Gianaroli L, Ng CS, Dharmawardena V, Magli MC, et al. Development of the human dispermic embryo. Hum Reprod Update 1999;5:553-560.
Sathananthan AH, Gunasheela G. Human oocytes and embryo assessment for ART. En: Elder K, Cohen J, editors. Human preimplantation embryo selection. London: Informa Healthcare; 2007. p. 1-14.
Scott L. Oocyte and embryo polarity. Semin Reproductive Med 2000;14:171-183.
Spanos S, Rice S, Karagiannis P, Taylor D, Becker DL, Winston RM, Hardy K. Caspase activity and expression of cell death genes during development of human preimplantation embryos. Reproduction 2002;124:353-363.
Staessen C, Janssenwillen C, Devroey P, Van Steirteghem A. Cytogenetic and morphological observations of single pronucleated human oocytes after in-vitro fertilization. Hum Reprod 1993;8:221-223.
Staessen C, Van Steirteghem A. The chromosomal constitution of embryos developing from abnormally fertilized oocytes after intracytoplasmatic sperm injection and conventional in-vitro fertilization. Hum Reprod 1997;12:321-327.
Staessen C, Van Steirteghem A. The genetic constitution of multinuclear blastomeres and their derivative daughter blastomeres. Hum Reprod 1998;13:1625-1631.
Sultan KM, Munné S, Palermo GD, Alikani M, Cohen J. Ploidy assessment of embryos derived from single-pronucleated human zygotes obtained by regular IVF and intracytoplasmic sperm injection (ICSI). Hum Reprod 1995;10:132-136.
Tanoue T, Takeichi M. Mammalian Fat1 cadherin regulates actin dynamics and cellcell contact. J Cell Biol 2004;165:517-528.
Tesarik J, Kopecny V, Plachot M, Mandelbaum J. Ultrastructural and autoradiographic observations on multinucleated blastomeres of human cleaving embryos obtained by in vitro fertilization. Hum Reprod 1987;2:127-136.
Tesarik J, Mendoza-Tesarik R, Greco E, Mendoza C. Morphology and kinetics of human pronuclei. En: Elder K, Cohen J, editors. Human preimplantation embryo selection. London: Informa Healthcare; 2007. p. 21-29.
Trounson A, Mohr LR, Wood C, Leeton JF. Effect of delayed insemination on in vitro fertilization, culture and transfer of human embryos. J Reprod Fertil 1982;64:285-294.
Van Blerkom J, Henry G, Porreco R. Preimplantation human embryonic development from polypronuclear eggs after in vitro fertilization. Fertil Steril 1984;41:686-696.
Van Blerkom J, Bell H, Henry G. The ocurrance, recognition and developmental fate of pseudo-multinucleated eggs after in vitro fertilization of human oocytes. Hum Reprod 1987;2:217-225.
Van Blerkom J. Developmental failure in human reproduction associated with preovulatory oogenesis and preimplantation embryogenesis. En: Van Blerkom J, Motta PM, editors. Ultrastructure of human gametogenesis and early embryogenesis. Kluwer Academic Publishers; 1989. p.125-180.
Van Royen E, Mangelschots K, Vercruyssen M, De Neuburg D, Valkenburg M, Ryckaert G, et al. Multinucleation in cleavage stage embryos. Hum Reprod 2003;18:1062-1069.
Veeck LL. An atlas of human gametes and conceptuses. An illustrated reference for assisted reproductive technology. New York: The Parthenon Publishing Group Inc; 1999.
Wessel GM, Conner SD, Berg L. Cortical granule translocation is microfilament mediated and linked to meiotic maturation in the sea urchin oocyte. Development 2002;129:4315-4325.
Winston NJ, Braude P, Pickering S, George M, Cant A, Currie J, et al. The incidence of abnormal morphology and nucleocytoplasmic ratios in 2-3 and 5 day human pre-embryos. Hum Reprod 1991;6:17-24.