¿CÓMO Y PORQUÉ SE PRODUCE LA SEÑALIZACIÓN POR ONDAS DE CA2+ DURANTE LA FECUNDACIÓN?
Aida M. López-Guerrero1, Vanessa Casas-Rua2, Mario J. Perianes2, Patricia Tomás-Martín1, eulalia Pozo-Guisado1, Ignacio Santiago Álvarez-Miguel2,3, Francisco Javier Martín-Romero1
1Departamento de Bioquímica y Biología Molecular, Facultad de Ciencias, Universidad de extremadura, Badajoz.
2Departamento de Biología Celular, Facultad de Ciencias, Universidad de extremadura, Badajoz.
3Instituto extremeño de Reproducción Asistida-González Carrera (IeRA-GC), Badajoz.
email:fjmartin@unex.es
Resumen: La señalización mediada por Ca2+ es esencial en la fecundación de mamíferos ya que las variaciones en la concentración intracelular de este ión que se generan en el ovocito, conocidas como ondas de Ca2+, controlan casi todos los procesos necesarios para la progresión normal de la transición ovocito-zigoto-embrión. En este artículo nos centraremos en la descripción de los últimos avances en el estudio de los diferentes transportadores de Ca2+ en el ovocito que nos permitirán comprender la base molecular del origen de las ondas de Ca2+, de su transmisión por el citosol del ovocito, así como de sus consecuencias funcionales. La señalización mediada por Ca2+ es responsable de la activación de diferentes quinasas que controlan procesos relacionados con la salida del bloqueo meiótico y la evolución del ciclo celular. Además, dedicaremos un apartado para mostrar la participación de la entrada de Ca2+ regulada por depósitos intracelulares (store-operated calcium entry, SOCE) en la señalización ovocitaria durante la fecundación, y la especial sensibilidad de esta vía de entrada de Ca2+ al estrés oxidativo generado por la manipulación de los ovocitos durante su cultivo in vitro. Rev Asoc est Biol Rep 2010; 15(2):45-53.
Palabras clave: Calcio, fecundación, STIM1, canal SOC, estrés oxidativo
HOW AND WHY IS TRIGGERED THE CALCIUM WAVES–MEDIATED SIGNALING DURING FERTILIZATION?
Summary: Calcium signaling in the mammalian oocyte is essential at fertilization. The repetitive and transient increases of the intracellular free Ca2+ concentration, known as calcium waves, control almost all the oocyte events required for the progression of cell cycle and the zygote-embryo transition. In this review we will focus on the description of the recent knowledge regarding Ca2+ transport systems, required for the better understanding of the molecular basis of the generation and transmission of the calcium waves, as well as for the functional consequences in the oocyte. Ca2+-mediated signaling activates a series of protein kinases that control many cellular aspects, including the Ca2+ influx, the exit of meiotic arrest and cell cycle progression. In addition we will describe the contribution of the store-operated calcium entry (SOCE) to the Ca2+-dependent signaling in the mammalian oocyte at fertilization. Finally we will show how this Ca2+-influx is functionally altered by the oxidative stress generated by the culture media during the handling and in vitro culture of gametes during assisted reproduction techniques. Rev Asoc est Biol Rep 2010; 15(2):45-53.
Keywords: Calcium, fertilization, STIM1, SOC channel, oxidative stress
.
1. CALCIO COMO MENSAJERO INTRACELULAR
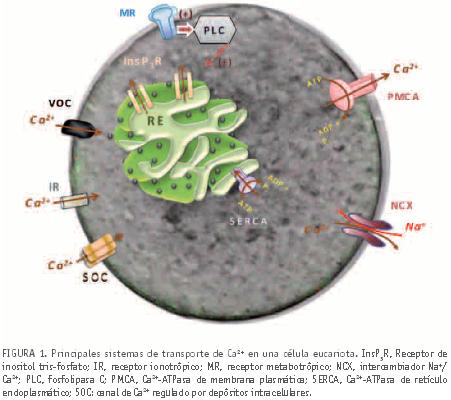
Entre los numerosos mensajeros intracelulares que podemos encontrar en las células eucariotas, la concentración de calcio citosólico destaca por su importancia ya que se encuentra implicada en un elevado número de eventos celulares, desde el control del ciclo celular hasta la muerte celular, ya sea apoptótica o necrótica, pasando por otros procesos como la transmisión de impulsos nerviosos, la contracción muscular, secreción, o fecundación. Sin embargo no es la concentración de calcio total la que actúa como señalizador, sino la concentración de calcio libre. En el citosol de las células eucariotas la concentración de Ca2+ libre ([Ca2+]i) es aproximadamente 100nM, muy inferior a la concentración de Ca2+ libre extracelular ([Ca2+]o) que suele ser 1-2 mM. Para mantener este gradiente de concentración se requiere la extrusión activa de Ca2+ al medio extracelular, acción que se lleva a cabo mediante bombas de Ca2+ denominadas Ca2+-ATPasas. Encontramos varios tipos de Ca2+-ATPasas en la célula, una de ellas localizada en la membrana plasmática, que se denomina PMCA, por sus siglas en inglés (plasma membrane Ca2+-ATPase). La PMCA emplea la energía liberada por la hidrólisis de ATP (adenosina-5’-trifosfato) para impulsar el transporte de Ca2+, en contra del gradiente de concentración, hacia el exterior de la célula (véase figura 1). A esta extrusión también colaboran otros sistemas, como el intercambiador Na+/Ca2+, que extruye Ca2+ gracias a la energía obtenida por el transporte de Na+ desde el medio extracelular al citosol.
A pesar de que estos sistemas mantienen los niveles basales de la [Ca2+]i, ésta sufre incrementos que pueden llegar hasta concentraciones micromolares en respuesta a una gran variedad de estímulos. El incremento de la [Ca2+]i viene facilitado por canales de Ca2+ que permiten la entrada de Ca2+ al citosol desde el exterior celular. También encontramos canales de Ca2+ en algunos orgánulos subcelulares, que permiten la salida parcial de Ca2+ desde estos orgánulos hacia el citosol. Es precisamente esta variación de la [Ca2+]i lo que se considera un mensajero intracelular, o segundo mensajero, (casi) universal (Bootman et al., 2001). Los estímulos que conducen a un incremento de la [Ca2+]i son muy variados: desde la despolarización de la membrana plasmática en el caso de células excitables, como neuronas o miocitos, hasta la unión de hormonas a receptores de superficie, o la propia fusión espermatozoide-ovocito, como veremos más adelante. El incremento de la [Ca2+]i en respuesta a la estimulación es muy variado en cuanto a frecuencia, duración y amplitud, dependiendo del tipo celular e incluso dentro del mismo tipo celular dependiendo del estado fisiológico o de la fase del ciclo celular.
En cualquier caso este incremento de la [Ca2+]i debe ser contrarrestado de alguna forma para que los niveles de Ca2+ citosólicos vuelvan a su nivel basal (aproximadamente 100 nM), transcurrido el estímulo. Es decir la señalización mediada por Ca2+, como cualquier otro señalizador fisiológico, tiene un tiempo de duración limitado y además es reversible. El mecanismo principal para disminuir la [Ca2+]i hasta niveles basales incluye los sistemas de extrusión localizados en la membrana plasmática antes mencionados (PMCA e intercambiador Na+/Ca2+) y de otro importante transportador activo que bombea Ca2+ desde el citosol hasta el principal depósito intracelular de Ca2+, el retículo endoplasmático (RE). Este transportador se denomina Ca2+-ATPasa de retículo endoplasmático o SERCA (sarco(endo)plasmatic reticulum Ca2+-ATPase) y permite que el RE actúe como reservorio o depósito de Ca2+ intracelular, alcanzándose concentraciones de Ca2+ intraluminales muy superiores a los niveles citosólicos. Además, en la membrana del RE existen canales de Ca2+ que permiten la salida de Ca2+ desde el RE al citosol. Entre estos canales podemos destacar los receptores de InsP3 (inositol1,4,5-trisfosfato), o InsP3R, que se activan tras la unión a este ligando intracelular, permitiendo la salida de Ca2+ desde el RE e incrementando temporalmente la [Ca2+]i.
Aunque existen muchos otros participantes en la regulación del transporte de Ca2+ en ovocitos, éstos son los actores principales en el esquema actualmente aceptado de la señalización mediada por Ca2+ en fecundación.
2. SEÑALIZACIÓN MEDIADA POR Ca2+ EN LA FECUNDACIÓN OOCITARIA. ONDAS DE Ca2+
Tal y como hemos mencionado antes, la fecundación representa un estímulo mediado por variaciones de la [Ca2+]i en el citosol del ovocito. Durante la fecundación de ovocitos de diferentes especies podemos observar un incremento en la [Ca2+]i que puede alcanzar valores de 1-3 μM. Este incremento es diferente tanto en tiempo global, como en frecuencia y amplitud dependiendo de las especies (Stricker, 1999), aunque para abreviar nuestra descripción nos centraremos en los ovocitos de mamíferos. En mamíferos, incluyendo la especie humana, tras la fusión espermatozoide-ovocito se producen elevaciones transitorias y repetitivas de la [Ca2+]i que son iguales en amplitud (es decir todas alcanzan el mismo nivel de concentración de Ca2+ citosólico, 1-3μM), como en duración (aproximadamente 1-2 minutos cada una). Estas elevaciones transitorias son conocidas como ondas de calcio y, aunque se generan en un punto localizado del ovocito, se transmiten muy rápidamente al resto del citosol. La frecuencia de estas ondas varía entre especies, pero en la mayoría se producen con una cadencia de 1 onda cada 10-20 minutos.
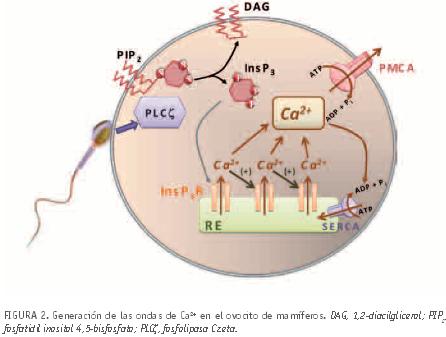
¿Cómo se inicia y transmite el proceso generador de ondas de calcio? Actualmente se encuentra muy aceptado el hecho de que las ondas de calcio se inician por una actividad enzimática específica del espermatozoide. Tras la fusión de membranas entre espermatozoide y ovocito, la fosfolipasa C zeta (PLCζ) del espermatozoide es liberada al citosol del ovocito (Saunders et al., 2002). La actividad PLCζ hidroliza el lípido de membrana fosfatidil inositol 4,5-bisfosfato (PIP2) produciendo cantidades significativas de inositol 1,4,5-trisfosfato (InsP3) y 1,2-diacilglicerol (DAG ). Mientras que DAG es hidrofóbico y queda retenido en la membrana plasmática del ovocito, el InsP3 es soluble y por lo tanto difunde con facilidad hacia el citosol. InsP3 se une a su receptor, InsP3R, localizado en la membrana del RE y que tiene actividad como canal de Ca2+, activando la salida de Ca2+ desde el interior del RE hacia el citosol (Malcuit et al., 2006) y de esta manera el espermatozoide induce la generación de la primera subida de la [Ca2+]i en el ovocito (figura 2). Además el canal InsP3R presenta un modo de regulación que provoca su activación por el propio Ca2+ citosólico, de modo que incrementos locales de la [Ca2+]i en las cercanías de un receptor InsP3R activan a este receptor, permitiendo la salida de más Ca2+ y activando a su vez a InsP3R vecinos, en un proceso conocido como liberación de Ca2+ inducida por Ca2+ (calcium-induced calcium release, CICR) que es la base de la transmisión de la onda de Ca2+ al resto del ovocito.
Una vez generada la liberación de Ca2+ desde el RE se activan mecanismos en el ovocito, como en otros tipos celulares, para restaurar los niveles basales de Ca2+ citosólico que permitan generar una nueva onda de Ca2+ con posterioridad. Entre estos mecanismos destaca la actividad de las bombas de Ca2+, PMCA y SERCA, que llevarán a cabo la extrusión de Ca2+ al exterior celular y el bombeo al interior del RE, respectivamente. de esta forma se alcanza en pocos segundos el nivel basal de Ca2+ citosólico. La PLCζ va a continuar activa en el ovocito durante varias horas, concretamente hasta la formación de los pronúcleos, por lo que esta ruta de señalización (liberación de InsP3→unión a InsP3R→salida de Ca2+ desde el RE →recaptura hasta el RE y extrusión al medio extracelular) va a ser predominante en el ovocito durante los primeros estadios de la fecundación. La proteína PLCζ presenta en su extremo N-terminal una secuencia que determina su localización nuclear (Larman et al., 2004), por lo que en ausencia de membrana nuclear, como ocurre durante la metafase de la segunda división meiótica en ovocitos maduros, su localización es citosólica. De esta forma el ovocito se asegura un tren de ondas de Ca2+ mientras no exista membrana nuclear. Cuando esta membrana se forma, la PLCζ queda secuestrada en los pronúcleos, es decir sin acceso directo al citosol, por lo que deja de producirse InsP3, y el tren de ondas de Ca2+ termina.
Es muy interesante el hecho de que una célula pueda mantener este tipo de señalización durante horas con el objetivo, como ya veremos más adelante, de salir del bloqueo meiótico en el que se encuentra el ovocito. Sin embargo, nuestro grupo de investigación se ha preguntado si la continua extrusión de Ca2+ al exterior del ovocito (mediante la PMCA) en este tipo de señalización tan repetitiva no estaría disminuyendo los niveles de Ca2+ dentro del RE, la fuente inicial de Ca2+ para generar las ondas. De ser así, el agotamiento o depleción de los niveles de Ca2+ intraluminales conduciría a la finalización temprana de las ondas de Ca2+, y por tanto al mantenimiento del bloqueo meiótico, es decir constituiría un fallo en la fecundación.
3. ¿CUÁLES SON LAS FUENTES DE Ca2+ PARA LA GENERACIÓN DE ONDAS?
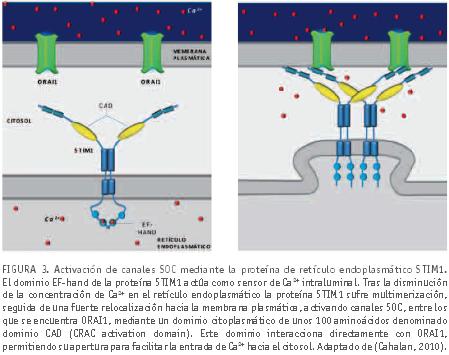
Para asegurar que los depósitos intracelulares de Ca2+ dentro del ovocito (principalmente el RE) no sufren una depleción que ponga en peligro la continuidad de la señalización mediada por Ca2+, existe un sistema de canales de Ca2+ en la membrana plasmática que están regulados precisamente por el nivel de Ca2+ intraluminal en el retículo endoplasmático (Gomez-Fernandez et al., 2009; Koh et al., 2009). Estos canales de Ca2+ permiten la entrada de Ca2+ desde el exterior celular al citosol, para que la SERCA pueda bombear Ca2+ al interior del RE, y así restaurar los niveles de Ca2+ intraluminales. Por ello estos canales se denominan canales de Ca2+ regulados por depósitos intracelulares, o canales SOC (store-operated Ca2+ channels) y la entrada de Ca2+ extracelular a través de estos canales SOC se denomina entrada de Ca2+ regulada por depósitos intracelulares o SOCE (store-operated calcium entry). Esta vía de entrada, SOCE, se definió por primera vez en 1986 (Putney, 1986) y hoy sabemos que esta ruta de entrada de Ca2+ es activa en todos los tipos celulares, incluyendo los ovocitos humanos (Martin-Romero et al., 2008b), aunque la contribución de esta vía a la señalización mediada por Ca2+ difiere de un tipo celular a otro. Los mecanismos por lo cuales los canales SOC localizados en la membrana plasmática son sensibles al nivel de llenado del RE están aún por aclarar, aunque es conocido que en este mecanismo participa una proteína denominada STIM1 (stromal interaction protein 1) (Liou et al., 2005; Roos et al., 2005). STIM1 es una proteína transmembranal localizada en la membrana del RE, con un dominio “EF-hand” de unión a Ca2+, cerca del extremo N-terminal, que le permite actuar como sensor de Ca2+ intraluminal. El dominio citosólico presenta varios dominios entre los que destaca un doble dominio “coiled-coil” cuya función es la activación de canales SOCs localizados en la membrana plasmática (figura 3).
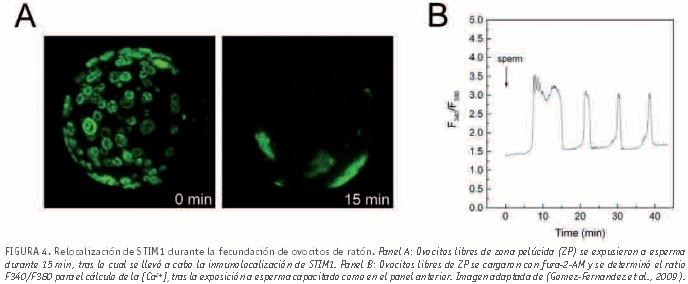
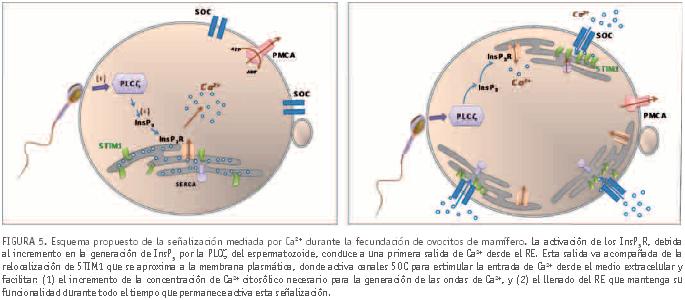
Cuando la concentración de Ca2+ dentro del RE disminuye por debajo de 200μM, STIM1 sufre oligomerización y se produce la aproximación de STIM1 hacia la membrana plasmática, formándose yuxtaposiciones RE-membrana plasmática (Liou et al., 2007; Muik et al., 2008; Smyth et al., 2008). Esta oligomerización es necesaria para la activación de los canales SOC de membrana plasmática. De esta forma gracias a STIM1 se establece un puente entre el exterior celular y el RE para reponer la concentración de Ca2+ dentro de este orgánulo y asegurar que el RE no sufrirá grandes cambios de concentración de Ca2+, permitiendo la continuidad de las ondas de Ca2+ durante un largo periodo de tiempo. Empleando un modelo murino, nuestro grupo de investigación ha demostrado recientemente que la proteína STIM1 es funcionalmente activa en ovocitos (Gomez-Fernandez et al., 2009), y que la activación de los canales SOC es un proceso muy temprano en la fecundación (≈10 minutos tras el inicio de la fecundación), lo que apoya la hipótesis de que esta vía de entrada de Ca2+ extracelular (SOCE) no sólo constituye un modo de mantener la señalización mediada por Ca2+ a largo plazo, sino que probablemente participa en la generación de las primeras ondas de Ca2+. Esta hipótesis se sustenta en dos hechos constatados experimentalmente: (a) cuando se transfieren los ovocitos a una solución libre de Ca2+, la señalización mediada por Ca2+ cesa inmediatamente (Kline and Kline, 1992), y (b) la relocalización de STIM1 se observa de forma concomitante a la generación de la primera onda de Ca2+ (Gomez-Fernandez et al., 2009) (ver figura 4). Por ello nuestro grupo ha propuesto una modificación al esquema hasta ahora aceptado y mostrado en la figura 2, en la que se incluye la participación temprana de STIM1. De esta forma, tras la liberación de PLCζ al citosol, se produciría una salida masiva de Ca2+ desde el RE, lo que llevaría asociado una fuerte relocalización de STIM1 para activar canales SOC que permitirían la entrada de Ca2+ desde el exterior celular contribuyendo a la generación de las ondas de Ca2+ (figura 5). Esto explicaría que los ovocitos requieran Ca2+ extracelular durante su fecundación y terminaría por contestar la pregunta inicial: las fuentes de Ca2+ para la generación de ondas son el RE y el medio extracelular.
4. EL INFLUJO DE Ca2+ A TRAVÉS DE CANALES SOC ES SENSIBLE A ESTRÉS OXIDATIVO
Según lo expuesto sería muy interesante conocer la naturaleza molecular de estos canales de Ca2+, los canales SOC, que se expresan y son activos en el ovocito. Durante más de dos décadas los investigadores han tratado de definir qué proteínas eran las encargadas de constituir los canales SOC empleando otros tipos celulares, y no fue hasta el año 2006 cuando se describió ORAI1 (también conocida como CRACM1), una proteína de membrana plasmática con cuatro segmentos transmembranales que constituye el canal responsable de la entrada de Ca2+ regulada por depósitos intracelulares (Feske et al.,2006; Soboloff et al., 2006; Vig et al., 2006; Zhang et al., 2006). Además de unirse a ORAI1, STIM1 se une a otros canales de Ca2+, impulsando de esta forma su actividad como canal SOC: los canales de la familia TRPC (transient receptor potential canonical channels) (Yuan et al., 2007). Hoy conocemos que STIM1 interacciona directamente, además de con ORAI1, con TRPC1, TRPC4 y TRPC5, e incluso forma interacciones heteroméricas con TRPC1 y ORAI1,constituyendo complejos TRPC1-ORAI1-STIM1 que actúan como canales SOCs con diferentes propiedades de conductancia (Ambudkar et al., 2007). Sin embargo, los canales TRPC pueden actuar de forma dependiente de STIM1 o de forma independiente de STIM1, y es el ratio STIM1/TRPC lo que determina que estos canales actúen regulados dependiendo del nivel de llenado del RE, o independientes de este nivel, es decir que actúen como canales SOC o no (Lee et al., 2010).
Debido a su papel fundamental en la generación de ondas de Ca2+ durante la fecundación resulta necesario determinar qué proteínas actúan como canales SOC en el ovocito, ya que este estudio nos permitirá no sólo avanzar en el conocimiento en este área de la biología reproductiva, sino aprovechar esta información con efectos prácticos durante el empleo de técnicas de reproducción asistida, puesto que los diversos canales muestran diferente farmacología. Con este objetivo nuestro grupo de investigación trabaja actualmente en la identificación de estos canales en ovocitos de ratón, y en la evaluación de su participación activa en la señalización mediada por Ca2+ en fecundación. Además de esta identificación molecular hemos constatado que la entrada de Ca2+ a través de estos canales es muy sensible a especies reactivas de oxígeno (reactive oxygen species, ROS) generadas en el medio de cultivo (Martin-Romero et al., 2008b). Este hecho es de una importancia crítica, puesto que los gametos, durante su manipulación en el laboratorio y durante su cultivo in vitro, están expuestos a niveles de ROS muy superiores a los que se generan en situaciones fisiológicas debido principalmente a que la tensión de oxígeno (O2) atmosférica es significativamente mayor que la tensión de O2 in vivo. Empleando sondas sensibles a diversas ROS hemos demostrado que los medios de cultivo comerciales habitualmente empleados en centros de reproducción asistida generan ROS, entre las que destaca peróxido de hidrógeno (H2O2),ya que se pueden llegar a alcanzar concentraciones de esta especie del orden de micromolar (Martin-Romero et al., 2008a). Este hecho puede explicarse en base a la combinación de luz +O2 atmosférico + presencia en los medios de cultivo de agentes fotosensibles como la riboflavina, aminas, nucleótidos de piridina, etc., que pueden actuar como generadores fotoquímicos de anión superóxido (O2-) y oxígeno singlete (Cunningham et al., 1985; Michelson, 2000; Wells-Knecht et al., 1995). La generación de O2·- potencia la formación de H2O2, y éste último reacciona con O2·- (reacción de Haber-Weiss) para producir radicales hidroxilo y peroxilo (Michelson, 2000), amplificando la generación de ROS. El líquido folicular por el contrario no produce cantidades significativas de ROS y los niveles de H2O2 en este fluido se encuentran en el intervalo submicromolar (Martin-Romero et al., 2008a). La exposición de los ovocitos a concentraciones micromolares de H2O2 de forma sostenida durante todo el proceso de aislamiento de los ovocitos, denudación y posterior FIV/ICSI, conduce a la disminución del contenido en glutatión reducido (GSH), un importante antioxidante no enzimático intracelular, así como al incremento de la peroxidación lipídica (Martin-Romero et al., 2008a), y todos estos procesos conducen finalmente a la desregulación de la homeostasis de Ca2+ libre citosólico.
En trabajos paralelos hemos descrito que la desregulación inducida por estrés oxidativo se produce fundamentalmente por una sobrecarga del ovocito debido a la entrada descontrolada de Ca2+ a través de canales SOC (Martin-Romero et al.,2008b). Esta desregulación tiene una importante consecuencia, la finalización temprana de la generación de las ondas de Ca2+ y por lo tanto el mantenimiento del bloqueo meiótico. Hemos observado que el empleo de bloqueantes específicos de canales SOC protege al ovocito de esta sobrecarga de Ca2+. Sin embargo, no es posible usar de forma rutinaria bloqueantes de canales SOC en medios de cultivo ya que la entrada controlada y regulada de Ca2+ a través de estos canales SOC (la entrada regulada por STIM1) es necesaria para el progreso de la fecundación. Por ello, nuestra recomendación, a la luz de nuestros propios datos experimentales, es que se deben acortar los tiempos de incubación de ovocitos en los tampones y medios de cultivo en la medida de lo posible, mientras que es posible prolongar los tiempos de espera en el propio líquido folicular o en medios de cultivo de composición química sencilla (Martin-Romero and Álvarez, 2008; Martin-Romero et al., 2008a; Varghese et al., 2010, in press). De hecho existen resultados experimentales que apoyan esta recomendación, ya que en un modelo murino las tasas de embarazo tras FIV y posterior cultivo embrionario son superiores cuando el cultivo se lleva a cabo en un medio químicamente definido en comparación con medios más complejos suplementados con suero (Han and Kiessling, 1988).
5. LAS ONDAS Ca2+ SE REQUIEREN PARA LA PROGRESIÓN DEL CICLO CELULAR
La generación de las ondas de Ca2+ durante la fecundación sigue un patrón específico muy determinado. Hemos visto hasta ahora cómo y por qué se generan estas ondas, pero ¿Cuál es su función? ¿Cuál es la diana molecular que se activa gracias a estas ondas? ¿Qué relación hay entre estas ondas y la salida del bloqueo meiótico? En primer lugar hay que aclarar que las dianas moleculares activadas por el tren de ondas de Ca2+ es múltiple, pero destacan una serie de proteínas quinasas, entre ellas la extracellular signal-regulated kinase 1 y 2 (ERK1/2, Ca2+/calmodulin-dependent kinase II (CaMKII), protein kinase C (PKC) y la cyclin dependent kinase 1 (CDK1 o p34cdc2), por su estrecha relación con la salida del bloqueo meiótico que se produce durante la fecundación (Ducibella and Fissore, 2008).
Las quinasas ERK1/2 se activan por incrementos en la [Ca2+]i, y aunque esta activación es indirecta tiene particular relevancia ya que nuestro grupo ha descrito recientemente que STIM1 es diana de la actividad ERK1/2 tanto in vitro como in vivo , y que la fosforilación de STIM1 en residuos de serina dianas de ERK1/2 (Ser575, Ser608 y Ser621) es necesaria para que puedan activarse los canales SOC (Pozo-Guisado et al.,2010), permitiendo la entrada de Ca2+ extracelular para continuar con la generación de ondas de Ca2+. Aunque inicialmente se sugirió que la PKC también podría regular positivamente la entrada de Ca2+ (Halet et al., 2004), hemos comprobado que STIM1 no es diana de PKC y recientemente se ha descrito que PKC fosforila a ORAI1, pero esta fosforilación conduce a su inhibición como canal SOC y no a su activación (Kawasaki et al., 2010).
En 2002 se describió que la actividad del complejo MPF (M-phase Promoting Factor), que mantiene el bloqueo meiótico en los ovocitos maduros MII, se regula de forma proporcional al número de oscilaciones de la [Ca2+]i y al tiempo total en el que la [Ca2+]i permanece elevada (Nixon et al., 2002). El complejo MPF está constituido por la quinasa CDK1 que actúa como subunidad enzimática, y por la ciclina B1, que actúa como subunidad reguladora (Labbe et al., 1989). Una elevada actividad del complejo MPF es responsable del bloqueo meiótico, pero la disminución de los niveles de ciclina B1, conduce a una disminución de la actividad del complejo MPF y a la salida del bloqueo meiótico. Durante la fase M del ciclo celular la cantidad de ciclina B1 está regulada por su proteólisis controlada mediante el proteosoma 26S. La degradación de la ciclina B1 está estimulada por su poli-ubiquitinación, una modificación post-traduccional que consiste en incorporar cadenas de ubiquitina (Ub, una proteína de 76 aminoácidos) unidas a residuos de lisina de la diana molecular. Esta modificación post-traduccional es debida a una serie de enzimas específicas, denominadas genéricamente E3 ligasa, que reconocen el sustrato para ser marcado con poli-Ub. En el caso de la ciclina B1, la E3 ligasa del complejo APC/C (anaphase promoting complex) es la responsable de su ubiquitinación y posterior degradación por el proteosoma 26S. El grupo de Keith T. Jones demostró empleando ovocitos de ratón que la degradación de ciclina B1 dependiente de APC/C se inicia cuando la concentración de [Ca2+]i en el ovocito supera un umbral mínimo (≈600 nM), tras la fecundación. Sin embargo esta degradación no es completa tras la primera onda de Ca2+ como ocurre en Xenopus y en otros organismos en los que sólo se observa un único aumento de la [Ca2+]i tras la fusión espermática (una única onda). Para continuar con la degradación de la ciclina B1 se requieren en mamíferos múltiples ondas de Ca2+ y cada una de ellas solapa con una disminución significativa en el nivel de ciclina B1 y, de forma consecuente, en la actividad MPF responsable del bloqueo meiótico (Nixon et al., 2002). Como consecuencia, tras una serie de ondas de Ca2+ de forma repetitiva, la ausencia de ciclina B1 conduce finalmente al reinicio del ciclo celular con la conclusión de la meiosis.
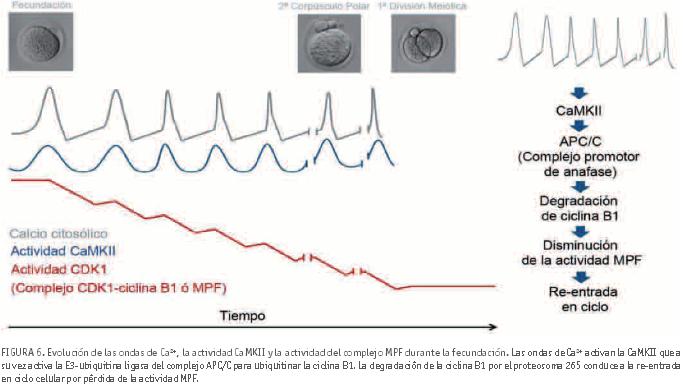
Pero, ¿cuál es la conexión entre la [Ca2+]i y el complejo MPF? La respuesta se encuentra en la CaMKII, que controla indirectamente la actividad del complejo MPF. Es conocido desde hace casi dos décadas que existe una correlación entre la actividad CaMKII y la progresión del ciclo celular. La actividad de la CaMKII es regulada por el complejo Ca2+/calmodulina, lo que ha originado diversas hipótesis para explicar la relación que existe entre los incrementos cíclicos de la [Ca2+]i, la actividad CaMKII y el complejo MPF. En primer lugar hay que destacar que el aumento cíclico de la [Ca2+]i, como el que ocurre en fecundación, lleva asociado una estimulación de la actividad CaMKII también de forma cíclica, de forma que existe una elevada sincronización entre ambos eventos celulares (Markoulaki et al., 2004) (ver figura 6). Durante cada onda de activación de la CaMKII, ésta a su vez activa la E3 Ub ligasa del complejo APC/C, aunque esta activación es indirecta y en ella participan otros elementos (ver revisión en Ducibella and Fissore, 2008). La activación del complejo APC/C conduce a la poli-ubiquitinación de la ciclina B1 del complejo MPF y su degradación por el proteosoma 26S, estimulando la salida del bloqueo meiótico. En resumen, existe una elevada correlación causal y temporal entre onda de Ca2+→ activación de CaMKII→ubiquitinación de ciclina B1 (y su posterior degradación)→disminución de la actividad del complejo MPF.
6. CONSIDERACIONES FINALES
Teniendo en cuenta todo lo expuesto en esta revisión, cabe preguntarse por tanto, ¿qué ocurre cuando no se alcanza un número adecuado de ondas de Ca2+ durante la fecundación oocitaria? ¿Qué ocurre cuando el incremento de la [Ca2+]i no alcanza el umbral descrito de 600 nM para activar la CaMKII? La primera situación podría presentarse durante la actividad clínica en aquellos casos en los que se emplean espermatozoides defectivos en PLCζ, o bien cuando se emplean ovocitos no maduros citosólicamente, es decir ovocitos que a pesar de mostrar un claro corpúsculo polar no muestran una elevada densidad de InsP3. En todos estos casos no se conseguirá una sucesión de ondas con una frecuencia y amplitud adecuadas para degradar totalmente ciclina B1, por lo que el ovocito no progresará en ciclo celular. Por ello, los estudios encaminados a determinar marcadores moleculares de maduración citosólica resultan especialmente necesarios. La densidad de canales InsP3, así como la densidad de bombas SERCA, son dos marcadores de maduración citosólica que pueden emplearse en estudios de maduración ovocitaria y que podrían ser útiles para la evaluación de la eficiencia de diferentes medios de maduración in vitro (IVM). Por otro lado hemos destacado que los canales SOC del ovocito son especialmente sensibles a modulación redox, de modo que un incremento en el nivel ROS puede llegar a sobreactivar estos canales, alterando la frecuencia de las ondas de Ca2+ y frustrando la fecundación. En definitiva, se requieren estudios básicos para conocer todos los detalles moleculares que rigen la función de los principales transportadores de Ca2+ en el ovocito, ya sean bombas o canales de Ca2+, que nos permitan manipular estas células con el objetivo de asegurar tasas de éxito en FIV muy superiores a las actuales.
AGRADECIMIENTOS
La financiación del grupo de investigación es llevada a cabo gracias a proyectos financiados en convocatorias competitivas del ministerio de ciencia e innovación (BFU2008-00104) y de la Junta de Extremadura-Fondo Social Europeo (PDT08A027). AML-G, VC-R, MJP, PT-M y EP-G están contratados con financiación de la Junta de Extremadura-Fondo Social Europeo y de la Universidad de Extremadura. Agradecemos a todo el personal del Instituto Extremeño de Reproducción Asistida-González Carrera su colaboración en la ejecución de los experimentos realizados con muestras de origen humano.
Referencias
Ambudkar IS, Ong HL, Liu X, Bandyopadhyay B, Cheng KT . TRPC1: the link between functionally distinct store-operated calcium channels. Cell Calcium 2007; 42:213-223
Bootman MD, Collins TJ, Peppiatt CM, Prothero LS, MacKenzie L, De Smet P, et al. Calcium signalling--an overview. Semin Cell Dev Biol 2001; 12:3-10.
Cahalan MD. Cell biology. How to STIMulate calcium channels. Science 2010; 330:43-44.
Cunningham ML, Krinsky nI, Giovanazzi SM, Peak MJ. Superoxide anion is generated from cellular metabolites by solar radiation and its components. Free Radic Biol Med 1985; 1:381-385.
Ducibella T, Fissore R. The roles of Ca2+, downstream protein kinases, and oscillatory signaling in regulating fertilization and the activation of development. Dev Biol 2008; 315:257-279.
Feske S, Gwack y, Prakriya M, Srikanth S, Puppel SH, Tanasa B, et al. A mutation in Orai1 causes immune deficiency by abrogating CRAC channel function. nature 2006; 441:179-185.
Gomez-Fernandez C, Pozo-Guisado e ,Ganan-Parra M, Perianes MJ, Alvarez IS, Martin-Romero FJ. Relocalization of STIM1 in mouse oocytes at fertilization: early involvement of store-operated calcium entry. Reproduction 2009; 138:211-221.
Halet G, Tunwell R, Parkinson SJ, Carroll J. Conventional PKCs regulate the temporal pattern of Ca2+ oscillations at fertilization in mouse eggs. J Cell Biol 2004; 164:1033-1044.
Han HD, Kiessling AA. In vivo development of transferred mouse embryos conceived in vitro in simple and complex media. Fertil Steril 1988; 50:159-163.
Kawasaki T, Ueyama T, Lange I, Feske S, Saito n. Protein kinase C-induced phosphorylation of Orai1 regulates the intracellular Ca2+ level via the store-operated Ca2+ channel. J Biol Chem 2010; 285:25720-25730.
Kline D, Kline JT. Thapsigargin activates a calcium influx pathway in the unfertilized mouse egg and suppresses repetitive calcium transients in the fertilized egg. J Biol Chem 1992; 267:17624-17630.
Koh S, Lee K, Wang C, Cabot RA, Machaty Z. STIM1 regulates store-operated Ca2+ entry in oocytes. Dev Biol 2009; 330:368-376.
Labbe JC, Capony JP, Caput D, Cavadore JC, Derancourt J, Kaghad M, et al. MPF from starfish oocytes at first meiotic metaphase is a heterodimer containing one molecule of cdc2 and one molecule of cyclin B.eMBOJ 1989; 8:3053-3058.
Larman MG, Saunders CM, Carroll J, Lai FA, Swann K. Cell cycle-dependent Ca2+ oscillations in mouse embryos are regulated by nuclear targeting of PLCzeta. J Cell Sci 2004; 117:2513-2521.
Lee KP, y uan JP, So I, Worley PF, Muallem S. STIM1-dependent and STIM1-independent function of TRPC channels tunes their store-operated mode. J Biol Chem 2010; In Press.
Liou J, Fivaz M, Inoue T, Meyer T. Live-cell imaging reveals sequential oligomerization and local plasma membrane targeting of stromal interaction molecule 1 after Ca2+ store depletion. Proc natl Acad Sci U S A2007; 104:9301-9306
Liou J, Kim ML, Heo WD, Jones JT, Myers JW, Ferrell Je, Jr., et al. STIM is a Ca(2+) sensor essential for Ca(2+)-store-depletion-triggered Ca(2+) influx. Curr Biol 2005;15:1235 -1241.
Malcuit C, Kurokawa M, Fissore RA. Calcium oscillations and mammalian egg activation. J Cell Physiol 2006; 206:565-573.
Markoulaki S, Matson S, Ducibella T. Fertilization stimulates long-lasting oscillations of CaMKII activity in mouse eggs. Dev Biol 2004; 272:15-25.
Martin-Romero FJ, Álvarez IS. Reactive oxygen and nitrogen species in reproductive biology. en: Gutiérrez-Merino C, Leeuwenburgh C, editors. Free Radicals in Biology and Medicine. Research Signpost:Kerala (India); 2008.
Martin-Romero FJ, Miguel-Lasobras eM, Dominguez-Arroyo JA, Gonzalez-Carrera e,Alvarez IS. Contribution of culture media to oxidative stress and its effect on human oocytes. Reprod Biomed Online 2008a; 17:652-661.
Martin-Romero FJ, Ortiz-de-Galisteo JR, Lara-Laranjeira J, Dominguez-Arroyo JA, Gonzalez-Carrera e, Alvarez IS. Store-operated calcium entry in human oocytes and sensitivity to oxidative stress. Biol Reprod 2008b; 78:307-315
Michelson AM. Photochemical production of oxy radicals. en: Greenwald RA, editor. Handbooks of Methods for Oxygen Radical Research. CRC Press: Boca Raton, Florida; 2000. p. 71-75.
Muik M, Frischauf I, Derler I, Fahrner M, Bergsmann J,eder P, et al. Dynamic coupling of the putative coiled-coil domain of ORAI1 with STIM1 mediates ORAI1 channel activation. J Biol Chem 2008; 283:8014-8022.
nixon VL, Levasseur M, McDougall A, Jones KT. Ca(2+) oscillations promote APC/C-dependent cyclin B1 degradation during metaphase arrest and completion of meiosis in fertilizing mouse eggs. Curr Biol 2002; 12:746-750.
Pozo-Guisado e, Campbell DG, Deak M,Alvarez-Barrientos A, Morrice nA, Alvarez IS, et al. Phosphorylation of STIM1 ate RK1/2 target sites modulates store-operated calcium entry. J Cell Sci 2010;123:3084-3093.
Putney JW, Jr. A model for receptor-regulated calcium entry. Cell Calcium 1986;7:1-12.
Roos J, DiGregorio PJ,yeromin AV, Ohlsen K, Lioudyno M, Zhang S, et al. STIM1, an essential and conserved component of store-operated Ca(2+) channel function. J Cell Biol 2005; 169:435-445.
Saunders CM, Larman MG, Parrington J, Cox LJ, Royse J, Blayney LM, et al. PLC zeta: a sperm-specific trigger of Ca(2+) oscillations in eggs and embryo development. Development 2002; 129:3533-3544.
Smyth JT, Dehaven WI, Bird GS, Putney JW, Jr. Ca2+-store-dependent and -independent reversal of Stim1 localization and function. J Cell Sci 2008; 121:762-772.
Soboloff J, Spassova MA, Tang XD, Hewavitharana T, Xu W, Gill DL. Orai1 and STIM reconstitute store-operated calcium channel function. J Biol Chem 2006; 281:20661-20665.
Stricker SA. Comparative biology of calcium signaling during fertilization and egg activation in animals. Developmental Biology 1999; 211:157-176
Varghese A, Pozo-Guisado e, Alvarez IS, Martin-Romero FJ. extended embryo Culture Supplementation. en: Agarwal A, editor. Male Infertility: Contemporary Concepts and the role of Antioxidants. Springer-Verlag: USA; 2010. en prensa.
Vig M, Peinelt C, Beck A, Koomoa DL, Rabah D, Koblan-Huberson M, et al. CRACM1 is a plasma membrane protein essential for store-operated Ca(2+) entry. Science 2006; 312:122 0 -1223.
Wells-Knecht KJ, Zyzak DV, Litchfield Je, Thorpe SR, Baynes JW. Mechanism of autoxidative glycosylation: identification of glyoxal and arabinose as intermediates in the autoxidative modification of proteins by glucose. Biochemistry 1995; 34:3702-3709.
yuan JP, Zeng W, Huang Gn, Worley PF, MuallemS. STIM1 heteromultimerizes TRPC channels to determine their function as store-operated channels. nat Cell Biol 2007; 9:636-645.
Zhang SL,yeromin AV, Zhang XH,yuy,Safrina O, Penna A, et al. Genome-wide RNAi screen of Ca(2+) influx identifies genes that regulate Ca(2+) release-activated Ca(2+) channel activity. Proc natl Acad Sci U S A 2006; 103:9357-9362