IMPLEMENTACIÓN DE LOS NUEVOS CRITERIOS DE LA OMS EN LA PRÁCTICA CLÍNICA
Cristina González Ravina1,3, Alberto Pacheco Castro2,3
1Laboratorio de Andrología y Banco de Semen. Clínica IVI Sevilla
2Laboratorio de Andrología y Banco de Semen. Clínica IVI Madrid,
3Grupo de Interés de Andrología ASEBIR
Como es bien sabido, el primer Manual de Laboratorio para el análisis de semen humano y su interacción con el moco cervical se publicó en 1980, en respuesta a la elevada necesidad de estandarizar los protocolos para dicho análisis (WHO Laboratory Manual, 1999a). Dicho manual ha sido sometido a 3 revisiones posteriores, y el año pasado, la OMS elaboró la 5a edición del “Manual para el examen y procesamiento del semen humano”. En esta última versión, entre otros aspectos, se han revisado los valores de referencia,el algoritmo para los diagnósticos y la interpretación clínica de estos diagnósticos. Hasta el año pasado, en todos los laboratorios de Andrología, así como los de reproducción asistida, se trabajaba conforme a las directrices recomendadas en los tres manuales de 1999 (WHO, 1999a, b y c).
Haciendo un breve repaso de los mismos, así como de los valores de referencia existentes hasta el 2010, observamos que si bien cuando se establecieron en 1999 podrían haberse considerado como útiles, con el paso de los años se fue haciendo evidente una necesaria actualización de los mismos. No debemos olvidar que los trabajos realizados para establecer los valores de referencia en 1999 se basaron en el análisis de dos muestras de semen de un número no muy elevado de varones, en diferentes laboratorios en los que no se había estandarizado los métodos de trabajo ni implantado los sistemas de calidad correspondientes.
En el manual publicado en 1999, los espermatozoides se clasificaban en 4 categorías en función de la movilidad: tipo a (móviles progresivos rápidos), tipo b (móviles progresivos lentos), tipo c (móviles no progresivos) y tipo d (inmóviles). Una de las principales limitaciones de aquella clasificación es que se reconoció que el estudio de la movilidad progresiva espermática (espermatozoides tipo a y b), así como el de la morfología, aparte de ser subjetivos no estaban sujetos a ningún protocolo bien estandarizado entre los laboratorios (Cooper et al., 1992; Dunphy et al., 1989; Neuwinger et al., 1990). Sin embargo, los valores obtenidos para la concentración espermática y la movilidad total (a+b+c) sí se consideraron aceptables, puesto que podían medirse de manera reproducible en la mayoría de los centros. Por esto, se recomendó que cada laboratorio estableciese sus valores límite de normalidad para dichas variables, y que además incluyese los adecuados controles de calidad tanto interno como externo, que han quedado ampliamente desarrollados en el nuevo manual de 2010.
A pesar de todo, comparando las características espermáticas de una serie de varones y utilizando análisis estadístico, se definieron rangos de referencia para los principales parámetros seminales atendiendo a su capacidad para discriminar entre las dos poblaciones estudiadas (fértil vs sub- fértil o sub-fértil vs infértil) (Comhaire et al., 1987; Ombelet et al., 1997a).
Con respecto a la morfología, el manual refiere la puesta en marcha de un estudio multicéntrico para el análisis de este parámetro seminal. En esta edición de 1999 se especifica que los datos obtenidos en centros con programas de reproducción asistida sugieren que valores de morfología por debajo del 15% están relacionados con una disminución de la tasa de fecundación en FIV (Ombelet et al., 1997b).
En cuanto a la nomenclatura, los términos utilizados para expresar valores del seminograma por debajo de los valores de referencia son:
ASTENOZOOSPERMIA: móviles progresivos <50% a+b o <25% a
OLIGOZOOSPERMIA: concentración < 20 millones/ml
TERATOZOOSPERMIA: morfología < 15% formas normales
NECROZOOSPERMIA: vitalidad < 75 %
CRIPTOZOOSPERMIA: ausencia de espermatozoides en la muestra de eyaculado en su análisis inicial, y presencia de espermatozoides tras la centrifugación.
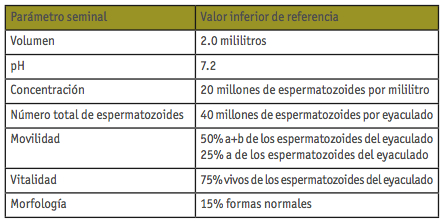
En la tabla se muestran los valores de referencia establecidos en 1999:
AZOOSPERMIA: ausencia de espermatozoides en la muestra de eyaculado en su análisis inicial y ausencia de espermatozoides tras la centrifugación. Concentración = 0.
ASPERMIA: ausencia de eyaculado. Volumen = 0.
En base a la clasificación seminal del varón, su historia clínica y su exploración física (así como cualquier otra información adicional) se podría dar el diagnóstico del varón atendiendo a un diagrama que recoge diferentes situaciones en cuanto a la concentración espermática, desde muestras con azoospermia, criptozoospermia u oligozoospermia (WHO, 1999). Cabe destacar que en el manual de 1999 se utiliza una subclasificación de las distintas alteraciones seminales (oligo-, asteno-, terato-, necrozoospermia) en grados que van de leve a grave pasando por moderado.
NOVEDADES DEL MANUAL OMS 2010
Tras 11 años desde la edición de 1999, se hizo cada vez más necesaria una revisión y actualización de los valores de referencia y los protocolos de trabajo establecidos, de manera que la nueva edición online del Manual OMS de 2010 presenta un nivel de detalle mucho más elevado en cuanto al análisis seminal: soluciones de trabajo, procedimientos, cálculos e interpretación de los resultados. Además recomienda usar un método concreto en aquellos casos en que exista más de una posibilidad o técnica de análisis.
Dentro de este aspecto, los principales cambios reflejados en la 5a edición incluyen:
a) un nuevo protocolo de trabajo a la hora de realizar el recuento de la concentración espermática. Se han modificado las diluciones de semen recomendadas y las áreas de la cámara de recuento necesarias para establecer el número de espermatozoides (concentración) con objeto de poder contar 200 espermatozoides por replicado. Se hace mayor hincapié en reducir los errores de muestreo, dando un mayor peso al volumen de la muestra (que antes no era tan relevante) que debe ser medido con precisión utilizando el método recomendado por la OMS
b) respecto al diagnóstico de azoospermia, se profundiza en el protocolo de trabajo a seguir con este tipo de muestras en las que no se encuentran espermatozoides en el eyaculado, diferenciando entre la necesidad de obtener un valor de concentración y/o movilidad preciso o centrifugar la muestra para aumentar la probabilidad de encontrar espermatozoides tras el lavado
c) se recogen cambios muy significativos en las categorías de movilidad espermática. Se recomienda a partir de ahora diferenciar los espermatozoides únicamente según 3 categorías: móviles progresivos (PM) (uniendo las anteriores categorías a y b), móviles no progresivos (NP) (la anterior categoría c) e inmóviles (IM) (como categoría previa d)
d) en esta edición se recoge con mayor detalle el análisis de la morfología, y se incluyen fotos de espermatozoides considerados normales y espermatozoides con una o varias anomalías morfológicas, así como explicaciones precisas para mejorar la formación de los técnicos en el estudio de dicho parámetro seminal
Por otra parte, cuenta con un capítulo sobre criopreservación de semen ampliado e incluido en el apartado de preparación de semen; así como un capítulo entero dedicado a los controles de calidad, que aparte de novedoso supone una recomendación de la OMS para tener garantía de calidad en nuestros laboratorios. Incluye tanto el control de calidad externo como el interno.
Con todo ello, la 5a edición del Manual queda dividida en 3 partes:
– Análisis de semen (capítulos 2-4) – técnicas estándar
– tests opcionales – tests de investigación
– Preparación de semen (capítulos 5 y 6) – Control de calidad (capítulo 7)
CRITERIOS DE INCLUSIÓN Y METODOLOGÍA EMPLEADA
Para el estudio se analizaron las muestras de semen de unos 4500 varones de 14 países y 4 continentes, divididos en 3 grandes grupos: varones fértiles, varones de fertilidad desconocida y varones normozoospérmicos según el manual de 1999. El grupo de varones cuya pareja había conseguido gestación en un plazo ≤ 12 meses se escogió como grupo control para establecer los valores de referencia de los parámetros seminales (1953 varones, 5 estudios en 8 países de 3 continentes).
Todos los laboratorios que participaron en el estudio obtuvieron los datos utilizando métodos estandarizados de análisis seminal (WHO, 1999a, b). Como en dicho manual se ofrecen diferentes métodos para la determinación del volumen, la concentración espermática y la tinción morfológica, el método empleado en cada laboratorio se ha tenido en cuenta a la hora de valorar los resultados. Además, en muchos laboratorios se implantaron con retraso controles de calidad externos e internos, por lo que los datos se han revisado para calcular la distribución de referencia teniendo en cuenta este hecho (Castilla et al., 2006).
Para el estudio se utilizó una única muestra de semen eyaculado por varón, que fue recogida con un periodo de abstinencia sexual de 2 a 7 días. La concentración se midió en la mayoría de los casos empleando el hemocitómetro de Neubauer mejorado, y, respecto a la movilidad, se recogieron datos sobre movilidad total (WHO 1999: a+b+c) y movilidad progresiva (WHO 1999: a+b) (Cooper and Yeung., 2006). Los datos de morfología se tuvieron en cuenta sólo de aquellos centros que utilizaron el criterio estricto de Tygerberg (WHO, 1999), y para la vitalidad (analizada por tinción eosina-nigrosina), el número de muestras estudiadas fue significativamente menor que para el resto de los parámetros seminales (sólo aportaron datos 2 centros). La ventaja de tener estandarizados los protocolos de trabajo es que se ha minimizado el error analítico y los valores presentados se consideran representativos de las características seminales de un varón fértil.
NUEVOS VALORES DE REFERENCIA Y DIAGNÓSTICOS
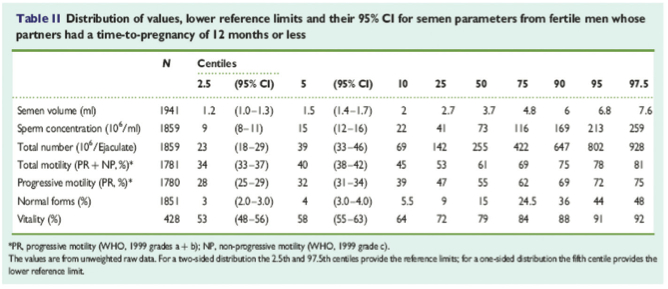
En esta edición se revisan y establecen los nuevos valores de referencia con los que debemos trabajar actualmente, que se encuentran recogidos en el artículo (de acceso libre) publicado en Mayo de 2010 en la revista internacional Human Reproduction Update (Cooper et al., 2010). En la tabla II, obtenida de este artículo, se recogen los valores de referencia establecidos con un 95% CI.
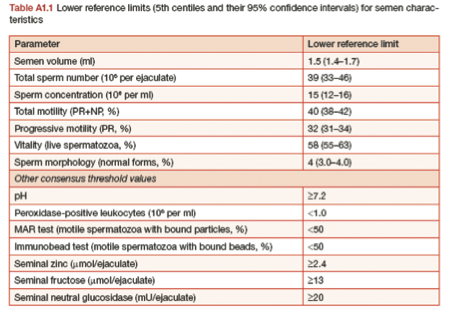
En la tabla A1.1 se recogen con mayor claridad los límites inferiores de referencia del quinto percentil de los valores en una población de referencia de varones fértiles (Cooper et al., 2010).
Todo esto va a su vez acompañado de algunos cambios en cuanto al diagnóstico de las muestras, de modo que aunque se mantiene la nomenclatura, se han producido algunas modificaciones:
TERATOZOOSPERMIA: Formas normales por criterio estricto (Tygerberg) < 4 %
ASTENOZOOSPERMIA: Móviles progresivos < 32 % (no se tiene en cuenta el total de móviles (% PR+NP) aunque esté por debajo del valor de referencia).
OLIGOZOOSPERMIA: Número total de espermatozoides < 39 millones. La OMS prefiere este parámetro antes que la concentración de la muestra, que era el parámetro de elección en el manual de 1999.
NECROZOOSPERMIA: Vitalidad < 58 % y porcentaje de espermatozoides inmóviles muy elevado. Este segundo criterio es arbitrario ya que la OMS no indica un número concreto, pero sí que haya también muchos inmóviles. De esta manera se evitan falsas necrozoospermias que alarmen injustificadamente.
CRIPTOZOOSPERMIA/AZOOSPERMIA: No hay cambios respecto a 1999.
PROBLEMAS Y MEJORAS DE LA NUEVA CLASIFICACIÓN OMS
Como en todo cambio o revisión, nos hemos encontrado con mejoras importantes pero también con algunos inconvenientes que tendremos que ir solucionando a medida que nos vayamos familiarizando con las modificaciones. Algunas de ellas han sido:
1. Cambio del concepto de oligozoospermia. La OMS de 1999 asignaba este diagnóstico a aquellas muestras con concentraciones por debajo del valor de referencia de dicho parámetro (20 millones/ml). Sin embargo, se ha hecho evidente que la propia concentración depende del volumen final de la muestra, por lo que en el Manual de 2010 se vincula preferentemente el diagnóstico de oligozoospermia al número total de espermatozoides, siempre que éste se encuentre por debajo de los 39 millones. Esto ha supuesto una mejora en la valoración de dicho parámetro.
2. Cambio en las categorías de movilidad espermática. Dado que la antigua categoría “a” del Manual de 1999 era difícil de justificar cuando el recuento de movilidad de una muestra se realizaba sin un sistema computerizado, y que realmente se observó que la información relevante de este parámetro se encontraba en el nº total de móviles progresivos (a+b), se han modificado las categorías de movilidad espermática que ahora recomiendan diferenciar los espermatozoides según 3 tipos: móviles progresivos (PM), móviles no progresivos (NP) e inmóviles (IM). Algunos centros consideran ventajosa la eliminación de dicha categoría.
3. Disminución del porcentaje de formas normales en la morfología. Es bien sabido que este parámetro es, no sólo el más subjetivo del análisis seminal sino el que mayor controversia ha suscitado a efectos de indicar uno u otro tipo de tratamiento en las clínicas de reproducción asistida. Se han publicado numerosos artículos en defensa o detrimento de la importancia de la morfología en muchos de los aspectos clave de estos tratamientos: tasa de gestación, tasa de implantación, éxito en la fecundación, etc. (Kruger et al., 1986; Kruger et al., 1988; Menkveld., 1990; Mortimer and Menkveld., 2001; Garrido et al., 2005). De cualquier modo, siempre ha sido objeto de debate, no sólo dentro del laboratorio de andrología y FIV, sino entre estos departamentos y los clínicos, pues, salvo casos extremos de morfologías con elevadas anomalías, se ha hecho difícil unificar los criterios de valoración morfológica de las muestras, incluso realizando los correspondientes controles de calidad tanto internos como externos.
4. La vitalidad espermática y la necrozoospermia. Parece que este parámetro, que además la OMS no incluye como “de obligatorio estudio” en el seminograma sino como algo muy recomendable, toma fuerza en esta nueva edición. Su vinculación con el porcentaje de espermatozoides inmóviles, sin que aparezca establecido un valor exacto a partir del cual diagnosticar una necrozoospermia, hace que sea fijado de manera individualizada por cada grupo de trabajo en función de la metodología empleada en el centro y la información que espera obtener con dicho diagnóstico. Es bien sabido que el estudio de la vitalidad resulta esencial en aquellos casos en que nos encontremos con un porcentaje de espermatozoides inmóviles por encima del 50%. No es lo mismo tener un porcentaje de espermatozoides inmóviles elevado pero que estén vivos tras test de tinción (que orientaría a posibles defectos estructurales de la cola; Chemes and Rawe, 2003), que un elevado porcentaje de inmóviles y además muertos (más relacionado con patología del epidídimo; Wilton et al, 1988; Correa-Pérez et al., 2004).
5. El hecho de que hayan desaparecido los “adjetivos” de leve, moderado y grave hace que los diagnósticos de las muestras con alteraciones queden incompletos y se obligue a tener en cuenta los valores numéricos de volumen, concentración, movilidad y morfología para poder hacernos una idea real del estado de la muestra. Ya que en función del número de millones de móviles progresivos determinaremos el tipo de tratamiento a realizar en una pareja, no será lo mismo un varón con alteraciones leves, que en algunos casos permitiría realizar técnicas de inseminación artificial, que otro varón con alteraciones graves que serían clara indicación de FIV o incluso ICSI.
6. Para finalizar, quizás el aspecto que más puede haber llamado la atención es la diferencia entre 1999 y 2010 de un varón con un seminograma con sus parámetros dentro de los valores de referencia en cada caso. Veamos las dos posibles situaciones.
Observamos que el cambio en cuanto al número de millones de móviles progresivos se ve reducido en un 64% (o un 40% si utilizamos el criterio de espermatozoides totales ahora recomendado), respecto al que se obtenía para un varón con una muestra de semen con los valores límite de referencia en 1999. El cambio en este aspecto podría resultar más problemático a nivel de consulta clínica, ya que varones ahora diagnosticados como normales en nuestros centros pueden recibir la recomendación de someterse a un ciclo de IAH o incluso de FIV. Evidentemente, cada centro deberá decidir si cambia sus criterios o bien si hace el esfuerzo de explicar a los pacientes que con los parámetros de referencia actualmente aceptados se asume la posibilidad de que, aun siendo normales, pueden indicar un determinado tratamiento de reproducción asistida.
DISCUSIÓN
Es importante en primer lugar recordar que el seminograma, por sí solo, no tiene capacidad diagnóstica (sensibilidad y especificidad) para indicar infertilidad masculina. Los diagnósticos del seminograma se entienden mejor como una simple descripción de la muestra para ver si se “asemejan” a los valores de una población fértil. Sí podrían tener utilidad diagnóstica clínica para detectar una criptozoospermia o azoospermia.
Por otra parte, no estaría de más reflejar que, para aquellos que nos dedicamos a la reproducción asistida, es conveniente diferenciar entre diagnóstico seminal de un varón y utilidad “real” de la muestra en un tratamiento de infertilidad. Sabemos que la OMS establece claramente que estar por debajo de los valores de referencia o tener una muestra no “normozoospérmica” no indica infertilidad masculina, sino que ese parámetro seminal está por debajo del quinto percentil del valor de ese parámetro en una población de referencia de varones fértiles. En otras palabras, que ese valor está por debajo del 95% de los valores que presentaban estos varones fértiles. En teoría, por la forma en la que se han obtenido (estadística de los parámetros en unos 2000 varones fértiles), es posible que los valores de referencia vayan actualizándose a medida que se vayan ampliando los estudios poblacionales. Pero, aparte de su utilidad para el diagnóstico de la pareja infértil, el seminograma, junto al resto de pruebas y reconocimientos, es una herramienta útil para tomar decisiones terapéuticas. El objetivo principal es valorar si la muestra, una vez capacitada, permite obtener el mínimo de millones de móviles progresivos para realizar uno u otro tratamiento de reproducción (inseminación artificial: IAH, Fecundación in Vitro: FIV o Microinyección Intracitoplasmática: ICSI). Podemos pensar que para una FIV estándar los nuevos valores de referencia no deberían modificar los valores internos que cada laboratorio establece según su protocolo de inseminación, sin embargo deberemos tener cuidado con muestras normozoospérmicas con valores en los límites inferiores de los diferentes parámetros, como ya hemos visto. Por su parte, la morfología sigue siendo un parámetro de dudosa utilidad clínica para evaluar un seminograma o derivar un paciente directamente a FIV/ICSI, y debe ser considerado en su justa medida.
Referencias
Castilla JA, Alvarez C, Aguilar J, González- Varea C, Gonzalvo MC, Martínez L. Influence of analytical and biological variation on the clinical interpretation of seminal parameters. Hum Reprod 2006; 21:847-851.
Chemes HE and Rawe VY. Sperm pathology: a step beyond descriptive morphology. Origin, characterization and fertility potential of abnormal sperm phenotypes in infertile men. Hum Reprod Update 2003; 9:405-428.
Comhaire FH, Vermeulen L, Schoonjans F. Reassessment of the accuracy of traditional sperm characteristics and adenosine triphosphate (ATP) in estimating the fertilizing potential of human semen in vivo. Int J. Androl 1987; 10:653-662.
Cooper TG, Neuwinger J, Bahrs S, Nieschlag E. Internal quality control of semen analysis. Fertil Steril 1992; 58:172-178.
Cooper TG, Noonan E, von Eckardstein S, Auger J, Gordon Baker HW, Behre HM, et al. World Health Organization
reference values for human semen characteristics. Hum Reprod Update 2010; 16(3): 231-245.
Cooper TG, Yeung CH. Computer-aided evaluation of assessment of “grade a” spermatozoa by experienced technicians. Fertil Steril 2006; 85:220-224.
Correa-Pérez JR, Fernández-Pelegrina R, Aslanis P, Zavos PM. Clinical management of men producing ejaculates characterized by high levels of dead sperm and altered seminal plasma factors consistent with epididymal necrospermia. Fert Steril 2004; 81(4): 114 8 -115 0 .
Dunphy BC, Kay R, Barratt CL, Cooke ID. Quality control during the conventional analysis of semen, an essential exercise. J Androl 1989; 10:378-385.
Garrido N, Meseguer M, Martínez- Conejero JA, Simón C, Pellicer A, Remohí J. Impacto de los criterios estrictos de morfología espermática en reproducción Asistida. Cuadernos de Medicina Reproductiva Vol.11 No 1. Año 2005.
Kruger TF, Menkveld R, Stander FS, Lombard CJ, Van der Merwe JP, van Zyl JA et al. Sperm morphologic features as a prognostic factor in vitro fertilization. Fertil Steril 1986; 46:1118-1123.
Kruger TF, Acosta AA, Simmons KF, Swanson RJ, Matta JF, Oehninger S. Predictive value of abnormal sperm morphology in vitro fertilization. Fertil Steril 1988; 49:112-17.
Menkveld R, Stander FSH, Kotze TJ, Kruger TF, van Zyl A. The evaluation of morphological characteristics of human spermatozoa according to stricter criteria. Hum Reprod 1990; 5(5):586-92.
Mortimer D, Menkveld R. Sperm morphology assessment. Historical perspectives and current opinions. J Androl 2001; 22:192-205.
Ombelet W, Bosmans E, Janssen M, Cox A, Vlasselaer J, Gyselaers W, et al. Semen parameters in a fertile versus subfertile population: a need for change in the interpretation of semen testing. Hum Reprod 1997a; 12:987-993.
Neuwinger J, Behre HM, Nieschlag E. External quality control in the andrology laboratory: an experimental multicenter trial. Fertil Steril 1990; 54:308-314.
Ombelet W, Wouters E, Bolees L, Cox A, Janssen M, Spiessens C, et al. Sperm morphology assessment: diagnostic
potential and comparative analysis of strict or WHO criteria in a fertile and subfertile population. Int J Androl 1997b; 20: 367-372.
Wilton LJ, Temple-Smith PD, Baker HWG, de Kretser DM. Human male infertility caused by degeneration and death of sperm in the epididymis. Fertil Steril 1988; 49:1052–1058.
World Health Organization. WHO Laboratory Manual for the Examination of
Human Semen and Sperm-cervical Mucus Interaction, 4th ed. Cambridge: Cambridge University Press, 1999a, 128 p.
World Health Organization. Sperm collection and processing methods, Cambridge: Cambridge University Press, 1999b.
World Health Organization. WHO manual for the standardized investigation and diagnosis of the infertile male, Cambridge: Cambridge University Press, 1999c