NUEVAS PERSPECTIVAS PARA EL EMBRIÓLOGO: PAPEL EN EL BANCO DE LÍNEAS CELULARES DE ANDALUCÍA (NODO CENTRAL BANCO NACIONAL DE LÍNEAS CELULARES)
José Luis Cortés*, Fernando Cobo, Carmen Cabrera, Angela Helen Barnie, Purificación Catalina, Ana Nieto, Rosa Montes, Alicia Barroso, Ángel Concha
Banco de Líneas Celulares de Andalucía (Nodo Central Banco Nacional de Líneas Celulares).* Banco de Líneas Celulares de Andalucía. Hospital Universitario Virgen de las Nieves. Email: josel.cortes.sspa@juntadeandalucia.es
Resumen: Un banco de líneas celulares troncales tiene como funciones la elaboración, el almacenamiento, la conservación y la gestión de líneas celulares de diverso tipo, de acuerdo con las normas y estándares que determina la legislación nacional e internacional. Dentro de los tipos de líneas celulares se encuentran las de origen embrionario, obtenidas a partir de la masa celular interna de blastocistos procedentes de preembriones sobrantes de ciclos de FIV, donde la figura de un embriólogo que manipule los preembriones es necesaria. Para poder definir aspectos en cuanto al perfil de este tipo de profesional, debemos buscar las similitudes con los centros de reproducción asistida. Mediante este trabajo se pretenden describir las funciones de un embriólogo dedicado a la derivación de líneas celulares embrionarias humanas dentro del Banco de Líneas Celulares de Andalucía.
Palabras clave: Banco de líneas celulares troncales, blastocisto, célula troncal embrionaria, embriólogo,
FIV, masa celular interna.
NEW PERSPECTIVES FOR THE EMBRYOLOGIST : ROLE IN THE ANDALUSIAN STEM CELL BANK (SPANISH CENTRAL NODE)
Abstract: The functions of a stem cell bank are the elaboration, storage, conservation and management of all the cell line types, according to national and international regulations currently in force. One of these cell lines is the embryonic stem cell line, which is obtained from the inner cell mass of blastocysts of IVF spare embryos, where the figure of an embryologist who manipulates the embryos is necessary. To be able to define some aspects about the profile of this type of professional, we must look for the similarities with the Assisted Reproduction Centres. A description of the functions of the embryologist who derives human embryonic stem cell lines in the Andalusian Stem Cell Bank has been carried out.
Key words: Stem cell bank, blastocyst, embryonic stem cell, embryologist, IVF, inner cell mass.
INTRODUCCIÓN
La creación de bancos de líneas celulares troncales públicos es un hecho reciente en Europa (aproximadamente 5 años), siendo España pionera en este sentido, con la inauguración del Banco de Líneas Celulares de Andalucía (BLCA), en Granada, el 23 de Enero de 2004. Tanto la derogada reforma de la Ley 35/1988 (Ley 45/2003, de 21 de Noviembre), como la actual Ley 14/2006, de 26 de Mayo, sobre Técnicas de Reproducción Asistida, así como la Directiva Europea (EuropeanUnion, 2004), permiten a los bancos de líneas celulares españoles derivar líneas celulares embrionarias humanas (siglas inglesas hESCs human embryonic stem cells) a partir de preembriones sobrantes de ciclos de FIV, siempre bajo el consentimiento informado de los progenitores.
Algo novedoso en la Ley es la eliminación de las diferencias en la consideración de los preembriones crioconservados con anterioridad a la entrada en vigor de la Ley 45/2003, y los que pudieran generarse posteriormente, en cuanto a sus posibles destinos, siempre supeditados a la voluntad de los progenitores. Es decir, cualquier preembrión crioconservado, sea cual fuere su tiempo de crioconservación, podría ser utilizado para fines de investigación siempre y cuando los progenitores firmen el consentimiento y estén asociados a un proyecto concreto que deberán autorizar posteriormente los Comités Éticos correspondientes.
PERFIL Y FUNCIONES DEL EMBRIÓLOGO
Aunque no es aún un título oficial,el embriólogo es aquel Licenciado en Ciencias Biomédicas (Medicina, Veterinaria, Farmacia, Biología o Química) con experiencia en Biología de la Reproducción. Según el R.D. 413/1996, de 1 de Marzo, para que un centro esté autorizado en la aplicación de las técnicas de reproducción asistida deberá estar dotado de una persona que cumpla los requisitos anteriores. Hasta ahora, la figura del embriólogo ha estado siempre relacionada con las clínicas de reproducción asistida, pero con el descubrimiento del poder regenerativo de las células troncales embrionarias, numerosos centros de investigación han iniciado proyectos de derivación de hESCs, donde la figura del embriólogo adquiere otra perspectiva.
Aún así, para poder definir aspectos referentes a la figura del embriólogo en un centro de investigación debemos buscar las “homologías” con el papel desempeñado en los centros de reproducción asistida.
ASEBIR ha publicado en el año 2006, dentro del programa de Cuadernos de Embriología Clínica, unas Recomendaciones sobre Recursos Humanos y Físicos para el Laboratorio de Reproducción Asistida Humana. En estas recomendaciones, el embriólogo sería el encargado de tomar las decisiones clínicas dentro del laboratorio de acuerdo con los protocolos establecidos, y realizaría la mayor parte de la labor asistencial del laboratorio de andrología y embriología.
Respecto a la formación del embriólogo, éste deberá haber obtenido el grado de Licenciado en Ciencias Biomédicas, como hemos expuesto anteriormente, poseer conocimientos de fisiología humana, endocrinología reproductiva, genética, técnicas de laboratorio de andrología y embriología, y conocimientos de cultivo celular. Además deberá poseer una experiencia de al menos 2 años y acreditar la realización de 100 ciclos de FIV con ICSI y 200 preparaciones de semen para inseminación artificial, supervisados por el coordinador del laboratorio en cuestión, o por otro embriólogo ya formado.
La ASMR 2004, en la guía para laboratorios de embriología y andrología, enumera los servicios que ofrecen en concreto los laboratorios de embriología clínica:
– Preparación de los medios de cultivo y control de calidad
– Identificación de ovocitos mediante examen del líquido folicular
– Evaluación de la madurez y calidad ovocitaria
– Preparación del esperma: recolección y análisis del semen, lavado y capacitación espermática
– Inseminación de los ovocitos
– Determinación de la fertilización y evaluación de la calidad del zigoto
– Cultivo embrionario y evolución de la calidad embrionaria
– Transferencia embrionaria
– Crioconservación, almacenaje y descongelación de esperma, ovocitos y embriones
– Micromanipulación de ovocitos humanos y/o embriones
Es obvio que en los centros de investigación en los que se deriven hESCs, la función del embriólogo será diferente a las descritas anteriormente, pero pensamos que la persona encargada de derivar estas líneas sí debe de haber adquirido anteriormente una amplia experiencia en este campo, lo que le otorgará propiedad a la hora de manipular los preembriones destinados a generar una línea celular.
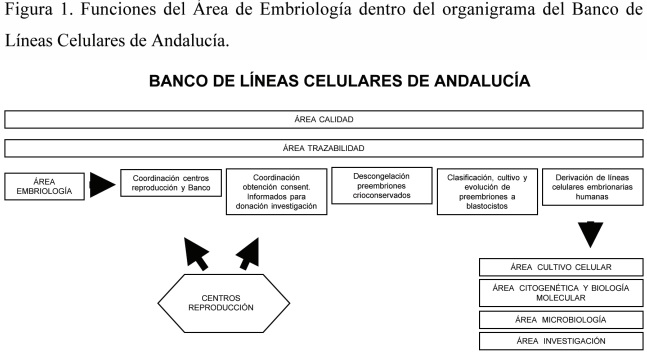
De esta manera, las funciones del profesional responsable del Área de Embriología dentro del BLCA son (Figura 1):
-Descongelación de preembriones crioconservados. Como los preembriones provienen de distintos centros, es competencia de esta área el conocimiento de todos los protocolos de congelación/descongelación utilizados para optimizar los resultados en cuanto a la obtención de hESCs.
-Clasificación de preembriones crioconservados descongelados, siguiendo criterios morfológicos (Calderón et al., 2002):
1.Ritmo de división de las blastómeras
2.Apariencia del citoplasma de las blastómeras
3.Contacto entre las blastómeras
4.Aspecto de la zona pelúcida
5.Fragmentación de las blastómeras
6.Multinucleación de las blastómeras
7.Evaluación de la calidad blastocitaria
Aunque algunos autores no relacionan la calidad embrionaria y blastocitaria con la tasa de obtención de líneas celulares (Mitalipova et al., 2004), desde nuestro centro pensamos que esta clasificación sí es importante a la hora de elegir el método de aislamiento de la masa celular interna (MCI) y posterior derivación de la línea celular (Ver abajo).
– Cultivo y evolución de los preembriones hasta estadio de blastocisto, donde se encuentra la MCI, compuesta por las células troncales, que darán lugar a las hESCs. Para evaluar la calidad blastocitaria atendemos al modelo propuesto por el Instituto Cornell (Veeck and Zaninovic, 2004), donde se valora el grado de expansión del blastocisto, así como el aspecto del trofoectodermo y la MCI, quedando establecidas tres categorías:
a.Blastocistos de buena calidad con una MCI bastante distinguible y con tamaño adecuado.
b.Blastocistos con una pequeña pero distinguible MCI.
c.Blastocistos de mala calidad con una MCI poco definida.
– Derivación de hESCs. Existen varios métodos que consisten en el aislamiento de la MCI y la eliminación de las células del trofoectodermo de los blastocistos. En nuestro centro hemos experimentado dos métodos para realizar el aislamiento de la MCI dependiendo de la calidad blastocitaria. Por un lado, un método mecánico, bien por micromanipulación o por empleo del disector láser, cuando los blastocistos son de buena calidad con una MCI bastante distinguible y con tamaño adecuado.
El empleo del láser es un nuevo método de aislamiento de la MCI probado en modelo murino por varios grupos, dando buenas tasas de derivación de líneas celulares embrionarias murinas (mESCs) (Tanaka et al., 2006; Cortés et al., 2006). Consiste en ir aplicando el láser a las células del trofoectodermo destruyéndolas, siendo solamente las células de la MCI las que se adhieren a la superficie de cultivo elegida (Fibroblastos murinos y humanos, MatrigelTM).
Para los blastocistos con una pequeña o nada visible MCI, utilizamos el método de cultivo directo del blastocisto sobre la superficie de cultivo elegida (Kim et al., 2005). Así, tanto las células del trofoectodermo, como las de la MCI se adhieren a dicha superficie. Pasados unos días, los dos tipos celulares sufren un crecimiento, y mecánicamente se separa la MCI. Aparte existe otro método de aislamiento de la MCI mediante inmunocirugía (Solter and Knowles, 1975), pero que está en desuso debido a que los medios utilizados contienen productos de origen animal, con el riesgo de contaminación cruzada.
– Coordinador entre los centros de reproducción y el banco para la perfecta interlocución en la donación de preembriones para fines científicos.
– Coordinador de la labor de obtención de los consentimientos informados. La Guía para la Investigación y Terapia con Células Troncales propuesta por la Indian Council of Medical Research (ICMR-DBT, 2006) expone que el profesional que realice el tratamiento de fertilidad y el investigador que derive la línea celular o que trabaje con ellas no sean la misma persona. Además explica que la decisión sobre el destino de los preembriones debe estar libre de la influencia de los investigadores que podrían alentar a los progenitores hacia su uso con fines de investigación.
En cambio, nosotros pensamos que el embriólogo del banco de células troncales sí debe ser parte activa en el proceso de entrevista, explicación y firma del consentimiento informado por parte de la pareja, o la mujer en su caso, estando disponible para realizar las entrevistas cuando sea necesario, ya que es experto en cuanto a cualquiera de los destinos propuestos por la Ley española (Ley 14/2006).
El BLCA es un centro multidisciplinario donde varias áreas interaccionan para una adecuada coordinación, con el objetivo de elaborar, almacenar, conservar y gestionar todos los tipos de líneas celulares, de acuerdo a las actuales normativas nacionales e internacionales. Estas áreas o secciones son las siguientes (Figura 1): Área de calidad; área de trazabilidad; área de embriología; área de cultivo celular; área de citogenética y biología molecular; área de microbiología y área de investigación.
CONCLUSIÓN
En el BLCA pensamos que existe una nueva figura de embriólogo investigador especializado en la manipulación de preembriones humanos destinados a generar nuevas hESCs. Este embriólogo debe haber acreditado experiencia previa en embriología clínica, y debe de estar en contacto con las clínicas de reproducción para la perfecta coordinación en la donación de preembriones con fines de investigación. Además, el área de embriología al que estará integrado el embriólogo formará parte del Banco de Células Troncales, con un stock propio de líneas celulares embrionarias, para su distribución a centros de investigación que las puedan utilizar para investigación básica y futuras aplicaciones clínicas.
AGRADECIMIENTO
Al Dr. José Antonio Castilla por su asesoramiento en la elaboración de este artículo
Referencias
ASEBIR, Recomendaciones sobre recursos humanos y físicos para el laboratorio de reproducción. Cuadernos de Embriología Clínica. Ed. Asociación para el Estudio de la Biología de la Reproducción, 2006.
ASRM. American Society for Reproductive Medicine. Reviewed guidelines for human embryology and andrology laboratories. 2004. www.asrm.org.
Calderón G, Prados N, Caligara C,Mantuana E, Navarro J, Pellicer A,Remohí J. Calidad embrionaria.Indicadores predictivos de vitalidad.En: Remohí J, Pellicer A, Simón C,Navarro J, editors. Reproducción Humana. 2º ed. Madrid: McGraw-HillInteramericana de España; 2002. p.463-468.
Cortés JL, Cobo F, Catalina P, Cabrera CM, Nieto A, Montes RM, Sánchez L, et al. Comparación de dos métodos de aislamiento de la masa celular interna en blastocistos de ratón para obtención de células troncales embrionarias: cultivo directo vs. láser. IX Congreso de la Asociación Española de Bancos de Tejidos; 2006 May 17-19; Oviedo, España. P. 73-4.
European Union 2004. Directive 2004/23/EC of the European Parliament and of the Council of 31 March 2004 on setting standards of quality and safety for the donation, procurement, testing, processing, preservation, storage, and distribution of human tissues and cells. Official Journal of the European Union, L102/48.
ICMR-DBT. Indian Council of Medical Research. Guidelines for Stem Cell Research and Therapy. 2006. www.icmr.nic.in.
Kim HS, Oh SK, Park YB, Anh HJ, Sung KC, Kang MJ, et al. Methods for derivation of human embryonic stem cells. Stem Cells 2005;23:1228-1233.
Ley 45/2003, de 21 de noviembre, por la que se modifica la Ley 35/1988, de 22 de noviembre, sobre Técnicas de Reproducción Asistida. BOE núm 280:41458-41463.
Ley 14/2006, de 26 de mayo, sobre Técnicas de Reproducción Humana Asistida.BOE núm 126: 19947-19956.
Mitalipova M, Calhoum J, Shin S, Wininger D, Schulz T, Noggle S, et al. Human Embryonic Stem Cell Lines derived from discarded embryos.
Stem Cells 2003;21:521-526.Real Decreto 413/1996, de 1 de marzo, por el que se establecen los requisitos técnicos y funcionales precisos para la autorización y homologación de los centros y servicios sanitarios relacionados con las técnicas de reproducción humana asistida. BOE núm 72: 11256-11260.
Solter D, Knowles BB . Immunosurgery of mouse blastocysts. Proc Natl Acad Sci USA 1975;72:5099-5102.
Tanaka N, Takeuchi T, Neri QV, Sills ES, Palermo GD. Laser-assisted blastocyst dissection and subsequent cultivation of embryonic stem cells in a serum/cell free culture system: applications and preliminary results in a murine model. J Transl Med. 2006. In press DOI:10.1186/1479-5876-4-20.
Veeck, LL, Zaninovic N. Human blastocyst in vitro. En Veeck LL, Zaninovic N, editors. An atlas of human blastocysts. New York:The Parthenon Publishing Group; 2003. p. 99-137.
Figura 1. Funciones del Área de Embriología dentro del organigrama del Banco de Líneas Celulares de Andalucía.