¿PUEDE LA ALTA MAGNIFICACIÓN SELECCIONAR ESPERMATOZOIDES GENÉTICAMENTE NORMALES?
Mónica Dorado Silva2, María Hebles Duvisón1, Beatriz Migueles Pastor2, Mercedes González Martínez2, Laura Aguilera Duvisón2, Pascual Sánchez Martín1,Fernando Sánchez Martín1
1 Clínica Ginemed, Sevilla
2Fundación Ginemed, Sevilla
e-mail: mdorado@ginemed.es
Fecha recepción: 3 Febrero 2012 Fecha aceptación: 19 Octubre 2012
La selección de espermatozoides en un microscopio convencional para microinyección intracitoplasmática (ICSI) está basada en la valoración morfológica del espermatozoide a 400 aumentos ópticos. El estudio espermático, debido al reducido tamaño de dichos gametos, queda muy limitado, pudiendo seleccionar espermatozoides que parecen tener buena morfología con otro tipo de alteraciones. El microscopio de alta magnificación permite observarlos y seleccionarlos a 1600 aumentos ópticos, consiguiendo de esta manera estudiarlos más profundamente, pudiendo descartar aquellos con anomalías no detectables a menos aumentos. Habitualmente las muestras de los pacientes son estudiadas a partir de una parte de la misma, extrapolando así el resultado al resto de espermatozoides no estudiados y considerando que se comportarán de igual manera.
La alta magnificación nos permite, entre otras cosas, hacer un estudio morfológico y seleccionar espermatozoides, ya sea para realizar la microinyección o para realizar pruebas adicionales.
El objetivo de nuestro estudio fue evaluar la eficacia de la alta magnificación para seleccionar espermatozoides genéticamente normales. Rev Asoc Est Biol Rep 2012; 17(2): 18-21.
INTRODUCCIÓN
La selección de espermatozoides en un microscopio convencional para microinyección intracitoplasmática (ICSI) está basada en la valoración morfológica del espermatozoide a 400 aumentos ópticos. Esto nos permite detectar alteraciones severas en los espermatozoides reconocidas en el análisis convencional del semen (de Almeida Ferreira Braga et al., 2011). No obstante, esta técnica presenta limitaciones porque solo permite observar grandes alteraciones pasando desapercibidas las de menor escala (Berkovitz et al,, 1999).
La imagen que obtenemos de los espermatozoides a alta magnificación permite observar anomalías estructurales indetectables a los aumentos convencionales (Bartoov, et. al, 2001), lo que permite seleccionar espermatozoides con mejor morfología. Es por ello por lo que algunos autores han demostrado que la selección de espermatozoides con microscopio de alta magnificación (1600 aumentos ópticos) mejora los resultados de la ICSI, sobre todo en aquellos casos en los que existe daño testicular (Garolla et al., 2008).
Habitualmente las muestras de los pacientes son estudiadas a partir de una parte de la muestra extrapolando así el resultado al resto de espermatozoides no estudiados y considerando que se comportarán de igual manera. De esta manera, si queríamos observar la morfología y porcentaje de aneuploidías que presentaba una muestra, se estudiaban ambos parámetros por separado. La alta magnificación nos permite, entre otras cosas, hacer un estudio morfológico a 6000x y seleccionar a su vez los espermatozoides que queramos, ya sea para hacer pruebas adicionales, por ejemplo estudio de aneuploidías, como para microinyectar con los de mejor morfología.
El objetivo de nuestro estudio fue evaluar la eficacia de la alta magnificación para seleccionar espermatozoides genéticamente normales a partir de la morfología observada a dichos aumentos
MATERIALES Y MÉTODOS
PREPARACIÓN DE LA MUESTRA
Para el presente estudio se utilizaron muestras seminales de 10 pacientes que acudieron a la Clínica en los últimos 6 meses del año 2010. De cada muestra se seleccionaron espermatozoides de los distintos grupos a estudiar. Como grupo control se utilizaron los espermatozoides morfológicamente normales de un donante.
Las muestras de semen usadas para la selección se prepararon por gradiente de densidad en capas de 0,3 a 1 mL de 40%yde0,3a1mLde80%deSperm Grad (Vitrolife ®) y Ham F-10 (Gibco) con gentamicina. La centrifugación se llevó a cabo a 300 g por 20 minutos seguida de un lavado a 400g por 10 minutos en medio tamponado: Quinn ́s Advantage Medium with HEPES de SAGE (HTF).
Los espermatozoides fueron depositados en una placa de microinyección específica (WillCo-Dish ®) para el microscopio de alta magnificación en gotas de Polivinil Pirrolidona (PVP, 7% Solution, SAGE). Tras la selección de los mismos, fueron depositados en gotas de medio tamponado HTF.
SELECCIÓN DE ESPERMATOZOIDES
Los espermatozoides fueron observados y captados uno a uno con el sistema de micromanipulación CellTram Oil, eppendorf acoplado a un microscopio de alta magnificación, LEICA CTR 6000 y depositados en un portaobjeto para su posterior análisis en cuatro grupos: grupo 1 (espermatozoides con cabezas grandes), grupo 2 (espermatozoides con cabezas elongadas), grupo 3 (espermatozoides con cabezas normales y grandes vacuolas) y grupo control (espermatozoides con cabeza normal sin vacuolas).
Para cada grupo se seleccionaron un total de 15 espermatozoides de los pacientes. Para el grupo control también se seleccionaron 15 espermatozoides.
FIJACIÓN DE LOS ESPERMATOZOIDES
Cada espermatozoide fue colocado en una parte específica del portaobjeto en 1μl de HTF y fijado con Carnoy posteriormente. El proceso se repitió para cada uno de los espermatozoides seleccionados obteniendo poblaciones de espermatozoides para cada grupo estudio.
PREPARACIÓN DE LOS ESPERMATOZOIDES PARA FISH
Antes de la hibridación los portaobjetos con los espermatozoides fijados eran lavados en 2X citrato sódico salino (SSC) durante 5 minutos, deshidratados en etanol (70/90/100%) y descondensación con ditiotreitol (DTT) durante 30 minutos a 37ºC.
HIBRIDACIÓN IN SITU FLUORESCENTE (FISH)
Se utilizaron las sondas comerciales del kit AneuvysionTM (Vysis) con las pruebas específicas para el cromosoma 18 (CEP 18 spectrumAquaTM 18p11- 1-q11.1), para el cromosoma X (CEP X spectrumGreenTM Xp11-1-q11.1) y para el cromosoma Y (CEP Y SpectrumOrangeTM Yp11.1-q11.1) para detectar el número de copias que existen para cada uno de los cromosomas.
La desnaturalización se realizó a 74oC durante 4 minutos y las sondas se dejaron al menos 16 horas a 37oC. Después de la hibridación los portas fueron lavados en 0.4x SSC, 0.3% de Nonidet P40 (NP40) a 71oC durante 2 minutos, seguido de 10 segundos en 2.0x SSC 0.1% NP40 a temperatura ambiente. Una vez secos eran cubiertos con 4’,6-Diamidino-2- fenilindol diclorhidrato (DAPI, Sigma) (Petit et al., 2005).
ANÁLISIS DE LOS DATOS
El estudio estadístico se realizó aplicando la prueba no paramétrica Kruskal-Wallis, con el programa estadístico SPSS v.17.
RESULTADOS
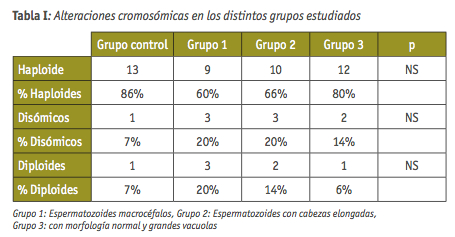
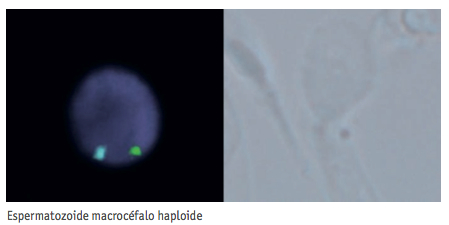
El FISH de espermatozoides realizado reveló la presencia de alteraciones en todos los grupos estudiados (Tabla I). En el grupo de espermatozoides con cabeza grande encontramos mayor porcentaje de espermatozoides con carga genética diploide que en los otros grupos, aunque también observamos la presencia de espermatozoides con disomías y con carga genética normal. El grupo de espermatozoides con cabezas elongadas mostraron espermatozoides con disomías en un número superior al que presentaba el grupo control, no encontrando diferencias significativas entre ambos grupos.
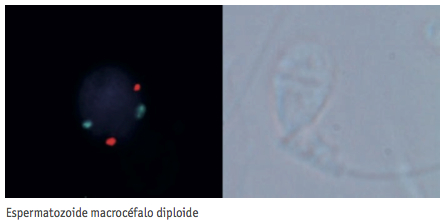
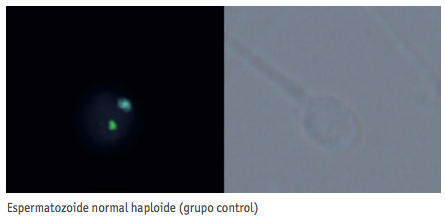
En los grupos de espermatozoides morfológicamente normales, tanto en el grupo control como en el que portaban vacuolas, el número de alteraciones genéticas era menor que en los otros grupos, no obteniendo tampoco diferencias significativas. En la figura 1 se muestran algunos ejemplos de espermatozoides con estas características.
DISCUSIÓN
El presente estudio reveló la existencia de alteraciones genéticas en todos los grupos estudiados. Devillard (2002) observó que los espermatozoides con cabezas grandes presentan un porcentaje mayor de alteraciones genéticas que aquellos que presentan un tamaño menor, hecho que concuerda con nuestros resultados. Prinsant (2007) en su estudio con pacientes que presentaban un porcentaje alto de espermatozoides con cabezas elongadas, realizaron un análisis estructural y genético, observando mayor número de alteraciones en el grupo de cabezas elongadas comparado con el grupo control.
En nuestro grupo control, espermatozoides de donante con cabezas normales, encontramos mayoritariamente carga genética normal para los cromosomas estudiados. Con respecto al grupo de cabezas normales pero con vacuolas, principalmente presentaron una dotación normal aunque el porcentaje de aneuploidías era superior al del grupo control.
Garolla et al. (2008) realizaron un estudio completo de espermatozoides que incluyó función mitocondrial, integridad del DNA espermático, fragmentación y aneuploidías. Encontraron mayor daño en muestras con daño testicular que en el grupo control o incluso aquellos que presentaban obstrucción parcial. Con respecto a las vacuolas, ellos encontraron aneuploidías en esos espermatozoides a pesar de tener cabeza normal, no observándolas en el grupo control con cabeza normal sin vacuolas.
De Almeida Ferreira Braga et al. (2011), encontraron una relación entre la fragmentación del DNA y la presencia de vacuolas, pero no encontraron correlación entre aneuploidías y alta magnificación.
Dado que nuestro estudio mostró presencia de alteraciones en todos los grupos estudiados, podemos pensar que el tamaño y la forma de la cabeza no son condición suficiente para asegurar la carga genética del espermatozoide, y por tanto la alta magnificación no nos sería útil para asegurarnos espermatozoides genéticamente normales. A pesar de ello, esta herramienta nos permitió seleccionar distintos tipos que mostraron diferencias entre ellos aunque no llegaron a ser significativas. No obstante sería necesario aumentar el tamaño muestral y estudiar cada grupo más ampliamente.
Referencias
Bartoov B, Berkovitz A, Eltes F. Selection of spermatozoa with normal nuclei to improve the pregnancy rate with intracytoplasmic sperm injection. N Engl J Med 2001;345(14):1067-1068.
Berkovitz A, Eltes F, Soffer Y, et al. ART success and in vivo sperm cell selection depend on the ultramorphological status of spermatozoa. Andrologia 1999;31(1):1-8.
De Almeida Ferreira Braga DP, Setti AS, Figueira RC, Nichi M, Martinhago CD, Iaconelli A Jr, Borges E Jr. Sperm organelle morphologic abnormalities: contributing factors and effects on intracytoplasmic sperm injection cycles outcomes. Urology 2011,78(4) :786-791.
Devillard F, Metzler-Guillemain C, Pellitier R, DeRobertis C, Hennebicq S, Guichaoaua M, et al. Polyploidy in large-headed sperm: FISH study of three cases. Hum Reprod 2002;17:1292-1298.
Garolla A, Fortini D, Menegazzo M, de Toni L, Nicoletti V, Moretti A, et al. High-power microscopy for selecting spermatozoa for ICSI by physiological status. RBM Online 2008;17:610 -616.
Petit FM, Frydman N, Benkhalifa M, Le Du A, Aboura A, Fanchin R, Frydman R, Tachdjian G. Could Sperm Aneuploidy Rate DeterminationBeUsedasapredictivetest before Intracytoplasmic Sperm Injection? Journal of Andrology 2005; 26 (2) :235-241.
Prisant N, Escalier D, Soufir J-C, Morillon M, Schoevaert D, Misrahi M, et al. Ultrastructural nuclear defects and increased chromosome aneuploidies in spermatozoa with elongated heads. Hum Reprod 2007; 22:1052-1059.