CRITERIOS DE VALORACIÓN MORFOLÓGICOS DE OOCITOS, PREEMBRIONES TEMPRANOS Y BLASTOCISTOS HUMANOS PROPUESTOS POR ASEBIR
José Luis Cortés*, Gertrudis Ligero, Laura Sánchez, Ana Nieto, Clara Bueno, Rosa Montes, Pablo Menéndez. Banco Andaluz de Células Madre. Centro de Investigación Biomédica. Universidad de Granada. Campus de la Salud. Granada. *Correspondencia: josel.cortes.sspa@juntadeandalucia.es
Resumen: ASEBIR ha publicado en sus Cuadernos de Embriología Clínica los Criterios de Valoración Morfológicos de Oocitos, Preembriones tempranos y Blastocistos Humanos, buscando poder consensuar los criterios de calidad entre todas las clínicas de reproducción asistida españolas. Sin embargo, estos criterios no sólo deben ser útiles para los embriólogos clínicos, sino que pueden servir a los embriólogos pertenecientes a centros de investigación como ayuda para facilitar la derivación de líneas celulares embrionarias humanas así como para estudios moleculares y genéticos básicos de embriología humana. El objetivo de este trabajo es mostrar si los criterios publicados por ASEBIR son extrapolables a preembriones congelados donados a investigación con células madre, utilizando para ello los preembriones autorizados para un proyecto de investigación del Banco Andaluz de Células Madre.
Palabras clave: Calidad blastocitaria, Calidad embrionaria, célula madre embrionaria humana, masa celular interna, preembrión congelado.
Morphological Assessment of Human Oocytes, early Embryos and Blastocysts proposed by ASEBIR
Summary: ASEBIR proposed in its Clinical Embryology Notebooks the Morphological Assessment for Human Oocytes, early Embryos and Blastocysts, aiming at reaching an agreement on the quality criteria between all Spanish assisted reproduction clinics. Nevertheless, these proposed criteria not only will be useful to clinical embryologists, but can also be useful to embryologists moving into basic research to help facilitate the derivation of human embryonic stem cells and further basic molecular and genetic studies on human embryo development. The aim of this work is to discuss if the criteria published by ASEBIR are useful and can be extrapolated to cryopreserved embryos which are donated to stem cell research using the authorized embryos for an ethically and scientifically approved research project to be carried out at the Andalusian Stem Cell Bank.
Key words: Blastocyst quality, embryonic quality, human embryonic stem cell, inner cell mass, cryopreserved embryo
INTRODUCCIÓN
Los estudios sobre células madre constituyen en la actualidad uno de los campos con más expectativas de la biomedicina. Cuando en noviembre de 1998, el grupo estadounidense liderado por James Thomson publicó los datos sobre la derivación de una línea de células madre embrionarias humana (hESCs, siglas inglesas de human embryonic stem cells) a partir de un blastocisto en fase de preimplantación, se abrió una nueva puerta de esperanza para la curación de enfermedades hasta ahora incurables (Thomson y cols., 1998). Estas células suponen una herramienta de enorme valor para el “screening” de nuevos fármacos, así como un modelo para estudiar la etiología de las enfermedades que tienen su origen durante la etapa embrionaria, o como fuente futura de células en medicina regenerativa (Menendez et al., 2006).
La legislación en España respecto al uso de preembriones humanos sobrantes de ciclos de fecundación “in vitro” (FIV) está actualmente regulada por la Ley 14/2006, sobre técnicas de reproducción asistida, por el Real Decreto 1301/2006, sobre células y tejidos humanos, y por la Ley 14/2007, sobre investigación biomédica. En nuestra interpretación de estas leyes, la pareja sometida a un ciclo FIV puede dar un destino final a aquellos preembriones sobrantes que se encuentren crioconservados en nitrógeno líquido, independientemente del tiempo de congelación, siempre bajo consentimiento informado de la pareja. Los diferentes destinos posibles que pueden darse a los preembriones sobrantes crioconservados son:
> Su utilización por la propia mujer o cónyuge.
> La donación con fines reproductivos.
> La donación con fines de investigación.
> El cese de su conservación sin otra utilización.
Respecto a la utilización de preembriones con fines de investigación, sólo se autorizará si se atiene a varios requisitos:
> Posesión del consentimiento informado.
> Que el preembrión no se haya desarrollado in vitro más allá de 14 días después de la fecundación.
> Que la investigación se realice en centros autorizados.
> Que la investigación se realice en base a un proyecto debidamente presentado y autorizado por las autoridades competentes
> Que se especifiquen las posibles relaciones de interés entre centros.
Esta legislación deja a España en un término medio de permisividad, englobándola en el grupo de países donde está permitido investigar con preembriones sobrantes de ciclos de FIV para derivar hESC (Canadá, Holanda, Australia, Suecia), lejos del grupo de países donde está prohibido utilizar preembriones para investigación con hESC (Irlanda, Austria, Noruega), aunque un peldaño por debajo del grupo de países donde se pueden generar preembriones con fines únicos de investigación (Reino Unido, Bélgica, Israel, Singapur).
Para la evaluación de la calidad embrionaria de aquellos preembriones crioconservados que han sido donados a investigación, el Centro de Reproducción Asistida facilita al Banco Andaluz de Células Madre (BACM) toda la información referente a cada preembrión; desde la calidad que poseía previo a la congelación, el método de congelación utilizado, así como el tiempo que llevan los preembriones congelados, entre otros datos.
ASEBIR, dentro de la Colección de Cuadernos de Embriología Clínica, ha publicado los Criterios de Valoración Morfológicos de Oocitos, Embriones Tempranos y Blastocistos Humanos. Esta propuesta ha sido diseñada debido a la falta de consenso en este aspecto clave de la embriología clínica y que conlleva problemas tan comunes como la imposibilidad de generar estudios multicéntricos con valoraciones de calidad embrionaria común, de interpretar informes clínicos de laboratorios ajenos, o de comparar datos bibliográficos.
Desde el BACM hemos querido sumarnos a esta propuesta, para ver si estos criterios de valoración morfológicos son extrapolables a los preembriones crioconservados que son donados a nuestro proyecto de investigación para derivación de hESC.
MATERIAL Y MÉTODOS
Para poder disponer de material biológico para nuestras investigaciones, el BACM ha realizado durante los años 2006 y 2007 una campaña de recuperación de preembriones sobrantes, tanto en hospitales públicos andaluces como en clínicas privadas (Cortes y cols., 2007). Estos preembriones han pasado los Comités necesarios (Comité de Investigación con Preembriones Humanos de Andalucía y la Comisión de Seguimiento y Control de la Donación del Instituto de Salud Carlos III), que han dado la autorización pertinente para su uso en investigación a nuestro proyecto de investigación.
A nivel de infraestructura y organización del espacio, disponemos de un completo laboratorio de embriología, dentro de salas GMP (siglas inglesas de Good Manufacturing Practice), con equipamiento y personal cualificado para realizar la manipulación de estos preembriones y su posterior derivación a hESCs (Cortes y cols., 2006a, b).
Para la configuración del laboratorio de embriología evaluamos las guías propuestas por distintas asociaciones de reproducción asistida, observando que el único enfoque fue el reproductivo, haciéndose necesaria una actualización de dichas guías, debido a la existencia de laboratorios de embriología que no se dedican a realizar técnicas de reproducción (Cortes y cols., 2006b).
Los Centros de Reproducción Asistida de donde proceden los preembriones donados a investigación han facilitado al BACM toda la información referente a cada preembrión, desde la calidad que poseía previo a la congelación, el método de congelación utilizado, así como el tiempo que llevan los preembriones congelados, entre otros datos. Los preembriones fueron congelados en estadio de división temprana (Día +2/+3), y fueron clasificados cualitativamente por las Clínicas de Reproducción de origen siguiendo los sistemas de evaluación de la calidad embrionaria tradicionales (Calderón y cols., 2002). Para los preembriones que llegaron al estadio de blastocisto utilizamos como criterio de clasificación tradicional el propuesto por Gardner (Gardner y cols., 1998).
Según los criterios propuestos por ASEBIR, la valoración morfológica en estos estadios ha constituido tradicionalmente la base de la determinación de la calidad embrionaria. Sin embargo, aunque hay cierto consenso entre la definición de un preembrión de buena o mala calidad, no existe consenso entre laboratorios cuando se trata de valorar preembriones de calidades intermedias. El objetivo de ASEBIR ha sido poder consensuar los criterios de calidad, creando una nueva tabla de clasificación embrionaria, cuando se trata del estadio de oocitos, preembriones tempranos, o cuando se trata de blastocistos. Nosotros nos vamos a centrar en los dos últimos estadios.
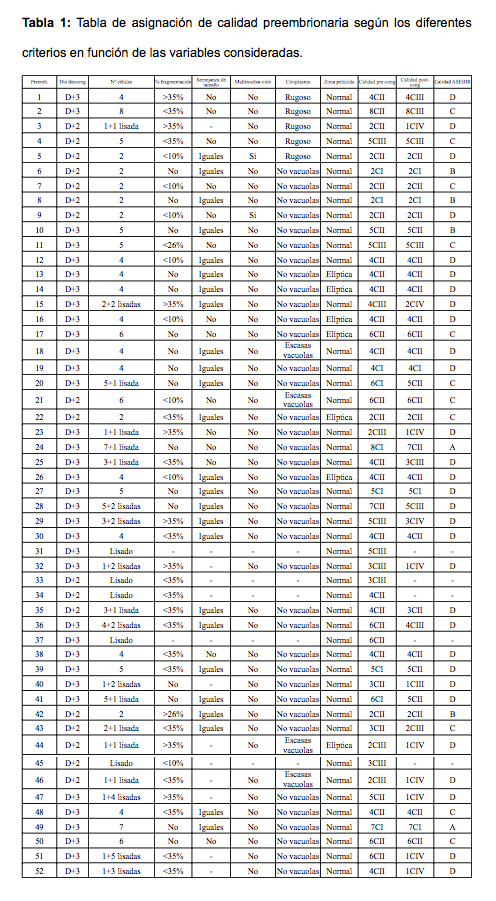
La calidad embrionaria fue evaluada por un embriólogo del BACM inmediatamente después del proceso de descongelación, y en los días sucesivos hasta su evolución a blastocisto, aunque sólo mostramos en este trabajo la situación inicial postdescongelación (Tabla 1) y la calidad de aquellos preembriones que llegaron al estadio de blastocisto (Tabla 2).
Una vez descongelados los preembriones fueron lavados en medio G-MOPS (Vitrolife, Suecia) y colocados en medio de cultivo (G-1 y G-2 V.5 plus, Vitrolife, Suecia). A continuación se evaluó la calidad embrionaria en base a los criterios de evaluación tradicionales y también en base a los nuevos criterios ASEBIR, y además se compararon con la calidad embrionaria precongelación, según los datos facilitados por los Centros de Reproducción de procedencia (Tabla 1).
Los 52 preembriones que hemos utilizado para este estudio fueron congelados mediante dos métodos distintos de crioconservación. Por una parte, se utilizó el protocolo de congelación denominado de congelación ultrarrápida (Trounson y cols., 1988), y que consiste en la inmersión directa de los preembriones, incluidos en dimetil sulfóxido (DMSO), en nitrógeno líquido. Por otra parte se utilizó el protocolo de congelación lenta (Freeze-kit 1, Vitrolife, Suecia), que consiste en el tratamiento de los preembriones con un crioprotector que ocupa el lugar del agua que hay en las células mediante procesos osmóticos, seguido de un programa de congelación llevado a cabo por un congelador programable (Nicool plus, Air Liquide,
España).
El objetivo de nuestro proyecto de investigación es poder derivar hESC a partir de estos preembriones. Esta derivación consiste en el desarrollo de los preembriones hasta estadio de blastocisto, la liberación de la zona pelucida mediante el uso de ácido Tyrode (Irvine Scientific, CA, USA), la posterior colocación del blastocisto desnudo sobre una superficie de células de soporte (feeders), y el posterior aislamiento mecánico de la masa celular interna (MCI), donde se encuentran las hESCs.
RESULTADOS
Día de desarrollo embrionario de los preembriones utilizados y métodos de congelación/descongelación utilizados
Para realizar nuestros experimentos hemos utilizado 52 preembriones que fueron congelados en estadio de división temprana (D+2 y D+3). Diecisiete preembriones fueron congelados en Día +2 (32,7%), mientras que 35 fueron congelados en Día +3 (67,3%). En todos los casos se utilizó para descongelar el protocolo de descongelación complementario al utilizado para la congelación.
Cinco preembriones (Preembriones 1-5) fueron congelados por el método de congelación ultrarrápida (9,6%). Los preembriones restantes (Preembriones 6-52) fueron congelados por el método de congelación lenta (90,4%).
Calidad embrionaria de los preembriones pre- y post-descongelación siguiendo los diferentes criterios de clasificación.
Para poder derivar nuevas hESC, partimos de 9 preembriones que poseían antes de la congelación calidad I (17,3%), 32 preembriones que poseían calidad II (61,5%) y 11 preembriones que poseían calidad III (21,2%). Tras el proceso de descongelación, nuestra evaluación con criterios tradicionales dio los siguientes resultados: 5 preembriones con calidad I (9,6%), 23 preembriones con calidad II (44,2%), 9 preembriones con calidad III (17,3%), 10 preembriones con calidad IV (19,3%), y tuvimos 5 preembriones que se lisaron por completo y que no pudieron ser evaluados (9,6%). Según los nuevos criterios propuestos por ASEBIR y tras la descongelación de los preembriones obtuvimos los siguientes resultados: 2 preembriones de categoría A (3,8%), 4 preembriones con categoría B (7,7%), 11 preembriones con categoría C (21,1%), y 30 preembriones con categoría D (57,8%) (Tabla 1). Queremos destacar que en 19 preembriones (36,5%) observamos la lisis de alguna blastómera que no comprometió la supervivencia de los preembriones, pero que se tuvo en cuenta a la hora de reclasificar su calidad.
Fase experimental de descongelación y establecimiento de hESCs: datos preliminares.
De los 52 preembriones descongelados, 12 preembriones llegaron al estadio de blastocisto (23,1%), siendo en todos los casos preembriones descongelados con el método de descongelación lenta y en día +3 de desarrollo. Estos blastocistos procedían de preembriones de categoría A en dos ocasiones (16,7%), de preembriones de categoría C en 3 ocasiones (25,0%) y de preembriones de categoría D en 7 ocasiones (58,3%). En ninguna ocasión el blastocisto se originó a partir de un preembrión de categoría B.
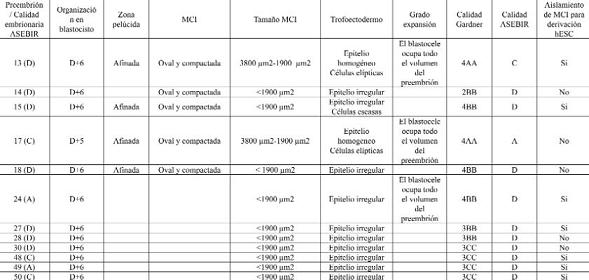
Respecto a la calidad blastocitaria evaluada con los criterios de Gardner, obtuvimos 2 blastocistos con calidad 4AA (16,7%), 2 blastocistos con calidad 4BB (16,7%), 3 blastocistos con calidad 3BB (25,0%), 4 blastocistos con calidad 3CC (33,3%), y un blastocisto con calidad 2BB (8,3%). Atendiendo a la nueva clasificación de ASEBIR obtuvimos un solo blastocisto con categoría A (8,3%), un solo blastocisto con categoría C (8,3%), y 10 blastocistos con categoría D (83,4%). Ninguno de los blastocistos se evaluó con categoría B (Tabla 2).
Los 12 blastocistos fueron liberados de la zona pelucida utilizando ácido Tyrode y puestos sobre “feeders” para proceder a la derivación de hESCs. En 7 de los blastocistos (58,3%) se pudo aislar la masa celular interna. En el momento de escribir este trabajo, pequeñas colonias con morfología similar a hESCs seguían en cultivo y desarrollo buscando el establecimiento de la línea celular, correspondiendo al preembrión número 24 y al preembrión número 27.
Tabla 2: tabla de asignación de calidad del blastocisto según los diferentes criterios en función de las variables consideradas.
DISCUSIÓN
En este estudio hemos intentado comparar la calidad embrionaria de los preembriones antes y después de la congelación, siguiendo los criterios tradicionales, con la clasificación que tendrían estos preembriones utilizando los nuevos criterios de ASEBIR, con el fin de observar si esta nueva clasificación es extrapolable a los criterios de calidad embrionaria que se deducen serían necesarios para derivar una línea de hESCs. Para poder realizar esta comparación hemos tenido que obviar y transformar algunos términos que sólo son aplicables al campo reproductivo:
i) Derivación de hESCs en vez de capacidad de implantación
ii) Día de descongelación en lugar de día de transferencia
Además, hemos observado que en los nuevos criterios de valoración de ASEBIR no se contempla información sobre los preembriones congelados, no atendiéndose por tanto a la posibilidad de que alguna blastómera resulte lisada durante el proceso de descongelación. Cuando este hecho ha ocurrido en nuestro laboratorio, lo hemos tenido en cuenta a la hora de determinar la calidad del preembrión (Tabla 1). De esta manera y según el sistema de graduación de ASEBIR, la categoría A sería para el preembrión de óptima calidad con máxima capacidad de derivar a hESCs, la categoría B de buena calidad con elevada capacidad de derivar a hESCs, la categoría C de calidad regular con una probabilidad de derivar a hESCs
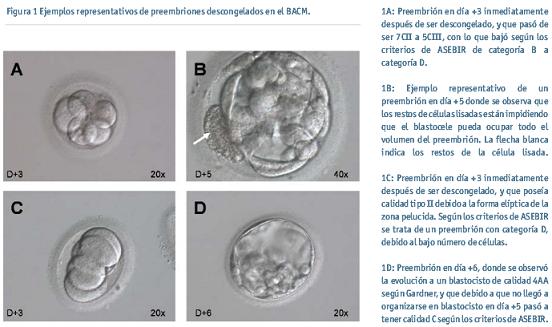
media/baja, y la categoría D para el preembrión de mala calidad con una probabilidad de derivar a hESCs baja/nula. Este hecho nos hace sospechar que algunos preembriones que hubieran podido tener categoría A o B previo a la congelación, pasaron a preembriones de categoría C o D al ser descongelados, como el preembrión número 28, que habiendo sufrido lisis de dos de sus blastómeras (5 morfológicamente normales+2 lisadas) (Figura 1A), con la consecuente bajada en el criterio de valoración ASEBIR de categoría B a categoría D (Tabla 1), llegó al estadio de blastocisto (Categoría ASEBIR D), aunque después no fuimos capaces de aislar la MCI (Tabla 2). Además, somos conscientes que la presencia de estos restos de lisis celular pueden dificultar, aún más que la presencia de fragmentos citoplasmáticos, la formación de blastocistos de buena calidad (Figura 1B).
Con respecto a los parámetros morfológicos a evaluar por ASEBIR en el estadio de D+2 y D+3, vimos concordancia entre los diferentes criterios de valoración en todas las variables consideradas, excepto en la que se refiere a número celular y ritmo de división. Aunque la hora de la congelación no es un dato que nos hayan facilitado los Centros de Reproducción, obviamos que estuvo en todos los casos dentro de los intervalos de observación recomendados por ASEBIR, siendo en D+2: 44-47 horas post-inseminación, y en D+3: 67-71 horas post-inseminación. En nuestra experiencia tuvimos el claro ejemplo del preembrión 27, que teniendo calidad 5CI por los criterios tradicionales, se clasificó con categoría D según ASEBIR debido a un ritmo de división algo más lento (Tabla 1), llegó al estadio de blastocisto, y tuvimos éxito en el aislamiento de la MCI para intentar la derivación de hESCs (Tabla 2).
Nos ocurrió lo mismo a la hora de comparar los distintos criterios de valoración de la calidad cuando observamos el estadio de blastocisto. Mientras que vimos concordancia a la hora de evaluar las variables consideradas por ASEBIR como el aspecto de la zona pelucida, aspecto y tamaño de la MCI y del trofoectodermo, y el grado de expansión, cuando evaluamos el día de organización del blastocisto pudimos comprobar que algún preembrión que alcanza una calidad blastocitaria óptima respecto a las demás variables, pasó a ser categoría C solamente porque se organizó en blastocisto en D+6, en lugar de en D+5. Esto le ha ocurrido en nuestro trabajo al preembrión 13 (Tabla 2). Teniendo en cuenta que procedía de un preembrión ya catalogado como categoría D cuando estaba en D+3, es lógico pensar que iba a llevar acumulado este retardo en su desarrollo (Figura 1C, D). Por tanto la variable de número celular y ritmo de división es para nosotros independiente de la calidad morfológica que se consiga, ya que al preembrión 13 también pudimos aislarle la MCI. Además, el hecho de que todos los preembriones que llegaron a blastocisto fueran congelados en día +3 corrobora los estudios reproductivos en los que mantener en cultivo los preembriones un día más antes de la crioconservación (Día+2 vs. Día+3) permite seleccionar mejor la calidad de estos (Sifer et al., 2006). Esto puede tener implicaciones importantes para la selección de preembriones congelados destinados a derivar hESCs.
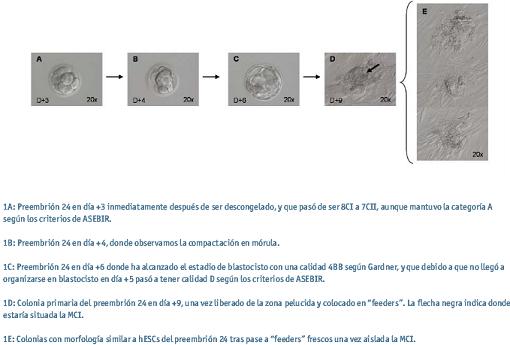
La tasa de éxito en la derivación de hESCs sigue siendo baja actualmente, necesitándose un gran número de preembriones para poder derivar un número bajo de líneas establecidas y caracterizadas, sobre todo cuando los preembriones a los que se puede optar son los sobrantes de las técnicas de reproducción asistida, y que, por tanto, no fueron prioritarios a la hora de realizar la transferencia. Este hecho ha dado lugar a que muchos grupos de investigación inmersos en la derivación de hESCs utilizando tanto preembriones frescos como congelados, comiencen a tener en cuenta la calidad embrionaria de estos preembriones (Zhang et al., 2006; Lerou et al., 2008). En nuestra experiencia, las colonias que tenemos actualmente han procedido de un preembrión de categoría A, y que evolucionó a un blastocisto de categoría D, en el caso del preembrión 24 (Figura 2), y de un preembrión de calidad D, que evolucionó a un blastocisto de categoría D, en el caso del preembrión 27 (Figura 3), lo que nos hace ver una vez más que el número celular y el ritmo de división en nuestra experiencia puede no ser un factor limitante sobre la posibilidad de éxito en derivación.
Figura 2. Evolución a blastocisto y aislamiento de la MCI del preembrión 24
Figura 3 Evolución a blastocisto y aislamiento de la MCI del preembrión 27
Desde el BACM opinamos que la propuesta de ASEBIR para estandarizar los criterios de valoración morfológicos de oocitos, embriones tempranos y blastocistos humanos es muy positiva y extrapolable en su mayor parte a la manipulación de estas células para propósitos diferentes de la reproducción, aunque creemos que es necesario publicar un anexo que se refiera concretamente a los preembriones congelados, y que no sea tan exigente con la variable de número de células y ritmo de división. Este anexo específico para estos preembriones sería útil tanto para el propósito de derivación de hESCs, donde la evolución de los preembriones al estadio de blastocisto es necesaria, como para los programas de criotransferencia que se realicen dentro de los Centros de Reproducción Asistida.
AGRADECIMIENTOS
Este trabajo ha sido financiado por la Consejería de Salud de la Junta de Andalucía (Proyecto 0030/2006 TC y MR). Queremos agradecer al Servicio Andaluz de Salud, a la Fundación Progreso y Salud, a ANACER y al Instituto de Salud Carlos III su continua colaboración.
Referencias
ASEBIR, II. Criterios de valoración morfológicos de oocitos, embriones tempranos y blastocistos humanos. Cuadernos de Embriología Clínica. 2007.
Calderón G, Prados N, Caligara C, Mantuana E, Navarro J, Pellicer A, Remohí J. Calidad embrionaria. Indicadores predictivos de vitalidad. En: Remohí J, Pellicer A, Simón C, Navarro J, editors. Reproducción Humana. 2º ed. Madrid: McGraw-Hill- Interamericana de España; 2002. p. 463- 468.
Cortes JL, Cobo F, Cabrera C, Barnie AH, Catalina P, Nieto A, Montes R, Barroso A, Concha A. Nuevas perspectivas para el embriólogo: papel en el Banco de Líneas Celulares de Andalucía (Nodo Central Banco Nacional de Líneas Celulares). Revista de la Asociación para el Estudio de la Biología de Reproducción (ASEBIR). Vol. 11, nº 2. p 11-14, Diciembre 2006.
Cortes JL, Cobo F, Barnie AH, Catalina P, Cabrera C, Nieto A, Montes R, Concha A. Role of the embryology laboratory in the human embryonic stem cell line derivation process. Cytotechnology 2006;52:1-11.
Cortes JL, Antiñolo G, Martinez L, Cobo F, Barnie A, Zapata A, Menendez P. Spanish Stem Cell Bank interviews examine the interest of couples in donating surplus human IVF embryos for stem cell research". Cell Stem Cell. 2007; 1:17-20.
Gardner DK, Vella P, Lane M, Wagley L, Schlenker T, Schoolcraft WB. Culture and transfer of human blastocyst increases implantation rates and reduces the need for multiple embryo transfers. Fertil Steril. 1998; 13:3434-3440.
Lerou PH, Yabuuchi A, Huo H, Takeuchi A, Shea J, Cimini T, Ince TA, Ginsburg E, Racowsky C, Daley GQ. Human embryonic stem cell derivation from poor-quality embryos. Nat Biotechnol. 2008; 26:212-214.
Ley 14/2006, de 26 de mayo, sobre Técnicas de Reproducción Humana Asistida. BOE núm 126: 19947-19956.
Ley 14/2007, de 3 de Julio, de investigación biomédica. BOE núm 159: 28826-28848.
Menendez P, Bueno C, Wang L. Human embryonic stem cells: a journey beyond cell replacement therapies. Cytotherapy 2006; 8:530-541.
Real Decreto 1301/2006, de 10 de noviembre, por el que se establecen las normas de calidad y seguridad para la donación, la obtención, la evaluación, el procesamiento, la preservación, el almacenamiento y la distribución de células y tejidos humanos y se aprueban las normas de coordinación y funcionamiento para su uso en humanos. BOE núm 270: 39475-39502
Sifer C, Sellami A, Poncelet C, Martin-Pont B, Porcher R, Hugues JN, Wolf JP. Day 3 compared with day 2 cryopreservation does not affect embryo survival but improves the outcome of frozen-thawed embryo transfers. Fertil Steril 2006; 86: 1537-1540.
Thomson JA, Itskovitz-Eldor J, Shapiro SS, Waknitz MA, Swiergiel JJ, Marshall VS, Jones JM. Embryonic stem cell lines derived from human blastocysts. Science 1998; 282:1145-1147.
Trounson A, Peura A, Freemann L, Kirby C. Ultrarapid freezing of early cleavage stage human embryos and eight-cell mouse embryos. Fertil Steril. 1988; 49:822-826. Zhang X, Stojkovic P, Przyborski S, Cooke M, Armstrong L, Lako M, Stojkovic M. Derivation of human embryonic stem cells from developing and arrested embryos. Stem Cells. 2006; 24:2669-2676.