ENFERMEDADES MITOCONDRIALES. FECUNDACIÓN IN VITRO TRIPARENTAL
Elisa Álvarez Sociasab. E-mail de contacto: elisaalvarez90@gmail.com
aEstudiante de Postgrado Oficial en Instituto Valenciano de Infertilidad (Plaza de la Policía Local, 3, 46015, Valencia) y b Embrióloga en Create Fertility (3-5 Pepys Road, SW20 8NJ, Londres)
La disfunción mitocondrial está relacionada con enfermedades, con infertilidad ligada a la edad y con repetidos ciclos fallidos de fecundación in vitro (FIV). Las terapias de remplazo mitocondrial en ovocitos o cigotos como son la transferencia pronuclear, la transferencia del huso meiótico materno, o la transferencia del corpúsculo polar podrían prevenir la transmisión de ADN mitocondrial (ADNmt) mutado a la segunda generación a través de la herencia materna, evitando así la transmisión de enfermedades ligadas a estas anomalías. Además, pueden ser de utilidad para la transferencia citoplasmática en pacientes de edad avanzada con repetidos ciclos fallidos al presentar un citoplasma con deficiencias y, que con ésta técnica se podrían beneficiar de una mayor tasa de embarazo después de someterse a un tratamiento de FIV. Aun así, estas técnicas englobadas en lo que se denomina FIV triparental, siguen ocasionando mucha controversia respecto a su eficacia y a sus efectos futuros sobre los recién nacidos y, es por esto que necesitan de una mayor investigación y de un mayor refuerzo por parte de comités éticos que las regulen y las legislen.
INTRODUCCIÓN
Mutaciones en el ADNmt o en genes nucleares que participan en la función mitocondrial son la causa de infertilidad y enfermedades neuromusculares y degenerativas, no sólo en los individuos, sino también en su descendencia (DiMauro and Davidzon, 2005). La prevalencia de padecer una enfermedad mitocondrial sintomática debido a la mutación del ADNmt es de 1:8000 (Scarpulla, 2008). Dado que la detección fiable y predecible de los trastornos mitocondriales en los embriones y ovocitos es inalcanzable en la actualidad, la sustitución parcial o completa de ADNmt mutado con el ADNmt de donante a través de manipulaciones de embriones ha supuesto un enfoque alternativo para abordar esta problemática. Los métodos que están potencialmente disponibles en la actualidad para lograr este objetivo son los que se engloban bajo el nombre de Fecundación in vitro triparental.
En contraste con el genoma nuclear, donde son habituales las familias de secuencias repetitivas, intrones y regiones intergénicas, el ADNmt de los mamíferos y otros vertebrados exhibe una sorprendente economía en la organización de su secuencia génica. El genoma mitocondrial de vertebrados se halla en forma de molécula circular cerrada de ~16.5 kb cuya capacidad de codificación de proteínas es exclusivamente destinada a la síntesis de 13 proteínas que funcionan como subunidades esenciales para los complejos respiratorios I, III, IV, V (Clayton, 2003).
El hecho de que el ADNmt sea un elemento extra cromosómico compartimentado contribuye a un tipo de herencia que difiere de la de los genes nucleares. Las células somáticas de mamíferos tienen generalmente 103-104 copias de ADNmt con ~2-10 genomas por orgánulo. Estos genomas se replican de manera independiente del ciclo celular que se rige por la replicación del ADN nuclear (Wilson et al., 2016). En mamíferos, el ADNmt se hereda por vía materna y no sigue un patrón de herencia mendeliana. En humanos, el ADNmt paterno se pierde durante la fecundación por un mecanismo dependiente de ubiquitina mediado por endonucleasas (Fernández-Silva et al., 2003). Los beneficios de una herencia mitocondrial uniparental es evitar el paso de mutaciones deletéreas por el gameto no sometido a control (las mitocondrias espermáticas llegan a los ovocitos con daños en su ADN y sin haber experimentado ningún control). Debido a este tipo de herencia se reducen al mínimo las copias del genoma mitocondrial en un ovocito produciendo un cuello de botella que eliminaría las copias defectuosas. El hecho de que el ADNmt sea un genoma de múltiples copias hace que un individuo pueda albergar más de una sola secuencia, una condición conocida como heteroplasmia. Una variante de la secuencia que contenga una mutación, y sea por tanto perjudicial, puede ser tolerada en bajo número de copias, porque el producto del gen defectuoso que codifica no alcanza el umbral para alterar la función celular. Sin embargo, se conocen variantes de la secuencia que segregan rápidamente desde heteroplasmia a homoplasmia al pasar de una generación a la siguiente (Wilson et al., 2016). Esto puede resultar en que la variante perjudicial predomina en la descendencia, lo que conduce a un fenotipo mitocondrial defectuoso (Wilson et al., 2016; Shoubridge, 2000).
Cabe destacar que el genoma mitocondrial no está protegido por histonas por lo que su tasa de mutación es más elevada que la del ADN nuclear. El estrés oxidativo en el ADNmt, junto con un desequilibrio en la cadena respiratoria mitocondrial y en la homeostasis del Ca2+, la excitotoxicidad, la apoptosis, los cambios en la permeabilidad de membrana, y los sistemas de defensa mitocondriales son las causas notables del desarrollo de enfermedades neurodegenerativas (Castro et al., 2012).
Alternativas a la terapia génica de la línea germinal, como son el diagnóstico prenatal y el diagnóstico preimplantacional (DGP), se han descrito para las parejas en riesgo de transmitir los trastornos derivados de mutaciones en el ADNmt. Aunque estas técnicas son potencialmente útiles para las condiciones de baja heteroplasmia, son ineficaces para las condiciones de homoplasmia donde la carga mutante de ADNmt del paciente puede llegar a ser del 100% y, además, la variación entre blastómeros de un mismo embrión limita la efectividad de este tipo de test. Las técnicas de transferencia de genoma nuclear (la transferencia pronuclear, la transferencia del huso meiótico y la transferencia del corpúsculo polar) en un ovocito enucleado que contenga mitocondrias sin mutaciones probablemente sería una buena elección para prevenir de manera efectiva la transmisión de enfermedades mitocondriales (Mitalipov et al., 2014).
MATERIAL Y MÉTODOS
La búsqueda de esta revisión bibliográfica se ha realizado mediante las bases de datos PudMed (NCBI), Google Académico (Google), las revistas Fertility & Sterility y Human Reproduction y la página web de la Human Fertilisation and Embryology Authority (HFEA) con artículos comprendidos entre 1983 a 2016. Las palabras clave usadas en la búsqueda bibliográfica fueron las siguientes: ‘mitochondria’, ‘mitochondrial DNA’, ‘mitochondrial diasease’, ‘pronuclear transfer’, ‘maternal spindle transfer’, ‘polar body transfer’, ‘tri-parenthood fertilisation’, ‘oocyte’, ‘gamete’ y ‘embryo’. La finalidad de esta revisión fue conocer las bases teóricas que sustentan las técnicas englobadas bajo el nombre de fecundación in vitro triparental y la metodología usada (desde sus inicios hasta la actualidad), así como reunir y analizar las evidencias a favor y en contra de la técnica, tanto a nivel de metodología como a nivel de normativa y conflictos éticos asociados.
RESULTADOS
Transferencia pronuclear
El estadio de cigoto en mamíferos se caracteriza por la presencia de dos pronúcleos (PN) claramente visibles y que contienen ADN nuclear haploide proveniente o bien del espermatozoide o bien del ovocito. La transferencia pronuclear (PNT) de cigoto a cigoto fue llevada a cabo por primera vez durante la década de los 80, cuando se demostró que los ratones manipulados por esta técnica daban lugar a descendencia. Ha sido más recientemente utilizada para la terapia de reemplazo mitocondrial, pero la técnica utilizada en ratones se ha visto negativamente afectada por los altos niveles de ADNmt residual en las crías (Sato et al., 2005).
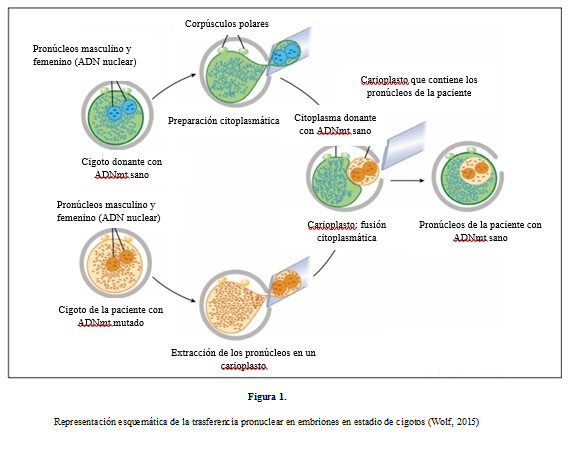
El pronúcleo masculino y el pronúcleo femenino ambos altamente visibles y de apariencia similar, son extraídos (enucleación) después de un tratamiento mediante inhibidores del citoesqueleto (nocodazole y cytochalasin B), tanto del ovocito de la paciente como del ovocito de la donante mediante la aspiración de carioplastos usando técnicas de micromanipulación (ver Figura 1). Hay que tener en cuenta que el carioplasto proveniente del ovocito de la paciente contiene tanto mitocondrias como ADNmt, conocido como carryover o residual. Los carioplastos que contienen los PN de la paciente se ponen en contacto con el citoplasma de los ovocitos de la donante. Las dos entidades se fusionan produciendo un embrión reconstruido que estaría listo para el cultivo o la transferencia embrionaria a la paciente. Debido a que con la inyección de los PN de la paciente se ha arrastrado también parte de sus mitocondrias, el cigoto reconstruido aún puede contener cantidades inaceptables de ADNmt mutado (McGrath and Solter, 1983).
Los resultados en ratones no fueron buen presagio para las técnicas de reemplazo mitocondrial (MRT) en los seres humanos. Sin embargo, en 2010 se informó de la viabilidad de la PNT en humanos usando cigotos anormales, ya fuera con uno o más de dos PN, que normalmente se desechaban durante la rutina de la fecundación in vitro. El 8% de los embriones creados por transferencia nuclear se desarrollaron hasta la etapa de blastocisto con niveles bajos de ADNmt residual (<2%). A pesar del bajo rendimiento de embriones que llegaban al estadio de blastocisto, los autores concluyeron que este enfoque arrojaba potencial a la técnica del reemplazo mitocondrial. Sin embargo, es imposible en la actualidad evaluar la seguridad y la eficacia de PNT en cigotos humanos normales sobre la base de este informe preliminar, ya que se tiene que seguir la investigación en primates no humanos antes de llegar a una conclusión definitiva en la viabilidad PNT como una técnica de MRT en humanos (Cravenet al., 2010; Tachibana et al., 2009).
Transferencia del huso meiótico
La transferencia del huso meiótico (ST) aplicada en ovocitos de macaco (Macaca mulatta) demostró en 2009 que la transferencia por remplazo mitocondrial podía ser usada en estadio de ovocito no fecundado. Se demostró la eficacia y la seguridad de la técnica al obtener nacidos vivos los cuales tenían curvas normales de crecimiento y bajos niveles de ADNmt residual (Tachibana et al., 2012).
A diferencia de los cigotos, la distribución de las mitocondrias en los ovocitos es uniforme, lo que permite llevar a cabo la técnica de transferencia del huso meiótico sin un significativo arrastre del ADNmt del ovocito que dona el núcleo (Tachibana et al., 2012).
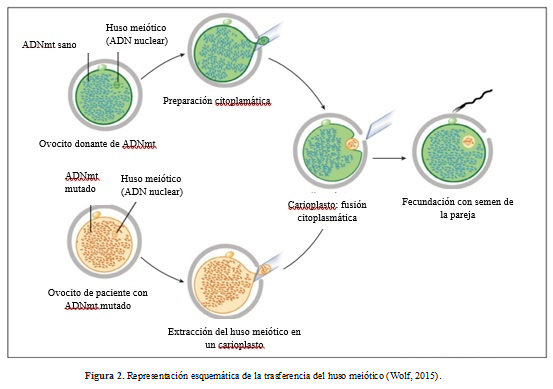
El huso meiótico rodeado por un pequeño volumen de citoplasma y de membrana es extraído del ovocito de la paciente y del ovocito de la donante. Estos carioplastos contienen sólo el 1.5% del volumen del citoplasma. Los carioplastos de los ovocitos de pacientes son fusionados en el citoplasma de los ovocitos donantes (previamente enucleados) y fecundados por el esperma de la pareja (ver Figura 2) creando un embrión libre de mutaciones en el ADNmt (Tachibana et al., 2013).
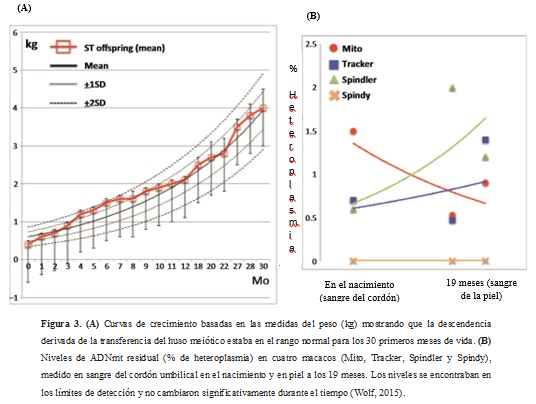
Se llevó a cabo un estudio en hembras de macacos de origen indio y macacos de origen chino portadoras de diferentes haplotipos de ADNmt wildtipe que fueron identificadas basándose en secuencias de polimorfismos. Los carioplastos de los macacos de origen chino se fusionaron con ovocitos donantes de macacos de origen indio y viceversa para crear ovocitos reconstruidos con donantes de ADNmt. Se fecundaron mediante inyección intracitoplasmática de espermatozoides (ICSI) y los embriones resultantes se cultivaron hasta blastocisto. El desarrollo y la calidad de los embriones fue comparable a la de los controles, y se establecieron dos líneas de células madre embrionarias (ESCs) a partir de 8 embriones a los que se les había realizado transferencia del huso meiótico siendo la eficiencia en la derivación comparable a la de los controles. Quince blastocistos se transfirieron a nueve hembras, dando lugar a tres embarazos y a cuatro nacidos vivos. La eficiencia fue similar a los resultados con embriones no manipulados (embriones control). Como se puede observar en la Figura 3, las crías de los macacos provenientes de la transferencia de huso meiótico tenían curvas de crecimiento normales, cantidades residual de ADNmt por debajo o igual al 2% y niveles normales de ATP (Paull et al., 2013).
Estos resultados en macaco alentaron los estudios en humanos donde donantes de ovocitos con diferentes haplotipos de ADNmt fueren reclutados con fines de investigación. De 106 ovocitos donados a investigación, 65 fueron sujetos a transferencia recíproca del huso meiótico y 33 fueron usados como controles. Las tasas de fecundación en ovocitos a los que se les había practicado la transferencia del huso fueron del 73%, muy similar a la de los controles (75%). Sin embargo, una porción significativa de los cigotos presentaba fecundación anormal (la mayoría de ellos con la presencia de tres pronúcleos). Este resultado reflejaba la activación prematura del ovocito a causa de condiciones de cultivo subóptimas. De los cigotos que presentaban una fecundación normal, sus tasas de desarrollo a blastocisto (62%) y de aislamiento de las células madre embrionarias (38%) fueron comparables con los controles, a la vez que se estimaron que los niveles de ADNmt residual eran indetectables (Tachibana et al., 2013; Paull et al., 2013).
La viabilidad de los ovocitos humanos con el huso meiótico transferido fue examinada mediante la activación artificial para mimetizar la fecundación y su posterior desarrollo. Algunos embriones partenogenéticos progresaron a blastocisto dando lugar a la derivación de ESCs. Los niveles de ADNmt heteroplasmático en las líneas de ESCs fueron menores al 1%. Aunque este estudio fue llevado a cabo con embriones partenogenéticos, los resultados eran consistentes con la conclusión de que la técnica de transferencia del huso meiótico podía ser consumada en humanos con el mínimo nivel de ADNmt residual (Paull et al., 2013).
Transferencia del corpúsculo polar
Los ovocitos humanos durante la meiosis sufren dos divisiones con reducción de la carga cromosómica con la segregación desigual del citoplasma y la extrusión de dos corpúsculos polares. El primer corpúsculo polar contiene un set diploide de cromosomas, y el segundo corpúsculo está dotado de un set haploide de cromosomas y se extruye después de que el espermatozoide haya fecundado el óvulo (Wakayama and Yanagimachi, 1998).
En la técnica de la transferencia del corpúsculo polar se usa un cigoto donante con ADNmt sano al cual se le extrae el pronúcleo femenino. Al cigoto donante se le fusiona el segundo corpúsculo polar proveniente del cigoto de la paciente que contiene ADNmt mutado tal y como se muestra en la Figura 4 (Wakayama and Yanagimachi, 1998).
En ratones, a los que se les llevó a cabo la transferencia del segundo corpúsculo polar se observó el desarrollo a término de la descendencia (Wakayama and Yanagimachi, 1998; Wakayama T. et al., 1997). La transferencia del corpúsculo polar ha sido descrita recientemente en el contexto de la terapia por reemplazo mitocondrial. Su justificación es que los corpúsculos polares que contienen pocas mitocondrias podrían ser fácilmente visualizados y manipulados, mientras su eficiente utilización podría doblar el rendimiento de los ovocitos y cigotos reconstruidos mediante ST y PNT. Usando un enfoque basado en transferencias simultáneas del primer corpúsculo polar y del huso meiótico de 27 ovocitos donantes, se produjeron 43 ovocitos reconstruidos. También se llevaron a cabo transferencias simultáneas del segundo corpúsculo polar y de pronúcleos para incrementar el rendimiento de los cigotos donantes. El número de recién nacidos vivos derivados de la reconstrucción de ovocitos o de embriones fue muy similar al de los controles, y el ADNmt residual, en crías derivadas de la transferencia del primer corpúsculo polar, de la transferencia del segundo corpúsculo polar, de la transferencia del huso meiótico, pero no de la transferencia de pronúcleos, fue muy bajo o indetectable. Las tasas de nacimiento fueron comparables con los controles, y todas las crías vivas derivadas de ovocitos reconstruidos respiraban normalmente y tenían un rango de peso comparable a la de los controles que no habían sido manipuladas. La transferencia del corpúsculo polar no ha sido replicada con éxito en otros mamíferos (incluidos primates) a pesar de los considerables esfuerzos. En muchas especies, los corpúsculos experimentan unas altas tasas de degeneración debido a las presiones apoptóticas que causan fragmentación del ADN y su degradación (Wakayama T. et al., 1997; Daughtry and Mitalipov, 2014).
En humanos, los esfuerzos se han centrado en el análisis genético del corpúsculo polar para la evaluación de enfermedades; sin embargo, su capacidad funcional para la transferencia del corpúsculo polar permanece sin determinar. Los esfuerzos por aislar corpúsculos polares viables después de una estimulación ovárica en pacientes podrían ser contraproducentes si hubiera alteraciones sustanciales en los tiempos del cultivo de los ovocitos y por consecuente, de sus corpúsculos polares (Daughtry and Mitalipov, 2014).
Transferencia mitocondrial para pacientes infértiles
La edad avanzada de la mujer (mayor de 35 años) es uno de los factores determinantes cuando se habla de infertilidad, abortos o defectos en el nacimiento como puede ser el Síndrome de Down. Diversos estudios apuntan que a medida que aumenta la edad de la paciente, su calidad ovocitaria disminuye siendo ésta la principal causa de su infertilidad. En pacientes con edad avanzada se observa una maduración citoplasmática despareja que podría explicar el aumento en anomalías y aneuploidías causadas por fallos tanto en el proceso de meiosis como en el de mitosis. Las deficiencias citoplasmáticas de estos ovocitos se observan en una deficiencia en sus transcritos y proteínas que podrían causar un impacto en el desarrollo del embrión preimplantatorio (Minami et al., 2007; Tanget al., 2007). Se han observado asociaciones entre el aumento de la edad de la paciente y el aumento de la tasa de mutación en el ADNmt de los ovocitos, la disminución de la actividad metabólica embrionaria, la disminución en la producción de ATP, y la alteración de la homeostasis del calcio mitocondrial. Además, se observa un aumento de deleciones en el ADNmt descritas en las células del cúmulo que son las que rodean al ovocito dándole a su vez un aporte metabólico. Las deficiencias citoplasmáticas en general y la disfunción mitocondrial en particular pueden contribuir a la inestabilidad del genoma nuclear en ovocitos provenientes de mujeres en edad avanzada, resultando en un embrión aneuploide. Pacientes de edad avanzada que no poseen ovocitos propios criopreservados durante una edad temprana reproductiva, ven como sus tratamientos de FIV se ven limitados a la utilización de ovocitos y embriones de donante. Con el uso de la técnica del remplazo mitocondrial este tipo de pacientes se podría beneficiar del remplazo completo del componente citoplasmático a la vez que se mantendría el ADN nuclear de la mujer de la pareja para intentar mejorar la calidad embrionaria (Eichenlaub-Ritter et al., 2001).
En 1998-1999, la primera transferencia citoplasmática realizada por Cohen et al. fue usada para transferir un pequeño volumen de citoplasma (1-5%) del ovocito donante en ovocitos de pacientes que habían sufridos fallos repetidos en ciclos de FIV. Han nacido ya más de 40 niños y la técnica se aplicó a una velocidad sorprendente en los seres humanos, en ausencia de una amplia investigación para evaluar la eficacia y los posibles riesgos del método, por lo que se puso en duda la técnica en distintas publicaciones (Eichenlaub-Ritter et al., 2001; Cohen et al., 1998).
DILEMAS ÉTICOS Y LEGISLACIÓN
La terapia génica en células somáticas no ha causado grandes controversias por lo referente a su aceptación ética principalmente porque los cambios genéticos no se transmiten a la descendencia. Por lo contrario, la terapia génica en la línea germinal lleva implícita la corrección permanente de genes mutados en las células germinales, resultando en la transferencia de esas alteraciones a las subsecuentes generaciones. Si tomamos como significado de modificación la introducción de nuevo material genético en los gametos (o embrión temprano), en el caso de la técnica de remplazo mitocondrial se introduce ADNmt de la donante no sólo a la descendencia, sino también a la siguiente generación (esta vez se restringe al linaje femenino). Si, por el contrario, consideramos modificación de la línea germinal únicamente la realización de cambios en el ADN nuclear, las técnicas de remplazo mitocondrial no supondrían una modificación de la línea germinal. Cabe destacar que es bien sabido que el ADNmt no codifica para componentes determinantes en la identidad genética o de parentesco (Robertson, 1999).
En cuanto a la aplicación de las técnicas de transferencia citoplasmática o de las técnicas de remplazo mitocondrial, se criticó sobre todo su introducción prematura, señalándose la ausencia de investigación básica y preclínica, así como de adecuados controles experimentales y falta de discusión pública ética y crítica. En las primeras aplicaciones de la transferencia citoplasmática, se informaron un número relativamente alto de anomalías cromosómicas y defectos en el recién nacido, por ello, a pesar de no estar claro si estaba relacionado con la técnica per se, ante la preocupación de los organismos reguladores, la Food and Drug Administration (FDA) declaró en 2001 que la transferencia citoplasmática y los protocolos relacionados estaban sujetos a revisión y aprobación formales. Así, se prohibieron de forma prematura los ensayos clínicos necesarios para abordar estas cuestiones debido al carácter controvertido que suscitaba la manipulación de gametos (Hawes et al., 2002).
El problema conceptual entre el remplazo mitocondrial y la transferencia citoplasmática se basa en el hecho de si se entienden o no como modificación de la línea germinal, lo que llevará a un diferente análisis normativo de la misma, ya que la modificación de la línea germinal humana es éticamente mucho más controvertida que la modificación genética de la línea somática. La modificación de la línea germinal humana está prohibida por órganos internacionales, como el Consejo de Europa. Sin embargo, algunos países hacen una distinción legal entre ambas. La Ley holandesa de Embriones (2002), por ejemplo, deja espacio para la modificación del ADNmt pero prohíbe la del ADN nuclear. La evaluación ética de la modificación de la línea germinal (en el contexto de los trastornos de ADNmt) difiere de si se trata de la transferencia del ST o del PNT. Ambas implican la donación de ADNmt, pero la última implica la creación y destrucción de un embrión durante el proceso de la técnica, lo que puede chocar con ciertas ideologías religiosas (Bredenoord et al., 2008).
En el Reino Unido, en febrero del 2015 se aprobó la ley que permite el uso de la transferencia del huso meiótico materno y la transferencia pronuclear para evitar enfermedades mitocondriales severas. En la página web de la Human Fertilisation and Embryology Authority (HFEA) se aclara que antes de que una clínica pueda poner en práctica estas técnicas, deberá seguir un proceso de licencia que consta de dos pasos: necesitarán aplicar para una licencia que les permita realizar la transferencia del huso meiótico y/o la transferencia pronuclear y luego pedir autorización para llevar a cabo el tratamiento de una paciente en concreto. Además, se requerirá que las clínicas presenten información sobre las donantes de mitocondrias, los pacientes que van a ser tratados y el proveedor de esperma, y del tratamiento al que se someten (HFEA website).
Por otra parte, se deben examinar las cuestiones éticas con respecto a si los niños resultantes de éstas técnicas pueden ser correctamente considerados como si tuvieran dos o tres padres (la técnica se conoce comúnmente como FIV triparental). Tras la transferencia citoplasmática o las técnicas de remplazo mitocondrial el embrión hereda la gran mayoría de su ADN de la madre y el padre intencional, más un porcentaje de ADNmt de la donante de ovocitos. Para poner esto en perspectiva: la donante podría contribuir en un 0.1% de su ADN, mientras que los padres intencionales contribuyen al restante 99.90% de su ADN. Estrictamente hablando, tendría tres padres. Algunos sostienen que esta división de la maternidad genética debe ser considerada como el principal problema ético en el debate sobre la técnica. Las consecuencias psicológicas, jurídicas y sociales de tener tres padres genéticos son en gran parte desconocidas. Por otra parte, es discutible si la donante de ovocitos, que contribuye con su ADNmt, debe ser considerada como un ‘padre genético’. La variación de secuencias entre diferentes haplotipos mitocondriales en la población humana es pequeña, ya que se trata de unas pocas sustituciones de amino ácidos. Esto tendría fácil solución, ya que es posible reducir las diferencias en ADNmt usando donantes de mitocondrias con el mismo haplotipo (Mitalipov and Wolf, 2014).
Los datos disponibles son insuficientes y no apoyan una decisión prudente acerca de la aplicación de la transferencia citoplasmática y de las técnicas de remplazo mitocondrial. Las razones por las cuales estas técnicas conduzcan a un anormal desarrollo del embrión transferido están lejos de aclararse. Por lo tanto, es necesaria una exhaustiva labor científica y de investigación antes de introducir está técnica definitivamente en la práctica clínica.
CONCLUSIÓN
La necesidad de la implementación de técnicas de remplazo mitocondrial y de transferencia citoplasmática parece evidente para familias portadoras de enfermedades debido a mutaciones en el ADNmt y para aquellas pacientes de edad avanzada (sin ovocitos criopreservados en su edad fértil) o con numerosos ciclos fallidos de FIV. Si la necesidad existe, y la ratio riesgo/beneficio es favorable, entonces nos formulamos la pregunta de cómo podríamos avanzar hacia la implementación de éstas técnicas. Se trata de técnicas cuya eficiencia debería ser mejorada por lo que sería necesario generar resultados confirmatorios adicionales. Aún dicho esto, la HFEA ha presentado una revisión bibliográfica sobre los resultados publicados sobre el ST y el PNT que muestran que ambas técnicas son potencialmente útiles para un grupo específico y definido de pacientes cuya descendencia tendría una enfermedad severa o letal producida por mutaciones en su ADNmt, y los cuales no tienen otra opción para engendrar su propia descendencia. El comité concluyó que las evidencias que se tienen actualmente no sugieren que las técnicas sean ‘inseguras’. Sin embargo, las primeras aplicaciones clínicas deberían ser llevadas a cabo en clínicas especializadas en enfermedades mitocondriales que impliquen ensayos clínicos. Se debería ofrecer una amplia información y apoyo a las familias inscritas en dichos ensayos y su participación debería estar comprometida a su consentimiento para el seguimiento de los hijos nacidos por estas técnicas.
Mirando mucho más lejos en el futuro, últimamente están emergiendo las tecnologías de edición del genoma y se erigen como las técnicas que permitirían la corrección dirigida de genes mutados en células humanas. Estas correcciones implican la modificación precisa de las secuencias de genes añadiendo, eliminando o corrigiendo locis genómicos específicos. Esos avances probablemente permitirán la corrección selectiva de defectos genéticos nucleares o mitocondriales en gametos humanos o embriones preimplantatorios, impidiendo así en última instancia el paso de la mayoría de las condiciones genéticas anómalas y evitando el uso de ADNmt de donante eliminando así la participación del tercer ‘progenitor’ genético.
Referencias
Fernández-Silva P, Enriquez JA, Montoya J. Replication and transcription of mammalian mitochondrial DNA. Exp Physiol, 2003, 88(1):41–56.
DiMauro S, Davidzon G. Mitochondrial DNA and disease. Am J Med Genet, 2005, 37: 222–232.
Scarpulla RC.Transcriptional Paradigms in Mammalian Mitochondrial Biogenesis and Function. Physiol Rev, 2008, 88: 611-638.
Clayton DA. Mitochondrial DNA replication: what we know. IUBMB Life, 2003, 55: 213–217.
Wilson IJ, Carling PJ, Alston CL et al. Mitochondrial DNA sequence characteristics modulate the size of the genetic bottleneck. Hum Mol Genet, 2016, 1; 25(5):1031-41.
Bredenoord AL, Pennings G, de Wert G. Ooplasmic and nuclear transfer to prevent mitochondrial DNA disorders: conceptual and normative issues. Human Reprod, 2008, 14:669-78.
Castro MR, Suarez E, Kraiselburd E, et al. Aging increases mitochondrial DNA damage and oxidative stress in liver of rhesus monkeys. Exp Gerontol, 2012, 47:29–37.
Cohen J, Scott R, Alikani M et al. Ooplasmic transfer in mature human oocytes. Mol Hum Reprod, 1998; 4 (3):269-80.
Craven L. et al. Pronuclear transfer in human embryos to prevent transmission of mitochondrial DNA disease. Nature, 2010, 465:82–85.
Daughtry B. and Mitalipov S. Concise review: parthenote stem cells for regenerative medicine: genetic, epigenetic, and developmental features. Stem Cells Transl. Med., 2014, 3:290-298.
Eichenlaub-Ritter U. et al. Age related changes in mitochondrial function and new approaches to study redox regulation in mammalian oocytes in response to age or maturation conditions. Mitochondrion 5, 2001, 783-796.
Hawes SM, Sapienza C, Latham KE. Ooplasmic donation in humans: the potential for epigenic modifications. Hum Reprod, 2002, 17:850-2.
HFEA website: http://www.hfea.gov.uk/9933.html.
McGrath J. and Solter D. Nuclear transplantation in the mouse embryo by microsurgery and cell fusion. Science, 1983, 220:1300–1302.
Minami N. et al. Zygotic gene activation and maternal factors in mammals. J. Reprodu. Dev, 2007, 53:707-715.
Mitalipov S, Wolf P. Clinical and ethical implications of mithocondrial gene transfer. Trends Endocrinol Metab, 2014, 25(1):5-7.
Mitalipov S. et al. Limitations of preimplantation genetic diagnosis for mitochondrial DNA diseases. Cell Rep, 2014, 7:935–937.
Paull D. et al. Nuclear genome transfer in human oocytes eliminates mitochondrial DNA variants. Nature, 2013, 493:632–637.
Robertson J.A. Reconstituting eggs: the ethics of cytoplasm donation. Fertil. Steril, 1999, 71:219-221.
Shoubridge EA. Mitochondrial DNA segregation in the developing embryo. Hum Reprod, 2000, 15: 229–234.
Tachibana M. et al. Chromosome transfer in mature oocytes. Fertil. Steril, 2012, 97:e16.
Tachibana M. et al. Mitochondrial gene replacement in primate offspring and embryonic stem cells. Nature, 2009, 461:367–372.
Tachibana M. et al. Towards germline gene therapy of inherited mitochondrial diseases. Nature, 2013, 493:627–631.
Tang F. et al. Maternal microRNAs are essential for mouse zygotic development. Genes Dev., 2007, 21:644-648.
Wakayama T. and Yanagimachi R. The first polar body can be used for production of normal offspring in mice. Biol. Reprod, 1998, 59:100-104.
Wakayama T. et al. Participation of the female pronucleus derived from the second polar body in full embryonic development of mice. J.Reprod. Fertil, 1997, 110:263-266.
Wolf D, Mitalipov N, Mitalipov S. Mitochondrial replacement therapy in reproductive medicine. Trends in Molecular Medicine, 2015; 21(2):68-76.