EVALUACIÓN DE DOS MÉTODOS DE CAPACITACIÓN ESPERMÁTICA (SWIM-UP Y GRADIENTES) MEDIANTE EL ESTUDIO DE LA MORFOLOGÍA, MADUREZ Y FRAGMENTACIÓN DEL DNA DE LOS ESPERMATOZOIDES EN MUESTRAS DESTINADAS A IA
Burguera Girau, Alba; de la Orden Rodríguez, Marina; Martínez Sanchis, Juan Vicente;Fernández Colom, Pedro José; Rubio Rubio, José María.
Objetivo: mejora de las muestras seminales para IA y puesta a punto de herramientas accesorias para su evaluación.
Diseño y tamaño muestral: 191 muestras seminales; estudio prospectivo y aleatorio.
Material y Métodos: las muestras se procesaron con Swim-Up o Gradientes. Se anotaron diferentes tiempos (recogida, procesado, capacitado y inseminado). Se realizaron 3 extensiones en fresco por muestra: morfología (Diff Quick), madurez (Azul de Anilina) y fragmentación de DNA (Naranja de Acridina), y 2 en capacitado (madurez y fragmentación).
Resultados: obtuvimos un 16% de gestación con Gradientes y un 9’37% en Swim-Up (p_valor de 0’08). La media de edad de las pacientes embarazadas fue de 31’7, siendo significativa (p_valor 0’02). Los gradientes seleccionaron mejor los espermatozoides maduros (89’48% vs 91’33%) y sin fragmentación de DNA (81’21% vs 88’2%) que el Swim-Up con (p_valores = 0’014 y 0’006 respectivamente). El tiempo que pasa la muestra en el laboratorio resulta significativo, siendo las que menos tiempo pasan en el, las que mejor tasa de gestación presentan (p_valor 0’024).
Conclusión: la edad de las mujeres condiciona el éxito de la IA. Los Gradientes mejoran las TG de IA en la Unidad, sin llegar a ser estadísticamente significativo. Los gradientes consiguen recuperar un mayor número de espermatozoides maduros y sin fragmentación de DNA. Cuanto menos tiempo pasa la muestra en el laboratorio mejor para la consecución del embarazo.
INTRODUCCIÓN:
Atendiendo a una mejora de los resultados en la técnica de Inseminación Artificial (IA) nos planteamos optimizar los protocolos de trabajo. Nos proponemos averiguar: la influencia de dos técnicas de capacitación (Swim-Up y Gradientes), la valoración de la morfología espermática (mediante ISAS), estado de DNA (madurez y fragmentación), y si el tiempo desde la recogida de la muestra hasta la inseminación es significativo en el éxito de la IA.
MATERIAL Y MÉTODOS:
Se analizó, junto con recuento y motilidad, la morfología, madurez y fragmentación de DNA de 191 muestras de semen procesadas mediante Swim-up o Gradientes para realizar IA en el Hospital La Fe de Valencia. Las muestras homólogas fueron obtenidas por masturbación, con abstinencia de 3 a 5 días, en botes estériles. Antes de procesar las muestras, se valoró su recuento y motilidad en fresco y en capacitado después de procesarse mediante el método correspondiente.
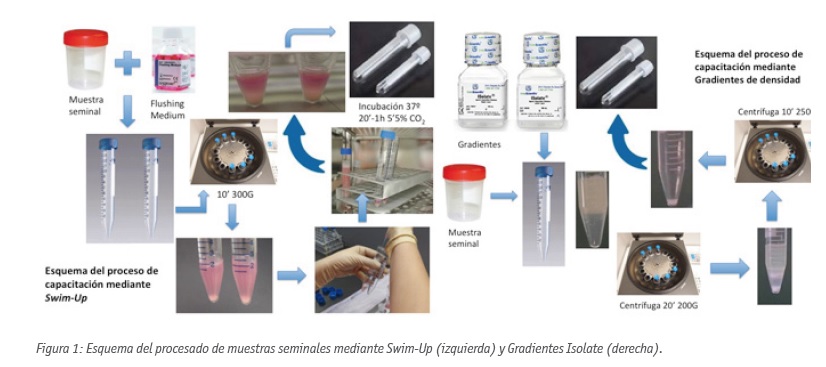
Procesamiento mediante Swim-Up.
97 muestras de las 191 se procesaron mediante Swim-Up. Se repartió cada muestra en dos tubos falcon (Fisher Scientific; Cat.: 05-539-5) y se mezcló volumen a volumen con Flushing Medium (Origio; Cat.:10845060). Las muestras fueron centrifugadas durante 10’ a 250G. Después se eliminó el sobrenadante y se añadieron 250 μl de medio de cultivo (IVF, Origio; Cat.: 10315060). Se incubaron entre 20’ y 1h y pasado el tiempo, se recogió la capa superficial de medio, y se aisló en un tubo estéril. La muestra se volvió a guardar en el incubador hasta su uso.
Procesamiento mediante Gradientes.
94 de las 191 muestras se procesaron mediante Gradientes. Se prepararon los gradientes según el protocolo de Isolate (Irvine; Cat.: 99264). El medio se sacó de la nevera 30’ antes de su uso, y en un tubo falcon (Fisher Scientific; Cat.: 05-539-5) se repartió 1’5 ml de cada fase. Sobre las dos fases se colocaron 2 ml de la muestra de semen (o toda la muestra en caso de poseer menos de 2 ml). Los tubos fueron centrifugados 20’ a 200G, y se separó el pellet metiendo una pipeta Pasteur hasta el fondo del tubo. Esta fase se mezcló con 2 ml de Flushing Medium (Origio; Cat.:10845060) y se centrifugaron los tubos 10’ a 200G. Al terminar la centrífuga, se eliminó el sobrenadante y los pellets se resuspendieron en 0’5 ml de medio de cultivo IVF (Origio; Cat.: 10315060). El resuspendido se separó en un tubo estéril y se guardó en campana, a temperatura ambiente, hasta su uso.
Morfología.
De cada muestra en fresco, se cogieron 7 μl con los que se realizó una extensión en un porta y se dejó secar al aire. Realizamos la tinción Diff Quick: las muestras se fijaron en 30’’ en etanol absoluto (Panreac; Cat.: 131086) y sin dejar secar se sumergieron 30’’ en eosina roja (Panreac; Cat.:253999) y 30’’ en eosina azul (Panreac; Cat.: 251416). Se lavó cada porta con agua destilada y se dejó secar. Posteriormente se montaron con un cubreobjetos con Eukitt y se dejaron secar para su posterior observación al microscopio. Las morfologías se analizaron utilizando un programa informático (ISAS, Proiser). Se obtuvieron fotografías de 100 espermatozoides de cada muestra obteniendo el porcentaje de espermatozoides normales de cada muestra (Figura 1).
Azul de Anilina.
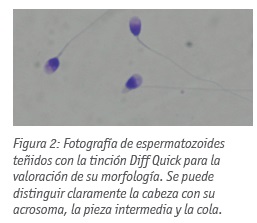
De cada muestra se realizaron 2 extensiones de 7 μl, una en fresco y otra en capacitado. Se dejaron secar al aire y se fijaron en Metanol (Merk) 10’. A continuación se lavaron con agua destilada y se dejaron secar. Posteriormente se tiñeron 5’ en azul de anilina (Panreac; Cat.: 253708.1606). Una vez teñidas las muestras, se lavaron con agua destilada, se dejaron secar y se montaron con un cubreobjetos y medio de montaje Eukitt. Se leyeron 100 espermatozoides a 100x y bajo aceite de inmersión, contando el número de cabezas teñidas (Figura 2).
Naranja de Acridina.
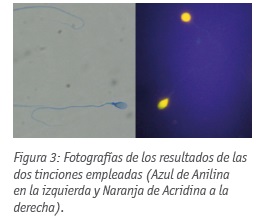
De cada muestra se realizaron 2 extensiones, una con la muestra en fresco y otra con la muestra capacitada, de 7 μl cada una. Se dejaron secar al aire y se fijaron entre 2’-4’ en Carnoy (metanol-ácido acético 3:1) y se dejaron secar. En el momento de leer las muestras, se tiñeron con Naranja de Acridina (Sigma) 4’, se lavaron con agua destilada y se dejaron secar para ser leídas inmediatamente a 100x bajo el microscopio de fluorescencia, contando el número de espermatozoides verdes y anaranjados (Figura 3).
Tiempos.
De cada inseminación anotamos 4 horas: hora de recogida (cuando el paciente eyacula la muestra), hora de procesado (momento en el que la muestra empieza a procesarse), hora de capacitado (momento en el cual la muestra está lista para inseminarse), hora de IA (cuando se realiza la inseminación). Con estas horas calculamos 3 tiempos que luego tuvimos en cuenta en nuestros análisis: tiempo de licuado de la muestra (TL: minutos que pasan entre que se recoge la muestra y se procesa), tiempo de Inseminación (TIA: minutos que pasan entre que el capacitado está preparado y se realiza la Inseminación Artificial), y tiempo total de procesado de la muestra (TTPM: minutos que pasa entre que se obtiene la muestra y se realiza la inseminación).
RESULTADOS:
Exponemos los datos en forma de medias. Las variables categóricas se analizaron usando un test de Chi-Cuadrado, y las continuas usando el test T. Utilizamos Regresión Logística para analizar las correlaciones entre las diferentes variables y la consecución o no de embarazo. Consideramos estadísticamente significativos los p_valores <0’05, y comprobamos que todas las variables se distribuyen de forma normal y homogénea.
Descripción general de la población de estudio
En total hemos analizado 191 ciclos de Inseminación Artificial en 131 parejas del Hospital La Fe de Valencia, entre Septiembre y Diciembre de 2013. La media de edad de las parejas fue de 33’6 años en ellas y 35’5 años en ellos. El 73’4% de las mujeres estaban diagnosticadas como función reproductora normal (FRN), 13’83% como anovuladoras, 2’13% como fase lútea inadecuada (FLI), 6’9% como fallo ovárico precoz (FOP), y 3’7% con otras causas (endometriosis leve, lesión tubárica no obstructiva, alteraciones genéticas o malformaciones genitales). En cuanto a ellos, el 5’5% estaban diagnosticados de normozoospermia, un 69’23% de astenozoospermia (leve y moderada), un 12’63% de azoospermia y un 12’63% de oligoastenozoospermia. En el momento de la realización de las inseminaciones, la media del índice de masa corporal (IMC) de las mujeres fue de 23’32%. La media de días que fueron estimuladas fue de 8’2%, la última FSH tomada de 6’43% y la última LH de 5’32%.
Resultados del estudio
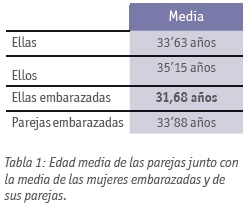
Analizamos si las edades de ellas y de ellos (Tabla 1) afectan a la TG de las IA, obteniendo un p_valor de 0’021 para ellas y de 0’309 para ellos; en ninguno de los dos casos el uso de Gradientes o Swim-Up beneficia o perjudica a las parejas más o menos jóvenes (p_valores de 0’16 y 0’2 respectivamente).
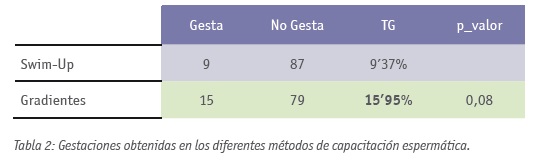
En cuanto a los datos analizados después de la realización de las IA, de las 191 IA, 24 resultaron gestantes (12’56%), dos de las cuales (8’3%) abortaron (un espontáneo y un ectópico). Analizamos si el número de gestaciones variaba en función de la técnica de capacitación espermática empleada, obteniendo 9 gestaciones de 96 muestras procesadas mediante Swim-Up (9’37%) y 15 gestaciones de 94 muestras procesadas mediante Gradientes (15’95%). El p_valor obtenido fue de 0’086>0’05, cercano a la significatividad (Tabla 2).
En cuanto a la morfología, el tener más o menos % de normales en fresco no parece afectar a la TG (p_valor = 0’315); sin embargo, cabe mencionar que ninguna de las pacientes embarazadas tenían un recuento de normales del 0%.
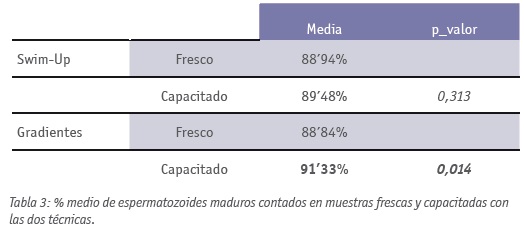
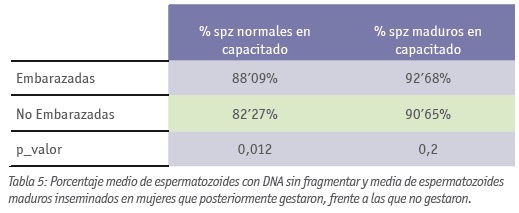
La técnica del Azul de Anilina nos permitió ver que la media de espermatozoides maduros recuperados con Gradientes era superior a los recuperados con Swim-Up (89’48% frente a 91’33% respectivamente) siendo estadísticamente significativo con un p_valor de 0’014 (Tabla 3). Sin embargo, no tenemos evidencia estadística de que las pacientes embarazadas fueran inseminadas con muestras con una mayor madurez espermática que las que no gestaron (p_valor 0’2) (Tabla 5).
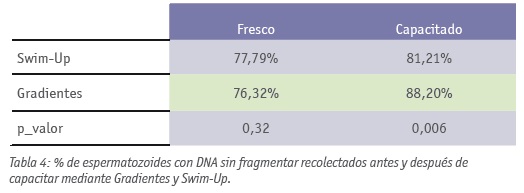
La tinción utilizada para valorar la fragmentación del DNA (Naranja de Acridina) nos permitió comprobar que los Gradientes seleccionan mejor espermatozoides sin fragmentación del DNA (81’21% de espermatozoides sanos recolectados mediante Swim-Up, frente al 88’2% mediante Gradientes, siendo el p_valor de 0’012) (Tabla 4); además, en este caso sí parece ser que las mujeres embarazadas fueron inseminadas con muestras con menor % de fragmentación del DNA espermático (88’09% en embarazadas frente al 82’27% de no embarazadas) (Tabla 5).
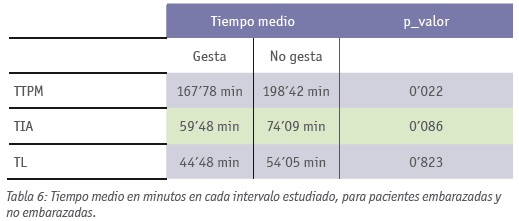
De los tiempos anotados en cada IA, resultó estadísticamente significativo el TTPM (p_valor = 0’022), siendo el promedio en pacientes embarazadas de 167’78 minutos y en no embarazadas de 198’42 minutos. El TL no resultó significativo (p_valor = 0’823), mientras que el TIA parece tener una leve significatividad, con un p_valor de 0’086, cercano al 0’05, siendo el tiempo medio de inseminación de las pacientes embarazadas de 59’48 minutos y en las pacientes no embarazadas de 74’09 minutos (Tabla 6).
Analizamos otros parámetros como el REM, diagnóstico de las parejas, número de folículos, IMC, o procedencia del semen (homólogo o donante), sin llegar a obtener datos estadísticamente significativos en ninguno de ellos.
DISCUSIÓN:
Uno de los factores más importantes a la hora de predecir el éxito o no de una IA es la edad de la mujer; Merviel et al. en su estudio de 2010 afirma que la edad de la mujer es uno de los factores más importantes que pueden predecir el éxito de la IA. En este estudio presentaban una tasa de gestación en mujeres menores de 30 años alrededor del 38%, mientras que pasaba a un 12’5% en mujeres cerca de los 40. Por otro lado, otro estudio de Brzechffa et al., 1998. afirma que por debajo de 40 años no hay variación en las tasas de gestación. Wainer et al., 2004 y Zapardiel Gutiérrez et al., 2007 están de acuerdo con que las mejores tasas de gestación se logran en mujeres jóvenes. En nuestro trabajo hemos obtenido una diferencia significativa en las edades de las mujeres embarazadas respecto a las que no lo están, siendo la media de las mujeres embarazadas de 31’7 años. Esto puede deberse a que la calidad ovocitaria de estas mujeres está menos deteriorada, lo cual, añadido al acortamiento de las distancias entre los gametos, el principal efecto de esta técnica, puede favorecer, junto a otros factores, el éxito de la gestación.
Cada laboratorio ha de encontrar su modo de trabajar, utilizando las técnicas y productos que más favorezcan sus resultados. Es por eso que decidimos probar una técnica de capacitación alternativa, los Gradientes Isolate (Irvine Scientific; California). Los resultados obtenidos (9 gestaciones en Swim-Up frente a las 15 con gradientes) nos permiten ver un ligero incremento de las tasas de gestación, de un 9’37% en Swim-Up, frente a casi un 16% por ciento en Gradientes (15’95%), datos similares a otros trabajos como el de Morshedi et al., 2003. Este resultado no resulta estadísticamente significativo (p_valor 0’086>0’05) como ocurre en el trabajo de Dodson et al., 1998. En el artículo de Ricci et al., 2009 justifican el uso de los gradientes para IA debido a que se obtiene una fracción mayor de espermatozoides móviles totales.
Muchos artículos, tales como Van der Zwalmen et al., 1991 y Prakash et al., 1998, estudian la diferencia de la morfología de los espermatozoides según el método de capacitación espermática, por lo que hemos querido evaluar la morfología en fresco para determinar si influye en el éxito de la inseminación, y valorar la inclusión de un análisis de rutina de la morfología en pacientes que van a someterse a IA. Sin embargo no hemos obtenido un resultado que correlacione la morfología en fresco con el éxito de la técnica, lo mismo que en el trabajo de Karabinus et al., 1997. De todas formas, cabe mencionar que ninguna de las muestras procesadas que dio lugar a embarazo, tenían un 0% de normales. Esto indica que por poco que sea el porcentaje de espermatozoides normales, la técnica de capacitado va a ayudar a mejorar la muestra, no siendo influyente el porcentaje del cual se parta (Karabinus et al., 1997). En el artículo de Zapardiel Gutiérrez et al., 2007 no obtienen diferencias significativas en cuanto a la TG según el porcentaje de formas normales, y en el de Hammadeh et al., 2001 y Prakash et al., 1998 obtienen resultados a favor de los gradientes en cuanto a mejora de la morfología tras el capacitado. En el repaso de la bibliografía que ofrece el estudio Van Waart et al., 2001 en cuanto a la morfología como predictor del éxito de las IAs, se observa que la tendencia a quedarse embarazada se ve disminuida si el porcentaje de espermatozoides es menor al 4%. Aún así, los autores de esta revisión recomiendan que si el porcentaje de normales es inferior al 4%, pero otros parámetros son adecuados (como el número total de espermatozoides móviles inseminados, motilidad o número de folículos) no se desaconseja el uso de una IA. Si todos estos parámetros, junto con la normalidad de los espermatozoides, se ven afectados, hay que recurrir a técnicas de fecundación in vitro. Wainer et al., 2004 observan una mejora en las morfologías tras capacitar la muestra, sin embargo estos datos no les ayudaron a predecir el éxito de la IA. También observaron que cuanto menor es el porcentaje de espermatozoides normales, mayor debe ser el número total de espermatozoides móviles inseminados. En nuestro trabajo analizamos la morfología mediante el ISAS (Integrated Semen Analysis System). Este sistema permite evaluar los parámetros morfológicos de los espermatozoides de forma objetiva (Soler et al., 2005); en el estudio de Soler et al. obtienen en muestras para IA una correlación negativa entre las TG y las cabezas grandes, recomendando su exclusión de esta técnica puesto que estos espermatozoides pueden tener problemas en la condensación de su cromatina.
Para analizar y justificar el uso de los Gradientes hemos utilizado dos técnicas para valorar la madurez espermática y la fragmentación del DNA, que son el Azul de Anilina y el Naranja de Acridina. El Azul de Anilina nos permite detectar un tipo de proteínas, presentes en el DNA del espermatozoide, las histonas, que durante la espermiogénesis deben sustituirse por protaminas (otro tipo de proteínas más compactas y densas), por lo tanto, aquellos espermatozoides azules tras la tinción lo son porque no han madurado correctamente (Golan et al., 1997; Kazerooni et al., 2009). Comparamos el porcentaje de espermatozoides maduros obtenidos tras capacitar con Swim-Up y con Gradientes, obteniendo diferencias estadísticamente significativas a favor de los Gradientes (p_valor 0’014). Esto quiere decir que los Gradientes seleccionan una mayor cantidad de espermatozoides maduros, debido a que al tratarse de una separación por diferencia de densidades, los espermatozoides más densos, es decir los que han sustituido sus histonas por protaminas, son los que se separan de los menos densos y los que son seleccionados para la Inseminación. En otros artículos como Kim et al., 2013 se correlaciona la condensación anormal de la cromatina detectada con el Azul de Anilina, con la morfología espermática, o en el de Alkhayal et al., 2013 que subraya el hecho de que pacientes infértiles con parámetros seminales normales pueden tener problemas en la cromatina de sus espermatozoides. Pese a todo esto, un dato curioso obtenido en nuestro estudio fue que las mujeres embarazadas no fueron inseminadas con un mayor porcentaje de espermatozoides maduros que las no embarazadas, lo cual nos indica que la madurez no es un factor clave a la hora de conseguir un embarazo; haría falta incrementar el número de muestras a evaluar para asegurar que no hay un sesgo.
El daño en el DNA de los espermatozoides puede ocurrir debido a 3 mecanismos: defectos en la condensación de la cromatina durante la espermiogénesis, inicio temprano de la apoptosis, o estrés oxidativo debido a la presencia de ROS (Duran et al., 2002). En un estudio reciente de 2012 (Jayaraman et al., 2012) se analizaron diferentes técnicas de capacitado en su capacidad para seleccionar espermatozoides no apoptóticos, y obtuvieron resultados similares para las técnicas empleadas, concluyendo que eran todas capaces de seleccionar espermatozoides no apoptóticos. La técnica del Naranja de Acridina marca de verde los espermatozoides con el DNA intacto, mientras que los que poseen fragmentación, su color vira a naranja-rojo (Cortés-Gutiérrez et al., 2007; Eggert-Kruse et al., 1996; Golan et al., 1997). En nuestros resultados obtenemos que con Gradientes se logra mejorar las muestras que poseen mayor porcentaje de espermatozoides con DNA fragmentado, con un p_valor de 0’012. Además en este caso si que parece ser que las mujeres embarazadas fueron inseminadas con mayor número de espermatozoides con el DNA sin fragmentar, lo cual nos permite poder relacionar los Gradientes con el aumento de gestaciones que ha experimentado la Unidad de Reproducción de nuestro Hospital. En el trabajo de Liu y Baker, 2007, en el que analizan la integridad del DNA de los espermatozoides unidos a la Zona Pelúcida (ZP) del ovocito, obtienen que los espermatozoides unidos a la ZP son los que mayor porcentaje de DNA normal poseen (en torno al 90%); además, pacientes con una proporción muy baja de espermatozoides con DNA normal, son los pocos que puedan ser normales los que consiguen unirse a la ZP, actuando ésta como barrera selectiva de espermatozoides. En otros estudios (Cortés-Gutiérrez et al., 2007; Duran et al., 2002) no obtienen embarazos en muestras con más de un 12% de fragmentación de la muestra.
Sin embargo, en el trabajo de Calderón-Mendoza et al., 2012 en el que comparan la mejora de las muestras espermáticas en cuanto a fragmentación del DNA usando las mismas técnicas de capacitación que en nuestro estudio, obtienen que tanto el Swim-Up como los Gradientes de Isolate mejoran las muestras, sin encontrar diferencias significativas entre ambas. Además, otro trabajo (Zini et al., 2000), encuentra mejores resultados en cuanto a fragmentación de DNA en las muestras procesadas mediante Swim-Up (cambe mencionar que utilizaron gradientes Percoll y no Isolate como en nuestro caso).
Del estudio de los tiempos podemos deducir que, cuanto menos tiempo pase la muestra en el laboratorio, más beneficiada resultará la pareja a la hora de conseguir el embarazo, siendo el TTPM el valor que más fuerza tiene a la hora de relacionarse con la tasa de gestación; el tiempo de IA, resultó estar cercano a la significatividad, lo cual nos incitó a analizar este tiempo por separado en las dos técnicas, y obtuvimos un p_valor de 0’016 en Swim-Up y de 0’33 en Gradientes, por lo tanto podemos deducir que el tiempo que pasa la muestra esperando después de procesar parece ser más importante cuando se realiza la primera técnica. Además, con nuestros datos pudimos observar que con los Gradientes el tiempo medio de procesado de la muestra es menor en comparación con el Swim-Up.
CONCLUSIÓN:
En este proyecto pretendíamos evaluar dos técnicas de capacitación espermática y plantearnos, en base a los resultados, modificar la metodología de trabajo en nuestro laboratorio. Obtuvimos más embarazos utilizando la técnica de Gradientes que con la de Swim-Up, sin embargo, pese a no ser resultados estadísticamente significativos, nuestras tinciones empleadas para detectar madurez espermática y fragmentación de DNA (Azul de Anilina y Naranja de Acridina respectivamente) indican que los Gradientes funcionan mejor a la hora de seleccionar los mejores espermatozoides, lo cual puede estar relacionado con el aumento de la tasa de gestación. El tiempo fue otro factor que consideramos analizar. Cuanto menos tiempo pase la muestra en el laboratorio, mejor para lograr una gestación, y la técnica que permitió una capacitación más rápida fueron los Gradientes. Independientemente y entre los factores clínicos a destacar según importancia, las mujeres de menor edad se ven favorecidas a la hora de quedar gestantes con esta técnica de Reproducción Asistida. Para finalizar, cabe mencionar que lo más importante es optimizar el trabajo en el laboratorio para lograr mejores resultados, adecuando los protocolos de trabajo dependiendo de las técnicas realizadas.
Referencias
Alkhayal A, San Gabriel M, Zeidan K, Alrabeeah K, Noel D, McGraw R, et al. Sperm DNA and chromatin integrity in semen samples used for intrauterine insemination. Journal of assisted reproduction and genetics 2013; vol. 30, 11:1519-1524.
Brzechffa PR, Daneshmand S, Buyalos RP. Sequential clomiphene citrate and human menopausal gonadotrophin with intrauterine insemination: the effect of patient age on clinical outcome. Human reproduction (Oxford, England) 1998; vol. 13, 8:2110-2114.
Calderón-Mendoza L, Vivas-Ramírez C, De los Reyes L. Evaluación de las técnicas de capacitación espermática y su efecto en la fragmentación del ADN. Revista Colombiana de Obstetricia y Ginecología 2012; vol. 63, no. 2.
Cortés-Gutiérrez E, Dávila-Rodríguez M, López-Fernández C, Fernández J, Gosálvez J. Evaluación del daño en el DNA espermático. Actas Urológicas Españolas 2007; vol. 31, 2:120-131.
Dodson WC, Moessner J, Miller J, Legro RS, Gnatuk CL. A randomized comparison of the methods of sperm preparation for intrauterine insemination. Fertility and sterility 1998; vol. 70, 3:574-575.
Duran EH, Morshedi M, Taylor S, Oehninger S. Sperm DNA quality predicts intrauterine insemination outcome: a prospective cohort study. Human reproduction (Oxford, England) 2002; vol. 17, 12:3122-3128.
Eggert-Kruse W, Rohr G, Kerbel H, Schwalbach B, Demirakca T, Klinga K, et al. The Acridine Orange test: a clinically relevant screening method for sperm quality during infertility investigation?. Human reproduction (Oxford, England) 1996; vol. 11, 4:784-789.
Golan R, Shochat L, Weissenberg R, Soffer Y, Marcus Z, Oschry Y, et al. Evaluation of chromatin condensation in human spermatozoa: a flow cytometric assay using acridine orange staining. Molecular human reproduction 1997; vol. 3, 1:47-54.
Hammadeh M, Kühnen A, Amer A, Rosenbaum P, Schmidt W. Comparison of sperm preparation methods: effect on chromatin and morphology recovery rates and their consequences on the clinical outcome after in vitro fertilization embryo transfer. International journal of andrology 2001; vol. 24, 6:360-368.
Jayaraman V, Upadhya D, Narayan PK, Adiga SK. Sperm processing by swim-up and density gradient is effective in elimination of sperm with DNA damage. Journal of assisted reproduction and genetics 2012; vol. 29, 6:557-563.
Karabinus DS, Gelety TJ. The impact of sperm morphology evaluated by strict criteria on intrauterine insemination success. Fertility and sterility 1997; vol. 67, 3:536-541.
Kazerooni T, Asadi N, Jadid L, Kazerooni M, Ghanadi A, Ghaffarpasand F, et al. Evaluation of sperm’s chromatin quality with acridine orange test, chromomycin A3 and aniline blue staining in couples with unexplained recurrent abortion. Journal of assisted reproduction and genetics 2009; vol. 26, 11-12:591-596.
Kim H, Kang MJ, Kim S.A, Oh SK, Kim H, Ku S, et al. The utility of sperm DNA damage assay using toluidine blue and aniline blue staining in routine semen analysis", Clinical and experimental reproductive medicine 2013; vol. 40, 1:23-28.
Liu DY, Baker, HW. Human sperm bound to the zona pellucida have normal nuclear chromatin as assessed by acridine orange fluorescence", Human reproduction (Oxford, England) 2007; vol. 22, 6:1597-1602.
Merviel P, Heraud MH, Grenier N, Lourdel E, Sanguinet P, Copin H. Predictive factors for pregnancy after intrauterine insemination (IUI): an analysis of 1038 cycles and a review of the literatura. Fertility and sterility 2010; vol. 93, 1:79-88.
Morshedi M, Duran HE, Taylor S, Oehninger S. Efficacy and pregnancy outcome of two methods of semen preparation for intrauterine insemination: a prospective randomized study. Fertility and sterility 2003; vol. 79, 1625-1632.
Prakash P, Leykin L, Chen Z, Toth T, Sayegh R, Schiff I, et al. Preparation by differential gradient centrifugation is better than swim-up in selecting sperm with normal morphology (strict criteria). Fertility and sterility 1998; vol. 69, 4:722-726.
Ricci G, Perticarari S, Boscolo R, Montico M, Guaschino S, Presani G. Semen preparation methods and sperm apoptosis: swim-up versus gradient-density centrifugation technique. Fertility and sterility 2009; vol. 91, 2:632-638.
Soler C, Gassner P, Nieschlag E, de Montserrat J, Gutiérrez R, Sancho M, et al. Utilización del Integrated Semen Analysis System (ISAS) para el análisis morfométrico espermático humano y su significado en las técnicas de reproducción asistida. Revista Internacional de Andrología 2005; vol. 3, 3:112-119.
Van der Zwalmen P, Bertin-Segal G, Geerts L, Debauche C, Schoysman R. Sperm morphology and IVF pregnancy rate: comparison between Percoll gradient centrifugation and swim-up procedures. Human reproduction (Oxford, England) 1991; vol. 6, 4:581-588.
Van Waart J, Kruger TF, Lombard CJ, Ombelet W. Predictive value of normal sperm morphology in intrauterine insemination (IUI): a structured literature review. Human reproduction 2001; vol. 7, 5:495-500.
Wainer R, Albert M, Dorion A, Bailly M, Bergere M, Lombroso R, et al. Influence of the number of motile spermatozoa inseminated and of their morphology on the success of intrauterine insemination. Human reproduction (Oxford, England) 2004; vol. 19, 9:2060-2065.
Zapardiel Gutiérrez I, De La Fuente Valero J, Álvarez Álvarez P, Martínez-Lara A, Herrero Gámiz S. Sperm morphology, female age and hormonal levels as successful predictors in intrauterine insemination. Revista Iberoamericana de Fertilidad 2007; vol. 24, no. 6.
Zini A, Finelli A, Phang D, Jarvi, K. Influence of semen processing technique on human sperm DNA integrity. Urology 2000; vol. 56, 6:1081-1084.