SCREENING GENÉTICO PREIMPLANTACIONAL (PGS) POR FACTOR MASCULINO. ANÁLISIS MEDIANTE DOS TÉCNICAS: FISH Y a-CGH
Lluc Coll1, Mònica Parriego1*, Montserrat Boada1, Josep Mª Vendrell1, Bonaventura Coroleu1 y Anna Veiga1,2
1 Salud de la Mujer Dexeus. Hospital Universitario Quirón Dexeus. Gran Via Carles III, 71-75, 08028, Barcelona
2 Banco de Líneas Celulares. Centro de Medicina Regenerativa de Barcelona. Dr. Aiguader, 88, 08003, Barcelona
La indicación de screening genético preimplantacional (PGS) por factor masculino de origen genético ha sido poco estudiada a pesar de suponer el 9% de los casos reportados en el registro de la Sociedad Europea de Reproducción Humana y Embriología (ESHRE PGD Consortium). En el presente estudio se han evaluado los resultados de los ciclos de PGS por factor masculino genético en dos series distintas: una serie de 73 casos en la que se utilizó la técnica de hibridación in situ fluorescente (FISH) para el análisis genético y otra de 55 casos en los que el análisis cromosómico se realizó mediante arrays de hibridación genómica comparativa (a-CGH). Se ha observado un mayor poder de detección de anomalías cromosómicas en el grupo de a-CGH, lo que ha supuesto un porcentaje inferior de ciclos con transferencia en este grupo. No obstante, las tasas de implantación y embarazo se han visto significativamente mejoradas en el grupo de a-CGH. A día de hoy, la aplicación de PGS mediante análisis cromosómico completo (CCS) en el grupo de pacientes con factor masculino genético ofrece unos resultados muy positivos que validan su aplicación.
Introducción
A principios de los años 90 se describió la técnica de screening genético preimplantacional (PGS) en embriones humanos (Munné et al., 1993). Su aplicación supuso una alternativa para un gran grupo de parejas procedentes de ciclos de fecundación in vitro (FIV) de mal pronóstico. En dichas parejas, el PGS tiene como objetivo mejorar las tasas de implantación y reducir las tasas de aborto y concepciones afectas de cromosomopatías gracias a la posibilidad de seleccionar los embriones con una carga cromosómica normal (Gianaroli et al., 1997).
La técnica de análisis citogenético utilizada en PGS desde sus inicios fue la hibridación in situ fluorescente (FISH). Esta metodología presenta el gran inconveniente de no poder analizar todos los cromosomas debido a la limitación en el número de sondas fluorescentes y la pérdida de eficiencia en caso de realizar rondas sucesivas de hibridación sobre una misma muestra.
El PGS-FISH se comenzó a aplicar clínicamente en los centros de reproducción asistida sin demasiados estudios clínicos que ratificaran su utilidad. Por este motivo, la publicación de estudios determinando un efecto negativo del PGS sobre las tasas de embarazo evolutivo y niño nacido en mujeres de edad materna avanzada (Mastenbroek et al., 2007; Mastenbroek et al., 2011), sembró la duda en la comunidad científica en relación al PGS. Aún así, cabe decir que existe mucha controversia sobre la validez de estos estudios, y varios grupos de valía contrastada los ponen en duda aludiendo a deficiencias metodológicas (Rubio et al., 2009).
Recientemente, las técnicas de análisis cromosómico completo (CCS) han sido optimizadas permitiendo el análisis de una sola célula y la obtención de resultados en poco tiempo, suponiendo una nueva vía para el estudio de aneuploidías en embriones preimplantacionales. La gran ventaja que ofrece esta tecnología respecto al FISH es la capacidad de analizar todos los cromosomas de una forma exhaustiva. Actualmente, la técnica de arrays de hibridación genómica comparativa (a-CGH) está validada para PGS y es de extensa aplicación en la práctica clínica. No obstante, la comunidad científica es cautelosa y pide más estudios para confirmar el beneficio de su aplicación en reproducción asistida (Rubio et al., 2013)
Los pacientes con un factor masculino de origen genético han sido propuestos como un grupo candidato a beneficiarse del PGS. Aunque no es, en cuanto a número, una de la principales indicaciones para la realización de un PGS representa alrededor de un 9% de los casos descritos en el registro de la ESHRE (Moutou et al., 2014). Varios estudios han descrito un aumento significativo de anomalías meióticas en pacientes con oligozoospermia (Vendrell et al., 1999; Sarrate et al., 2010), así como un aumento en el número de embriones cromosómicamente anómalos en ciclos de PGS con esta indicación (Aran et al., 2004).
El objetivo de este trabajo ha sido evaluar los resultados obtenidos en ciclos de PGS con análisis cromosómico completo mediante a-CGH y los obtenidos anteriormente con la técnica de FISH.
Material y métodos
Se han incluido un total de 128 ciclos de PGS realizados hasta junio de 2014.
La indicación para el PGS fue el diagnóstico de un factor masculino de origen genético mediante estudio directo de meiosis testicular o mediante un FISH espermático. Todos los pacientes tenían un cariotipo normal con un estudio de microdeleciones del cromosoma Y negativo y presentaban oligozoospermia.
Los protocolos de estimulación ovárica y de cultivo de gametos y embriones fueron los habituales de nuestro centro.
Todos los embriones con ≥5 células en D+3 y <30% de fragmentación fueron considerados aptos para la biopsia.
La biopsia se realizó en D+3 con disección de la zona pelúcida mediante termólisis (Boada et al., 1998) y aspiración de un único blastómero. El análisis cromosómico se realizó mediante la técnica de FISH para 8 cromosomas (13, 15, 16, 18, 21, 22, X, Y) de acuerdo con los procedimientos estándares, o bien mediante a-CGH siguiendo el protocolo descrito por el fabricante (BlueGnome, UK). La transferencia de los embriones diagnosticados como normales se realizó en día +5 del desarrollo.
Los datos obtenidos para cada grupo del estudio (FISH o a-CGH) se compararon entre sí mediante las pruebas estadísticas de Mann-Whitney y Chi-Cuadrado.
Resultados
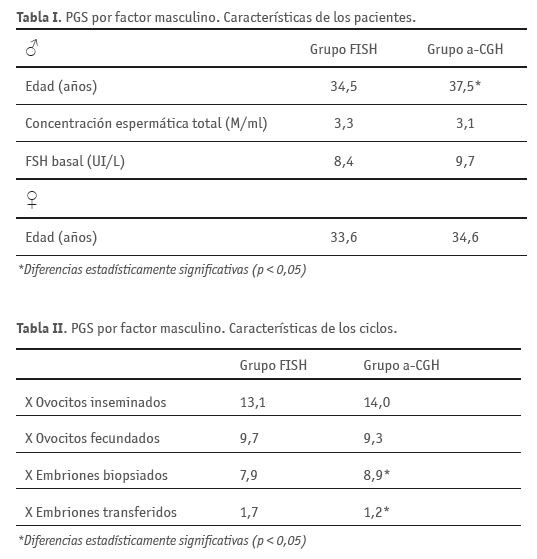
Las características clínicas de los pacientes masculinos de los dos grupos analizados no mostraron diferencias significativas a excepción de la edad, que resultó superior en el grupo de pacientes de la serie de CCS (Tabla I). La edad de la mujer fue similar en ambos grupos.
El número de ovocitos inseminados y fecundados fue equivalente en los dos grupos aunque se biopsiaron significativamente más embriones en el grupo de análisis cromosómico completo (Tabla II).
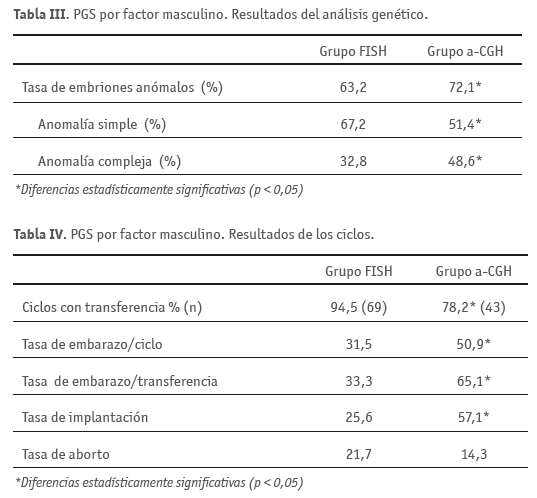
El análisis de todos los cromosomas llevó a la detección de un mayor porcentaje de embriones cromosómicamente anómalos: 72,1% de embriones anormales en el grupo de a-CGH vs 63,2% de embriones anómalos diagnosticados mediante FISH. También resultó superior el porcentaje de embriones con anomalías cromosómicas complejas (anomalías en ≥3 cromosomas) en el grupo de CCS en comparación con el de FISH (Tabla III). En consecuencia, la media de embriones transferidos resultó significativamente inferior en el grupo de a-CGH respecto al grupo de FISH (1,3 vs 1,7). También resultó inferior el porcentaje de ciclos que llegaron a transferencia embrionaria (78,2% vs 94,5%).
Las tasas de embarazo por ciclo fueron del 31,5% en el grupo de FISH y del 50,9% en el grupo de análisis cromosómico completo, y por transferencia del 33,3% y del 65,1% respectivamente, observándose diferencias estadísticamente significativas en ambos casos. No se observaron diferencias en las tasas de aborto entre grupos (Tabla IV).
Discusión
Las publicaciones que se centran en la evaluación de los resultados PGS para indicaciones concretas son escasas (Greco et al., 2014), especialmente en el caso de factor masculino. Por este motivo, pensamos que nuestro trabajo aporta datos precisos que pueden ser de utilidad clínica.
Los resultados obtenidos confirman que el análisis de todos los cromosomas aumenta el porcentaje de embriones diagnosticados como aneuploides en comparación con el análisis cromosómico parcial realizado mediante la técnica de FISH. Los resultados de PGS publicados en el registro ESHRE-2009 (Moutou et al., 2014) por factor masculino y analizados mediante FISH mostraron un porcentaje de anomalías cromosómicas del 58%, comparable al que hemos obtenido nosotros mediante la misma técnica (63,2%), e inferior al 72,1% que hemos detectado mediante a-CGH. Cabe destacar que en el grupo de a-CGH se observó una mayor edad de los pacientes masculinos respecto al grupo de FISH. No obstante, la diferencia de edad media entre ambos grupos es únicamente de 3 años y además, no hay evidencias de un aumento de aneuploidías en espermatozoides en edades crecientes (Martin et al., 2008), por lo que la detección de más embriones aneuploides con CCS no estaría relacionada con la mayor edad de los varones sino que lo atribuimos a un mayor poder de detección de la técnica de a-CGH. Así, aunque con el FISH ya se podía diagnosticar una elevada proporción de los embriones anormales, entre un 10-15% de los embriones habrían sido clasificados erróneamente como transferibles. También el CCS aumenta la proporción de embriones con anomalías complejas. Por lo tanto, el análisis de todos los cromosomas permite una caracterización citogenética más estricta y una mejor selección de los embriones euploides para la transferencia.
Como consecuencia de una mayor detección de anomalías cromosómicas en los embriones, tanto el porcentaje de ciclos que llegan a transferencia embrionaria como el número medio de embriones transferidos por ciclo son menores en el grupo de a-CGH. Esta diferencia también se confirma al comparar nuestros datos del grupo de a-CGH con los resultados de otras series mediante FISH (Aran et al., 2004; Moutou et al., 2014). En este sentido, estos resultados refuerzan la necesidad de informar a los pacientes de la probabilidad de no disponer de embriones aptos para transferir (22,8%) antes de iniciar el ciclo.
En el grupo de a-CGH observamos un incremento importante en las tasas de gestación por ciclo (50,9% vs 31,5%) y por transferencia (65,1% vs 33,3%) a pesar de realizar menos transferencias y transferir un número menor de embriones. Aunque en la serie analizada la tasa de embarazo obtenida en el grupo de FISH fue ligeramente inferior a la reportada por la ESHRE (Moutou et al., 2014) y a la obtenida por nuestro grupo en una serie previa (Aran et al., 2004) consideramos que aplicando la técnica de a-CGH la optimización de los resultados es indiscutible. Con una mejor selección del embrión a transferir, las tasas de implantación se duplican (57,1 vs 25,6% en el grupo FISH), incremento que también se observa respecto a los datos obtenidos en los estudios anteriormente citados.
Es importante señalar que en los casos de PGS mediante a-CGH por factor masculino severo, la elevada probabilidad de implantación de los embriones euploides refuerza la conveniencia de transferir un único embrión con el fin de minimizar el riesgo de embarazo múltiple.
Una de las principales limitaciones de nuestro estudio es que los datos incluidos en los dos grupos no corresponden al mismo periodo de tiempo. A pesar de ello durante toda la etapa analizada las condiciones generales de trabajo y de cultivo no han experimentado grandes cambios, aunque no podemos descartar pequeñas variaciones que hayan podido influenciar en cierto grado en los resultados. El hecho de que para el mismo número de ovocitos fecundados en ambos grupos se hayan podido biopsiar más embriones en el grupo de a-CGH es una prueba de ello.
Actualmente las técnicas de CCS en los ciclos de PGS están sustituyendo por completo la técnica de FISH y deben ser de elección en los centros de reproducción asistida. En la mayoría de estudios publicados, la biopsia se realiza en estadio de blastocisto y la transferencia diferida (Schoolcraft et al., 2010; Yang et al., 2012; Rubio et al., 2013). En nuestra serie, la biopsia se ha realizado en D+3 y la transferencia en fresco dos días más tarde. No obstante, los resultados en cuanto a tasas de implantación y embarazo obtenidos en el grupo de a-CGH son muy buenos. Es probable que a partir de ahora sea más frecuente retardar el momento de la biopsia con la intención de minimizar el daño al embrión, tener más robustez en el diagnóstico y optimizar los recursos.
Los resultados obtenidos nos muestran que la realización de PGS mediante CCS en el grupo de pacientes con factor masculino de origen genético ofrece resultados satisfactorios que, a día de hoy, validan y justifican su aplicación. Sería conveniente la realización de estudios prospectivos aleatorizados para confirmar los beneficios de la aplicación del PGS en este grupo de pacientes.
Referencias
Bibliografía
Aran B, Veiga A, Vidal F, Parriego M, Vendrell JM, Santaló J, et al. Preimplantation genetic diagnosis in patients with male meiotic abnormalities. Reprod Biomed Online 2004; 8:470-476.
Boada M, Carrera M, De la Iglesia C, Sandalinas M, Barri PN, Veiga A. Successful use of a Laser for Human Embryo Biopsy in Preimplantation Genetic Diagnosis: Report of Two Cases. J Assist Reprod Genet 1998; 15:302-307
Greco E, Bono S, Ruberti A, Lobascio AM, Greco P, Biricik A, et al. Comparative Genomic Hybridization Selection of Blastocysts for Repeated Implantation Failure Treatment: A Pilot Study. Biomed Res Int 2014; 2014:457913
Gianaroli L, Magli MC, Ferraretti AP, Fiorentino A, Garrisi J, Munné S. Preimplantation genetic diagnosis increases the implantation rate in human in vitro fertilization by avoiding the transfer of chromosomally abnormal embryos. Fertil Steril 1997; 68:1128-1131.
Mastenbroek S, Twisk M, Van Echten-Arends J, Sikkema-Raddatz B, Korevaar JC, Verhoeve HR, et al. In Vitro Fertilization with Preimplantation Genetic Screening. N Engl Med 2007; 357:9-17.
Mastenbroek S, Twisk M, Van der Veen F, Repping S. Preimplantation genetic screening: a systematic review and meta-analysis of RCTs. Hum Reprod Update 2011;17:454-466.
Moutou C, Goossens V, Coonen E, De Rycke M, Kokkali G, Renwick P, et al. ESHRE PGD consortium data collection XII: cycles from January to December 2009 with pregnancy follow-up to October 2010. Hum Reprod 2014; 29:880-903.
Munné S, Lee A, Rosenwaks Z, Grifo, J, Cohen J. Diagnosis of major chromosome aneuploidies in human preimplantation embryos. Hum Reprod 1993; 8:2185-2191.
Rubio C, Giménez C, Fernández E, Vendrell X, Velilla E, Parriego M, et al. The importance of good practice in preimplantation genetic screening: critical viewpoints. Hum Reprod 2009; 24:2045-2047.
Rubio C, Rodrigo L, Mir P, Mateu E, Peinado V, Milán M, et al. Use of array comparative genomic hybridization (array-CGH) for embryo assessment: clinical results. Fertil Steril 2013; 99:1044-1048.
Sarrate Z, Vidal F, Blanco J. Role of sperm fluorescent in situ hybridization studies in infertile patients: indications, study approach, and clinical relevance. Fertil Steril 2010; 93:1892-1902.
Schoolcraft WB, Fragouli E, Stevens J, Munné S, Katz-Jaffe, Wells D. Clinical application of comprehensive cromosomal screening at the blastocyst stage. Fertil Steril 2010; 94:1700-1706.
Vendrell JM, García F, Veiga A, Calderón G, Egozcue S, Egozcue J, et al. Meiotic abnormalities and spermatogenic parameters in severe oligoasthenozoospermia. Hum Reprod 1999;14-375-378.
Yang Z, Liu J, Collins GS, Salem SA, Liu X, Lyle SS, et al. Selection of single blastocysts for fresh transfer via standard morphology assessment alone and with array CGH for good prognosis IVF patients: results from a randomized pilot study. Mol Cytogenet 2012; 5:24